Lesiones pseudotumorales del hueso — Actualización 2026: procesos no neoplásicos que simulan tumores óseos
Las lesiones pseudotumorales del hueso constituyen un grupo heterogéneo de procesos no neoplásicos que,
por su aspecto clínico y radiológico, pueden simular tumores óseos benignos o malignos. Reconocerlas evita errores diagnósticos
que llevan a tratamientos innecesarios (cirugías agresivas, radioterapia, quimioterapia) y ayuda a indicar el manejo correcto
(observación, tratamiento médico o cirugía limitada).
Esta página (actualizada a 2026) cubre las entidades más frecuentes: quiste óseo aneurismático, quiste óseo solitario,
ganglión intraóseo, fibroma no osificante, granuloma eosinófilo / LCH, displasia fibrosa,
miositis osificante, tumor pardo y quiste epidermoide intraóseo. Integra claves de imagen, “pitfalls” y,
cuando aporta valor real, genética molecular (p. ej., USP6 en QOA primario; GNAS en displasia fibrosa;
alteraciones de la vía MAPK en LCH).
Ejemplo radiológico
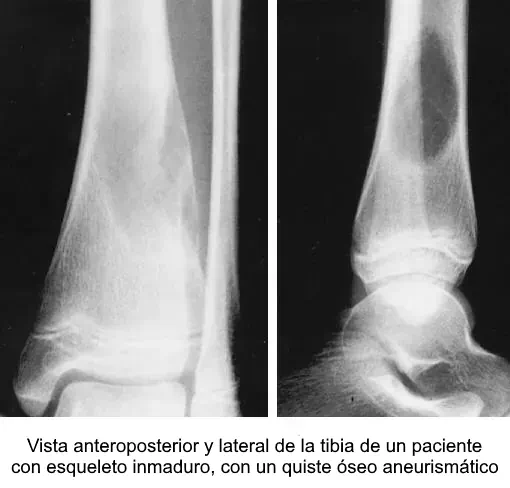
0) Accesos rápidos
Si prefieres leer cada entidad en su página propia, usa estos enlaces. Esta página mantiene el contenido completo y además actúa como punto de entrada con navegación.
1) En 1 minuto
- ✅ Definición: procesos no neoplásicos (reactivos, displásicos, metabólicos, traumáticos, infecciosos) que simulan tumores.
- ✅ Entidades frecuentes:
- 🔹 QOA: expansivo, niveles líquido-líquido; en primarios suele haber reordenamiento/fusión de USP6.
- 🔹 QOS: niño, metáfisis proximal húmero/fémur; “fallen fragment sign” si fractura.
- 🔹 FNO: metafisario, excéntrico, cortical, borde esclerótico; involuciona con la edad.
- 🔹 DF: matriz “vidrio deslustrado”, deformidad (cayado de pastor), mutación GNAS.
- 🔹 LCH (granuloma eosinófilo): vértebra plana, cráneo “beveled edge”; alteraciones de vía MAPK (p. ej. BRAF V600E en una proporción).
- 🔹 Miositis osificante: osificación periférica madura (“cáscara de huevo”), antecedente traumático frecuente.
- 🔹 Tumor pardo: hiperparatiroidismo: PTH elevada (y calcio alterado según contexto).
- ✅ Claves para el diferencial:
- 🔹 Edad + localización mandan (niño metafisario vs adulto epifisario, etc.).
- 🔹 Matriz: DF “vidrio deslustrado” es muy orientativa; QOA/QOS no tienen matriz tumoral.
- 🔹 Expansión: QOA/DF tienden a expandir; QOS suele “adelgazar” sin expansión marcada.
- ✅ Genética (cuando ayuda de verdad):
- 🔹 QOA primario: USP6 (FISH/NGS) apoya el diagnóstico y ayuda en diferenciales.
- 🔹 DF: GNAS (R201) es el hallazgo típico.
- 🔹 LCH: activación MAPK (BRAF/MAP2K1 y otros) puede guiar terapias en refractarios.
2) Conceptos generales
1.1 Definición y clasificación práctica
Las lesiones pseudotumorales son procesos no neoplásicos que simulan tumores. Clasificación útil por mecanismo:
- Quísticas: QOS, QOA, ganglión intraóseo, quiste epidermoide.
- Fibro-óseas: displasia fibrosa (y otras fibro-óseas según contexto).
- Fibrohistiocíticas reactivas: FNO / defectos fibrosos.
- LCH: granuloma eosinófilo (proliferación clonal con vía MAPK activada).
- Postraumáticas: miositis osificante, callo exuberante.
- Metabólicas: tumor pardo del hiperparatiroidismo.
- Infecciosas: osteomielitis crónica / absceso de Brodie (diferencial relevante).
1.2 Por qué importa el diferencial
- Evitar sobretratamiento: muchas no requieren nada (FNO) o se tratan con técnicas limitadas.
- Evitar infratratamiento: algunas (QOA agresivo, DF sintomática) sí requieren intervención.
- Detectar enfermedad sistémica: tumor pardo → buscar hiperparatiroidismo; DF poliostótica → síndromes asociados.
3) Quiste óseo aneurismático (QOA)
2.1 Concepto y epidemiología
- Definición: lesión quística expansiva benigna con espacios sanguíneos separados por tabiques fibrosos con células gigantes y osteoide reactivo.
- Edad: predominio en <20 años.
- Localización: metáfisis de huesos largos y elementos posteriores vertebrales.
- Primario vs secundario: primario (frecuente); secundario a otra lesión (no “dar por hecho” en atípicos).
2.2 Genética molecular (lo útil en práctica)
- USP6: reordenamientos/fusiones en muchos QOA primarios (p. ej., CDH11–USP6 clásico).
- Aplicación: ayuda en diferenciales (p. ej., otras lesiones quísticas con niveles líquido-líquido) y en casos con histología/imágenes dudosas.
- Detección: FISH para USP6 o NGS según disponibilidad.
2.3 Radiología
- Rx: lítica, excéntrica, expansiva, septada; adelgazamiento cortical.
- TC/RM: niveles líquido-líquido (característico, no exclusivo); tabiques con realce.
2.4 Histopatología
- Espacios sanguíneos sin endotelio; tabiques fibrosos con células gigantes, osteoide reactivo y hemosiderina.
- En sospecha de secundario: buscar/biopsiar componente sólido y correlación radio-patológica.
2.5 Tratamiento y pronóstico
- Legrado + relleno (injerto/cemento): estándar; recurrencia variable (más en jóvenes/axial).
- Adyuvantes locales: fenol, crioterapia, argón, etc. según experiencia.
- Escleroterapia (p. ej., polidocanol): útil en localizaciones complejas.
- Embolización: en casos seleccionados o como adyuvante.
- Denosumab: uso selectivo/off-label en casos agresivos/irresecables en centros expertos; vigilar efectos y rebote de calcio al suspender.
4) Quiste óseo solitario (QOS) / Quiste óseo unicameral
3.1 Concepto y epidemiología
- Edad: típico 5–15 años.
- Localización: metáfisis proximal de húmero y fémur.
- Clínica: a menudo incidental; fractura patológica como presentación.
3.2 Radiología
- Rx: lítica, central, geográfica, borde esclerótico; no expansiva (adelgaza la cortical).
- Fallen fragment sign: muy orientativo si hay fractura.
- RM: líquido simple, sin realce sólido.
3.3 Tratamiento
- Observación en pequeños/estables.
- Inyecciones percutáneas (según protocolos locales) o legrado + injerto en sintomáticos/riesgo de fractura.
5) Ganglión intraóseo
- Localización: subcondral/yuxtaarticular (rodilla, acetábulo, carpo/tarso).
- Rx: lítica geográfica, borde esclerótico, a veces multiloculada.
- Tratamiento: legrado + injerto si sintomático; recidiva baja.
6) Fibroma no osificante (FNO) / Defecto fibroso metafisario
5.1 Concepto
- Muy frecuente en niños/adolescentes; defecto de osificación, no neoplasia.
- Rx: excéntrico, cortical, lobulado, borde esclerótico; respeta epífisis.
- Conducta: normalmente observación; tratar si muy grande/riesgo de fractura.
7) Granuloma eosinófilo (Histiocitosis de células de Langerhans)
6.1 Concepto y epidemiología
- Proliferación clonal de células de Langerhans con infiltrado inflamatorio.
- Edad: típica pediátrica.
- Localización: cráneo, mandíbula, columna, costillas, fémur.
6.2 Genética / biología (lo que aporta)
- Alteraciones de la vía MAPK (p. ej., BRAF V600E en una proporción; también MAP2K1 y otras).
- Aplicación: en enfermedad refractaria/extendida puede guiar terapias dirigidas (BRAF/MEK) en centros expertos.
6.3 Radiología
- Cráneo: lesión lítica con “beveled edge” (botón a botón).
- Columna: vértebra plana (colapso cuerpo vertebral con arco posterior relativamente respetado).
- Diáfisis: lítica con reacción perióstica; diferencial con osteomielitis/Ewing.
6.4 Tratamiento (marco general)
- Lesión única: observación / curetaje / corticoide intralesional según localización.
- Multisistémica o refractaria: manejo por unidades expertas (protocolos y, en seleccionados, terapias dirigidas).
8) Displasia fibrosa (DF)
7.1 Concepto
- Lesión fibro-ósea benigna por mutación postcigótica GNAS.
- Formas monostótica y poliostótica; asociación a McCune-Albright en algunos casos.
7.2 Imagen
- Rx/TC: matriz “vidrio deslustrado”, expansión y deformidades.
- RM: variable; correlación con TC útil para confirmar matriz.
7.3 Tratamiento
- Observación si asintomática; manejo del dolor y prevención de fracturas.
- Cirugía en deformidades/fracturas/riesgo mecánico.
9) Miositis osificante (osificación heterotópica postraumática)
8.1 Imagen clave
- Osificación periférica madura (“cáscara de huevo”); plano de separación con la cortical.
- TC: muy útil (halo radiolúcido separando la lesión del hueso adyacente).
8.2 Diferencial importante
- Osteosarcoma parosteal y osteosarcoma extraesquelético (si duda: correlación clínica + imagen + circuito experto).
10) Tumor pardo del hiperparatiroidismo
9.1 Clave diagnóstica
- Lesiones líticas (a veces múltiples) + contexto bioquímico: pedir PTH, calcio, fósforo, FA.
- Tratamiento: corregir el hiperparatiroidismo → la lesión suele involucionar.
11) Quiste epidermoide intraóseo
- Típico de falange distal; postraumático/implantación.
- Legrado: curativo en la mayoría.
12) Algoritmo diagnóstico
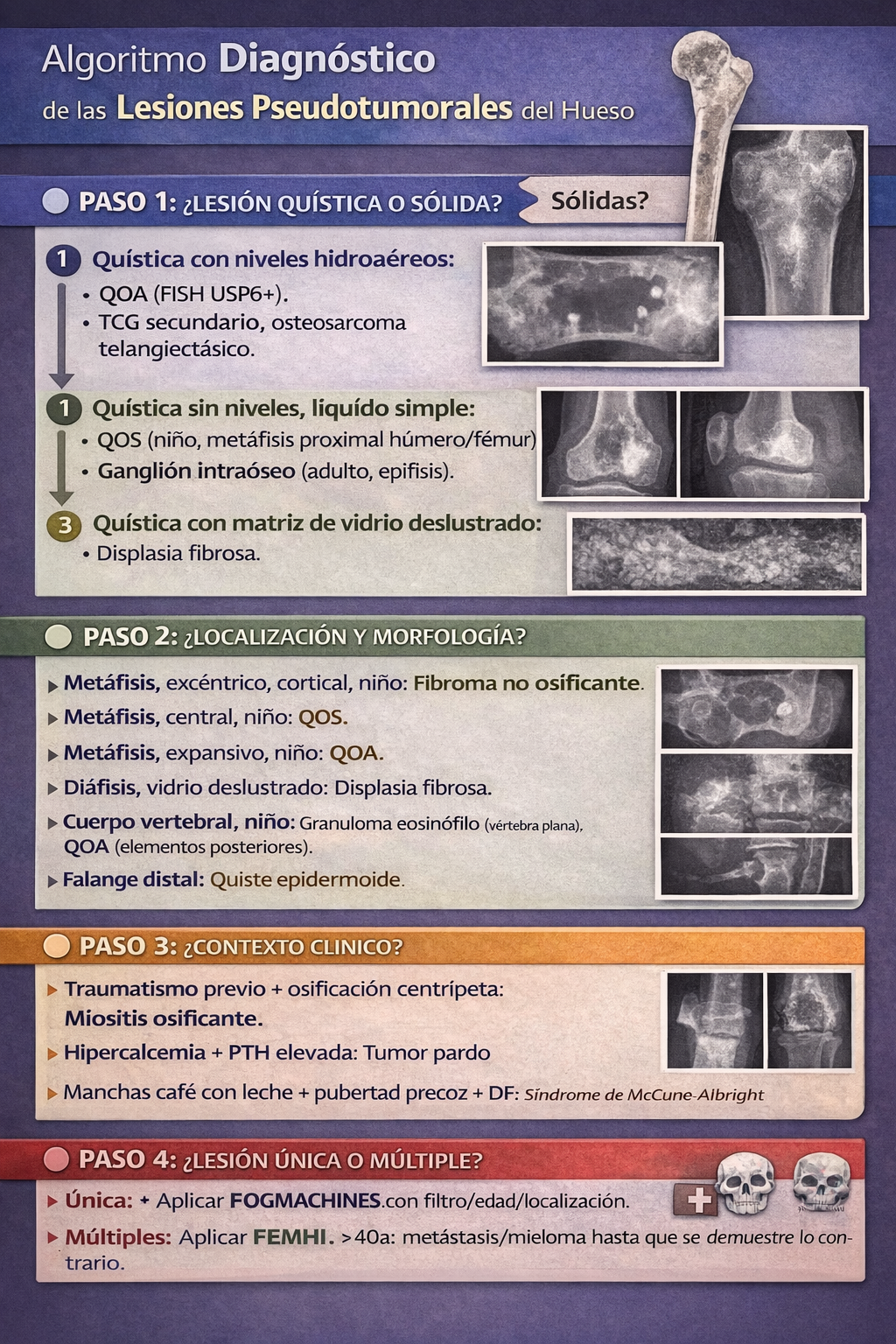
📌 Resumen para la práctica clínica
Indicaciones
- ✅ Radiografía simple en dos proyecciones: base del diagnóstico diferencial.
- ✅ RM (± contraste): tabiques/realce, extensión medular y partes blandas, y caracterización de niveles líquido-líquido.
- ✅ TC: matriz (vidrio deslustrado/osificación), cortical, nidus, y miositis osificante (halo).
- ✅ Laboratorio: Ca/P/PTH/FA (tumor pardo) según sospecha.
- ✅ Biopsia core en casos atípicos (edad/localización no típica, crecimiento, agresividad) y siempre planificada.
- ✅ Estudios moleculares selectivos: USP6 (QOA primario) y GNAS (DF) cuando aporten valor real.
Técnica
- 🔧 Radiografía: patrón de destrucción, matriz y localización.
- 🔧 RM: T1, T2/STIR, ± contraste; valorar tabiques y componente sólido real.
- 🔧 TC: cortes finos y reconstrucciones; técnica clave en osificación heterotópica.
- 🔧 Biopsia: incluir zonas sólidas; evitar áreas puramente quísticas si se sospecha lesión subyacente.
Riesgos
- ⚠️ Asumir “QOA primario” y pasar por alto una lesión subyacente (QOA secundario).
- ⚠️ Biopsiar un FNO típico por desconocimiento del patrón radiológico.
- ⚠️ Confundir miositis osificante inmadura con sarcoma y operar de forma inadecuada.
- ⚠️ No pedir PTH/calcio en lesiones líticas múltiples y etiquetar erróneamente como metástasis/mieloma.
Resultados
- ✅ FNO: involuciona espontáneamente; control excelente.
- ✅ QOS: alta tasa de curación con manejo adecuado según riesgo.
- ✅ QOA: buen control local con legrado/adyuvantes o alternativas percutáneas en seleccionados.
- ✅ DF: manejo sintomático y ortopédico; cirugía en deformidad/fractura.
- ✅ LCH ósea: pronóstico generalmente favorable en formas localizadas; manejo especializado si multisistémica.
13) Bibliografía
USP6 and CDH11 identify the neoplastic cell in primary aneurysmal bone cysts. Am J Pathol. 2004;165(5):1773–1780.
Aneurysmal bone cyst: review. Joint Bone Spine. 2022.
Denosumab in aneurysmal bone cysts: case series. Tumori. 2018.
Activating mutations of the stimulatory G protein in McCune–Albright syndrome. N Engl J Med. 1991;325(24):1688–1695.
Fibrous dysplasia/McCune–Albright syndrome. Endocr Rev. 2020;41(2):345–370.
Recurrent BRAF mutations in Langerhans cell histiocytosis. Blood. 2010;116(11):1919–1923.
Langerhans cell histiocytosis: tratamiento basado en quimioterapia y estratificación. 2022.
Imaging of Soft Tissue Tumors. 4th ed. Wolters Kluwer; 2023. (Capítulo: myositis ossificans).
