🔥 Osificación heterotópica / Miositis osificante — Actualización 2026
La osificación heterotópica (OH) y su variante más frecuente, la miositis osificante (MO), son lesiones reactivas benignas en las que se forma hueso maduro en tejidos blandos, generalmente después de un traumatismo (contusión muscular, cirugía, quemadura) o, en ocasiones, sin un desencadenante claro. En el ámbito de la oncología musculoesquelética, estas entidades adquieren una relevancia especial porque en sus fases iniciales pueden simular clínica y radiológicamente un sarcoma, lo que puede llevar a errores diagnósticos y a tratamientos inapropiados. La clave para distinguirlas de una neoplasia maligna reside en el “fenómeno de zonación” (maduración periférica del hueso) y en la evolución temporal característica.
0) Definición práctica y contexto clínico
La osificación heterotópica se define como la formación de hueso maduro fuera del esqueleto, es decir, en tejidos que normalmente no osifican, como el músculo estriado, la fascia, los tendones o el tejido conectivo subcutáneo. Cuando este proceso ocurre dentro del músculo, recibe el nombre clásico de miositis osificante, un término que, aunque históricamente arraigado, es en cierto modo inexacto, ya que el componente inflamatorio (miositis) no es el fenómeno predominante; se trata más bien de una metaplasia ósea reactiva.
Mensaje fundamental: No es un tumor, sino una lesión reactiva benigna. Sin embargo, su presentación clínica y radiológica en fases tempranas puede ser tan llamativa que simule un sarcoma de partes blandas, lo que exige un conocimiento profundo de su evolución natural y de las herramientas diagnósticas que permiten diferenciarlas.
Contextos típicos en los que aparece
- 🔹 Postraumático: es el mecanismo más frecuente. Tras una contusión muscular directa (por ejemplo, en deportistas), un desgarro o un hematoma intramuscular, se desencadena una respuesta reparativa que puede culminar en osificación.
- 🔹 Postquirúrgico: especialmente frecuente después de artroplastias de cadera, donde la manipulación de los tejidos blandos periarticulares puede inducir la formación de hueso heterotópico.
- 🔹 Neurológico: en pacientes con lesiones medulares o traumatismos craneoencefálicos graves, puede aparecer osificación heterotópica neurogénica, a menudo alrededor de grandes articulaciones (cadera, rodilla, hombro).
- 🔹 Quemaduras extensas: el daño tisular generalizado puede ser un desencadenante.
- 🔹 Sin antecedente claro (formas esporádicas): en algunos casos no se identifica un desencadenante evidente, lo que aumenta la dificultad diagnóstica.
1) Presentación clínica y evolución temporal
Curso clínico típico
La evolución de la miositis osificante sigue un patrón temporal característico que, si se conoce, orienta fuertemente al diagnóstico:
- ⏳ Fase inicial (primeras 2-3 semanas): aparece una masa dolorosa, sensible a la palpación, a menudo con aumento de la temperatura local y cierto grado de inflamación. Puede haber limitación funcional. En esta fase, la lesión es clínicamente indistinguible de un hematoma organizado o incluso de un sarcoma en crecimiento rápido.
- ⏳ Fase intermedia (3-8 semanas): el dolor tiende a disminuir, pero la masa se vuelve más firme y palpable. Comienza la calcificación, que suele ser detectable radiológicamente.
- ⏳ Fase de maduración (>8 semanas): la lesión se estabiliza, el dolor desaparece o se hace mínimo, y la masa adquiere una consistencia pétrea. Radiológicamente se observa una osificación bien definida, con un patrón de maduración periférica.
⚠️ Señales de alerta que obligan a descartar un sarcoma
- ⚠️ Crecimiento rápido y progresivo más allá de las 4-6 semanas, sin signos de estabilización.
- ⚠️ Dolor nocturno intenso o dolor que despierta al paciente.
- ⚠️ Síntomas sistémicos inexplicados (fiebre, pérdida de peso).
- ⚠️ Lesión profunda, sin antecedente traumático y con características radiológicas agresivas (destrucción ósea, invasión de planos adyacentes, márgenes mal definidos).
2) Imagen: la clave para el diagnóstico
El diagnóstico de la osificación heterotópica se basa fundamentalmente en la imagen, y la correcta interpretación de los hallazgos según el tiempo de evolución es esencial para evitar errores. Cada técnica aporta información complementaria.
Radiografía simple: el pilar del seguimiento
- 🩻 0–2 semanas: la radiografía suele ser normal o puede mostrar únicamente un aumento de partes blandas inespecífico. La ausencia de calcificaciones en esta fase no descarta el diagnóstico.
- 🩻 2–6 semanas: comienzan a aparecer calcificaciones tenues y mal definidas, que inicialmente pueden ser centrales pero que, con el tiempo, tienden a organizarse en la periferia.
- 🩻 6–8 semanas y posteriores: se hace evidente el patrón de maduración periférica (“fenómeno de zonación” radiológico). Se observa un anillo de hueso maduro en la periferia de la lesión, con un centro relativamente menos mineralizado. Este hallazgo es prácticamente diagnóstico.
Tomografía computarizada (TC): la confirmación definitiva
La TC es superior a la RM para demostrar la presencia de hueso maduro y el patrón de osificación periférica. En una lesión madura, se observa claramente una corteza ósea periférica que rodea un centro de densidad similar a la médula ósea o al tejido fibroso. Además, la TC permite descartar la continuidad con el hueso adyacente, lo que ayuda a diferenciarla de tumores óseos yuxtacorticales.
Recomendación: ante la sospecha de MO/OH, si la radiografía no es concluyente, la TC es la técnica de elección para confirmar el diagnóstico y evitar la realización de una biopsia innecesaria.
Hallazgo radiológico característico
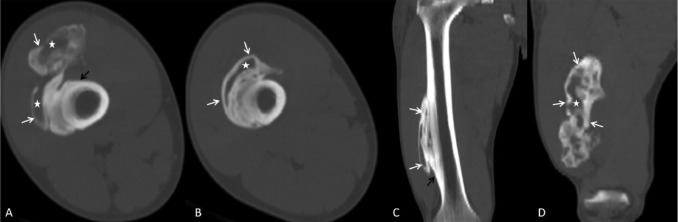
Resonancia magnética (RM): un arma de doble filo
La RM es la técnica que con más frecuencia puede inducir a error si no se correlaciona con la radiografía y la TC. En las fases precoces (2-6 semanas), la lesión muestra un intenso edema y realce tras contraste que puede ser muy llamativo y sugerir un proceso neoplásico agresivo. La masa puede tener bordes mal definidos y la zona central puede mostrar realce, imitando a la perfección un sarcoma.
Clave práctica: nunca se debe interpretar una RM de una masa de partes blandas de aparición reciente sin disponer de una radiografía simple y, preferiblemente, de una TC que demuestre la presencia o ausencia de calcificaciones/osificación periférica. La RM es útil para valorar la relación con estructuras vecinas, pero no para el diagnóstico etiológico.
3) Algoritmo diagnóstico: cómo no perderse
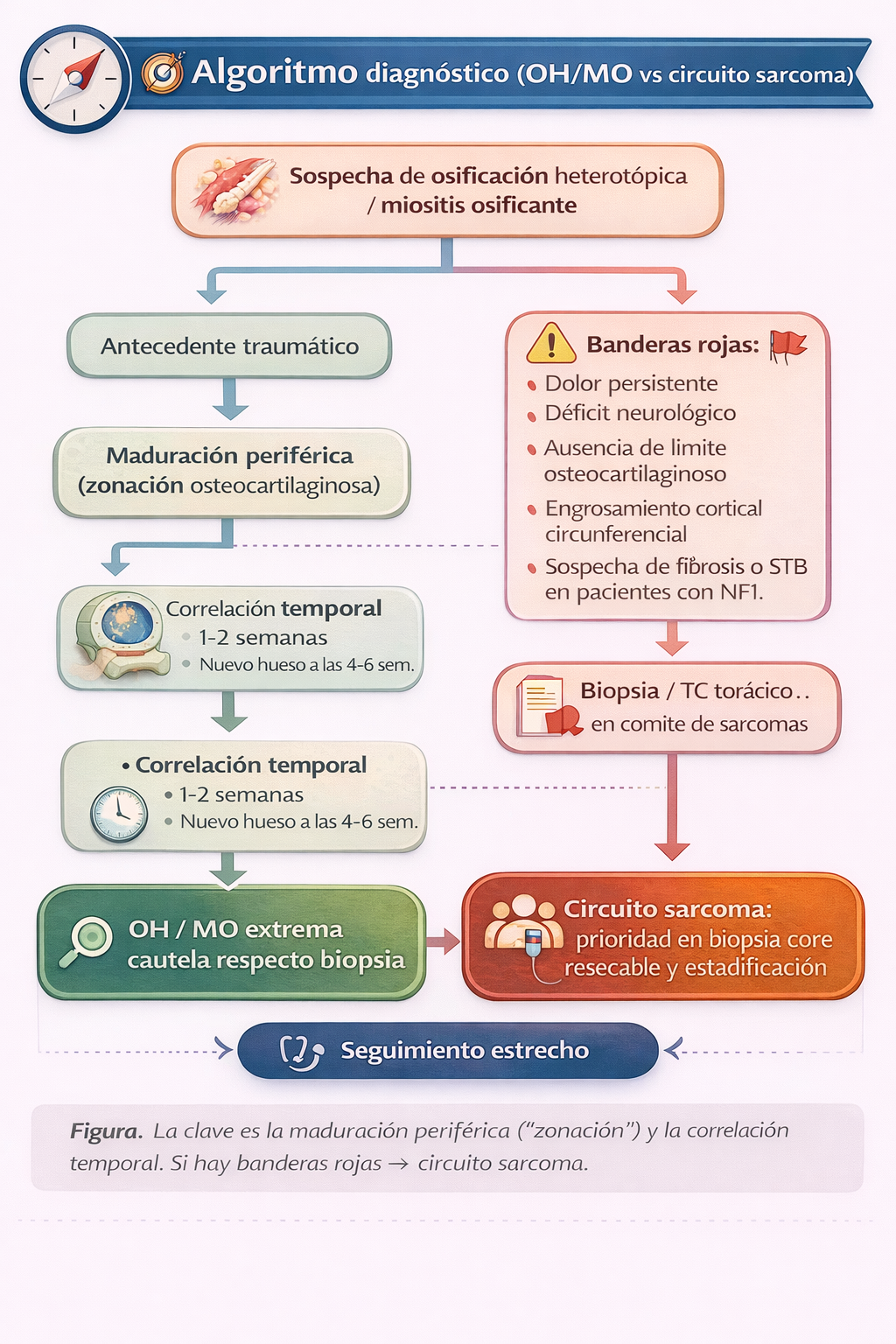
4) Histología: el fenómeno de zonación
Cuando es necesario recurrir a la biopsia (generalmente en casos atípicos o con sospecha de malignidad), el patólogo debe conocer la historia clínica y la imagen para poder interpretar correctamente los hallazgos. El rasgo histológico más característico de la miositis osificante madura es el fenómeno de zonación, una organización centrípeta del tejido que refleja su naturaleza reactiva.
Fenómeno de zonación (de fuera hacia dentro)
- Zona central: compuesta por fibroblastos y miofibroblastos inmaduros, con un estroma laxo y vascular. En las fases muy precoces, esta zona puede mostrar atipia celular y actividad mitótica, lo que puede llevar a un diagnóstico erróneo de sarcoma si se analiza de forma aislada.
- Zona intermedia: contiene osteoide y hueso inmaduro (no lamelar), formado por metaplasia directa del tejido conectivo.
- Zona periférica: constituida por hueso lamelar maduro, bien organizado, que puede incluir incluso médula ósea. Esta maduración periférica es la clave para diferenciarla de los sarcomas productores de osteoide.
⚠️ Pitfall crítico: la biopsia del centro
Si se toma una biopsia con aguja fina o una muestra pequeña que solo alcance la zona central de la lesión en fase precoz, el patólogo puede encontrar una proliferación de células fusiformes con atipia y mitosis, lo que puede inducir al diagnóstico de sarcoma. Por esta razón, si se realiza una biopsia, debe ser guiada por imagen y dirigida a la zona más madura de la lesión (la periferia), y siempre debe interpretarse en conjunto con los hallazgos radiológicos.
5) Diagnóstico diferencial: cómo separar la OH/MO del sarcoma
La tabla siguiente resume las principales entidades que pueden confundirse con una osificación heterotópica, especialmente en las fases precoces o cuando la presentación es atípica.
| Entidad | Clave radiológica / histológica | Cómo se diferencia |
|---|---|---|
| Osteosarcoma extraesquelético | Tumor maligno productor de osteoide, sin patrón de zonación. Crecimiento infiltrativo. | La ausencia de maduración periférica y la presencia de atipia celular franca, mitosis atípicas y necrosis tumoral son características. Clínicamente, suele haber dolor progresivo y masa en aumento. |
| Osteosarcoma parosteal / periosteal | Tumor óseo yuxtacortical, a menudo de bajo grado, adosado a la cortical. | Demostrar la continuidad con la cortical ósea y la ausencia de un plano de separación claro. El osteosarcoma parosteal suele tener un patrón de osificación más homogéneo y una base de implantación amplia. |
| Condrosarcoma extraesquelético con osificación metaplásica | Matriz condroide predominante, con áreas de calcificación en anillos y arcos, y posible osificación metaplásica periférica. | La presencia de matriz cartilaginosa franca y la inmunoexpresión de S100 y SOX9 orientan al condrosarcoma. La osificación, si existe, no sigue el patrón de zonación. |
| Hematoma organizado / calcificado | Masa quística o sólida, con calcificaciones distróficas amorfas, no organizadas en anillo. | La TC muestra calcificaciones irregulares, sin la formación de una verdadera corteza ósea periférica. La evolución clínica suele ser hacia la resolución. |
| Tumor de partes blandas con calcificación (p. ej., sarcoma sinovial) | Calcificaciones punteadas o amorfas en el seno de una masa de partes blandas. | La presencia de otras áreas sólidas con realce, la localización (a menudo yuxtaarticular) y la inmunohistoquímica (TLE1, citoqueratinas) son clave. |
6) Tratamiento: actitud conservadora en la mayoría
Manejo habitual (conservador)
La mayoría de las osificaciones heterotópicas no requieren tratamiento activo más allá del control sintomático. Las medidas generales incluyen:
- ✅ Reposo relativo del área afectada para evitar nuevos traumatismos.
- ✅ Fisioterapia suave y progresiva para mantener el arco de movimiento y prevenir contracturas. Se debe evitar la movilización forzada o los masajes profundos en la fase aguda, ya que podrían perpetuar el proceso inflamatorio.
- ✅ Analgésicos y antiinflamatorios no esteroideos (AINE) para controlar el dolor y la inflamación. Los AINE (especialmente el naproxeno o la indometacina) también se han utilizado para la profilaxis de la OH postquirúrgica, aunque su eficacia en lesiones ya establecidas es limitada.
Tratamiento quirúrgico
La cirugía está indicada en un número limitado de casos:
- 🔪 Dolor persistente que no cede con tratamiento conservador.
- 🔪 Limitación funcional importante (por ejemplo, rigidez articular o atrapamiento nervioso).
- 🔪 Compresión de estructuras vecinas (vasos, nervios).
- 🔪 Duda diagnóstica persistente tras completar el estudio, cuando no se puede descartar una neoplasia maligna.
Si se opta por la resección quirúrgica, es preferible realizarla cuando la lesión está madura y estable (generalmente después de 6-12 meses de evolución), ya que en fases activas el riesgo de recidiva es mayor. La cirugía debe ser completa, pero no es necesario obtener márgenes amplios como en los sarcomas, ya que la lesión es benigna.
Profilaxis en contextos de riesgo (OH postquirúrgica/neurogénica)
La prevención de la osificación heterotópica en pacientes de alto riesgo (cirugía de cadera, lesión medular) no es el objeto principal de este capítulo. No obstante, debe saberse que existen medidas profilácticas como los AINE (indometacina) o la radioterapia local, que se aplican según protocolos específicos.
7) Evolución y seguimiento
- 📈 La evolución natural de la miositis osificante es hacia la estabilización y maduración en un plazo de 3 a 6 meses. La lesión puede disminuir ligeramente de tamaño, pero a menudo queda una osificación residual palpable, aunque asintomática.
- 📈 El dolor y la limitación funcional suelen mejorar progresivamente a medida que la lesión madura.
- 📈 Si tras un período de observación adecuado (3-6 meses) la lesión no muestra signos de maduración, si continúa creciendo o si aparecen nuevos síntomas de alarma, se debe replantear el diagnóstico y considerar la derivación a una unidad de sarcomas.
- 📈 No se requieren controles de imagen rutinarios en lesiones asintomáticas y con diagnóstico firme. En casos dudosos, se puede realizar una radiografía de control a los 3-6 meses para confirmar la maduración.
📌 Resumen para la práctica clínica
Indicaciones
- ✅ Masa de partes blandas, a menudo con antecedente de traumatismo o cirugía, que aparece en las semanas siguientes.
- ✅ Hallazgo radiológico de calcificaciones en tejidos blandos con un patrón de maduración periférica (anillo periférico).
- ✅ Dolor y limitación funcional que mejoran con el tiempo, paralelamente a la maduración radiológica.
Técnica
- 🔧 Radiografía simple inicial y de control a las 2-4 semanas si la lesión es precoz y el diagnóstico no está claro.
- 🔧 TC para confirmar la presencia de osificación periférica madura y descartar otras lesiones.
- 🔧 RM solo indicada si se sospecha afectación de estructuras vecinas o si el diagnóstico diferencial con sarcoma persiste, pero siempre correlacionada con TC/RX.
- 🔧 Biopsia solo si hay dudas razonables tras la imagen, dirigida a la periferia de la lesión y con correlación radio-patológica.
Riesgos
- ⚠️ Sobrediagnosticar un sarcoma si se biopsia la zona central inmadura en una fase precoz.
- ⚠️ Interpretar una RM aislada sin correlación radiológica (RX/TC), lo que puede llevar a confundir el edema y el realce con una neoplasia.
- ⚠️ Realizar una resección quirúrgica precoz en fase activa, lo que aumenta el riesgo de recidiva local.
Resultados
- ✅ El pronóstico es excelente; la mayoría de los casos se resuelven o estabilizan sin secuelas funcionales.
- ✅ El reconocimiento del patrón de maduración periférica evita biopsias y cirugías innecesarias.
- ✅ La cirugía, cuando está indicada (síntomas mecánicos, duda diagnóstica), tiene buenos resultados si se realiza en fase madura.
8) Bibliografía recomendada
📘 Radiología y diagnóstico diferencial
- 📄 Lacout A, Jarraya M, Marcy P-Y, Thariat J, Carlier RY. Myositis ossificans imaging: keys to successful diagnosis. Indian J Radiol Imaging. 2012;22(1):35-39. PMCID: PMC3354355
- 📄 Kransdorf MJ, Meis JM, Jelinek JS. Myositis ossificans: MR appearance with radiologic-pathologic correlation. AJR Am J Roentgenol. 1991;157(6):1243-1248. PMID: 1950874
- 📄 Parikh J, Hyare H, Saifuddin A. The imaging features of post-traumatic myositis ossificans, with emphasis on MRI. Clin Radiol. 2002;57(12):1058-1066. PMID: 12475528
- 📄 Amendola MA, Glazer GM, Agha FP, Francis IR, Weatherbee L, Martel W. Myositis ossificans circumscripta: computed tomographic diagnosis. Radiology. 1983;149(3):775-779. PMID: 6647854
📑 Series clínicas y revisión
- 📄 Walczak BE, Johnson CN, Howe BM. Myositis Ossificans. J Am Acad Orthop Surg. 2015;23(10):612-622. doi:10.5435/JAAOS-D-14-00269
- 📄 Bégué T, Masquelet AC, Doursounian L, Saillant G. Myositis ossificans: a report of 12 cases. Rev Chir Orthop Reparatrice Appar Mot. 1995;81(5):438-445. (Artículo clásico).
- 📄 McCarthy EF, Sundaram M. Heterotopic ossification: a review. Skeletal Radiol. 2005;34(10):609-619. doi:10.1007/s00256-005-0958-z
🌐 Recursos en línea
- 📄 Radiopaedia.org. Myositis ossificans. Ficha completa
- 📄 StatPearls [Internet]. Myositis Ossificans. NCBI Bookshelf
