Quiste Óseo Aneurismático (QOA) — Actualización 2026
Lesión ósea benigna, expansiva y osteolítica, caracterizada por espacios quísticos llenos de sangre separados por septos fibrosos que contienen células gigantes osteoclásticas y osteoide reactivo. Se clasifica como una neoplasia de comportamiento intermedio (localmente agresiva) con tendencia a la recidiva local, pero sin potencial metastásico. El hallazgo de fusiones génicas que implican USP6 refuerza su naturaleza neoplásica y ayuda en casos difíciles (especialmente frente a mimickers críticos).
1) Conceptos y clasificación (WHO 2020/2023; práctica)
1.1 Definición (OMS)
Quiste óseo aneurismático (QOA): neoplasia benigna localmente agresiva compuesta por espacios quísticos hemorrágicos de paredes delgadas, separados por septos fibrosos con células gigantes multinucleadas, osteoide reactivo y estroma fibromixoide. Las células estromales mononucleares albergan fusiones génicas recurrentes que implican USP6 en gran parte de los casos primarios.
1.2 Clave práctica
Mensaje práctico:
- ✅ El QOA es benigno pero localmente agresivo y con recidiva si el tratamiento intralesional es insuficiente.
- ✅ El QOA primario suele ser una lesión de fusión USP6; el secundario depende de la lesión subyacente.
- ✅ En casos atípicos o agresivos, FISH/NGS para USP6 ayuda a confirmar y a excluir mimickers peligrosos.
1.3 En 1 minuto
- ✅ Edad: niños y adultos jóvenes (~80% < 20 años; pico 10–20). Muy raro en >30.
- ✅ Localización: metáfisis huesos largos (fémur distal, tibia proximal, húmero proximal), columna (elementos posteriores), pelvis.
- ✅ Clínica: dolor progresivo, tumefacción; fractura patológica ~10–20%.
- ✅ Imagen: lesión lítica expansiva “soplante” con septos; en RM niveles líquido–líquido frecuentes (orientan, no exclusivos).
- ✅ Recidiva: ~10–30% (más si curetaje simple; menos con curetaje extendido + adyuvantes/fresado).
- ✅ Tratamiento: curetaje intralesional + fresa alta velocidad ± adyuvantes + relleno; alternativas selectivas: escleroterapia/embolización; denosumab en casos agresivos/recurrentes (off-label).
2) Epidemiología
| Parámetro | Datos | Comentario práctico |
|---|---|---|
| Frecuencia | ~1–2% de tumores óseos primarios | Raro, pero típico en población pediátrica y juvenil |
| Edad | ~80% < 20 años (pico 10–20) | En >30 años, pensar en QOA secundario y buscar lesión primaria |
| Sexo | Ligero predominio femenino (≈1,2:1) | |
| Localización |
|
Puede cruzar fisis y afectar epífisis en casos seleccionados |
Regla de oro: QOA en paciente >30 años → sospechar QOA secundario (p. ej., sobre TCG) y descartar lesión subyacente.
3) Clínica
3.1 Presentación típica
- ✅ Dolor progresivo (semanas/meses)
- ✅ Tumefacción / masa por expansión ósea
- ✅ Fractura patológica ~10–20% (forma de presentación en algunos casos)
- ✅ Columna: dolor + síntomas neurológicos (radiculopatía/mielopatía) si compromiso canal
3.2 Red flags (revisar diagnóstico)
- ⚠️ Dolor nocturno intenso, crecimiento muy rápido, o masa de partes blandas prominente
- ⚠️ Patrón radiológico muy agresivo (permeativo) o reacción perióstica “sarcomatosa”
- ⚠️ Histología con atipia marcada / mitosis atípicas → descartar osteosarcoma telangiectásico
4) Imagen (precisión y correlación)
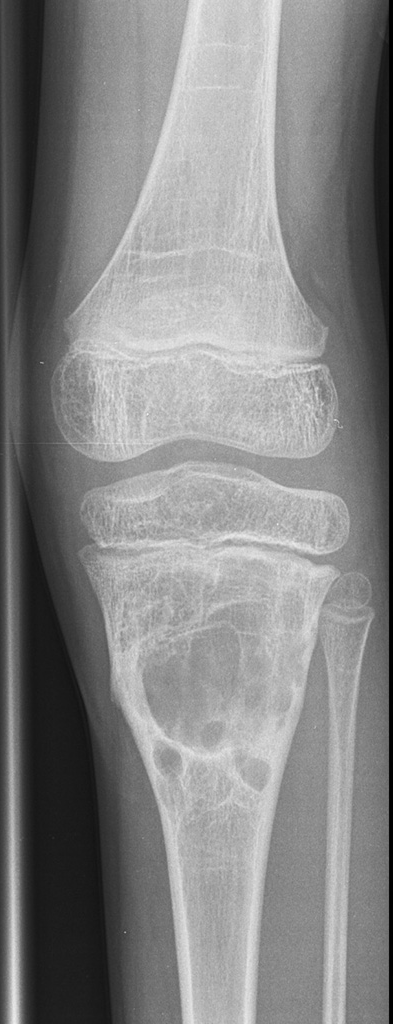
4.1 Radiografía / TC
Hallazgos típicos:
- 🔹 Lesión lítica excéntrica metafisaria
- 🔹 Expansiva “soplante / pompa de jabón”, con adelgazamiento cortical (a veces discontinuidad)
- 🔹 Septos internos (patrón trabeculado)
- 🔹 Sin matriz mineralizada típica (calcificaciones, en general ausentes)
- 🔹 En columna: expansiva en arco posterior; puede comprometer canal
TC es especialmente útil en pelvis/columna para cortical y planificación; puede mostrar niveles líquido–líquido, pero RM es superior.
Hallazgo radiológico característico
4.2 RM
| Secuencia | Patrón frecuente | Pista útil |
|---|---|---|
| T1 | Variable; septos más hipointensos | Define extensión medular/partes blandas |
| T2/STIR | Hiperintenso con niveles líquido–líquido frecuentes | Orientan, no son exclusivos de QOA |
| Post-contraste | Realce de septos y pared; cavidades no realzan | Arquitectura quística |
Nota: niveles líquido–líquido también pueden verse en OST, TCG, condroblastoma y metástasis. La RM ayuda, pero la biopsia es obligatoria si hay atipia clínica/radiológica.
4.3 Medicina nuclear / PET
Puede haber captación periférica con centro relativamente fotopénico; el SUV en PET puede ser variable y no discrimina benignidad/malignidad. Útil solo en escenarios seleccionados.
Protocolo práctico: 1) Rx. 2) RM con contraste. 3) TC si pelvis/columna. 4) Biopsia guiada por imagen si duda diagnóstica o patrón agresivo.
5) Genética e inmunohistoquímica (lo útil de verdad)
5.1 Alteración molecular característica
Reordenamientos de USP6: frecuentes en QOA primario. Habitualmente corresponden a fusiones con genes promotores que inducen sobreexpresión de USP6 y favorecen proliferación/angiogénesis/osteoclastogénesis.
5.2 QOA primario vs secundario
| Entidad | Molecular | Implicación práctica |
|---|---|---|
| QOA primario | Reordenamiento USP6 frecuente | Apoya diagnóstico en casos atípicos |
| QOA secundario | Habitualmente sin reordenamiento USP6 | Buscar y tratar lesión subyacente |
En >30 años, el diagnóstico de QOA debe hacer buscar lesión primaria subyacente (especialmente TCG si es epifisario/subarticular).
5.3 Qué pedir (práctico)
- ⚠️ FISH (break-apart) para USP6 cuando el caso es atípico, agresivo o la biopsia es limitada.
- ⚠️ NGS/RNA-seq si el laboratorio lo ofrece (útil en diferenciales complejos).
- ⚠️ Útil para diferenciar de osteosarcoma telangiectásico (que típicamente no muestra reordenamiento USP6).
5.4 IHQ / Patología (resumen)
- ✅ IHQ: orientativa e inespecífica (CD68 en células gigantes; SATB2 en osteoide reactivo).
- ✅ Microscopía: cavidades hemorrágicas sin revestimiento endotelial + septos con células gigantes irregulares + osteoide reactivo. Ausencia de atipia marcada/mitosis atípicas (si existen → descartar OST).
6) Algoritmo diagnóstico integrado
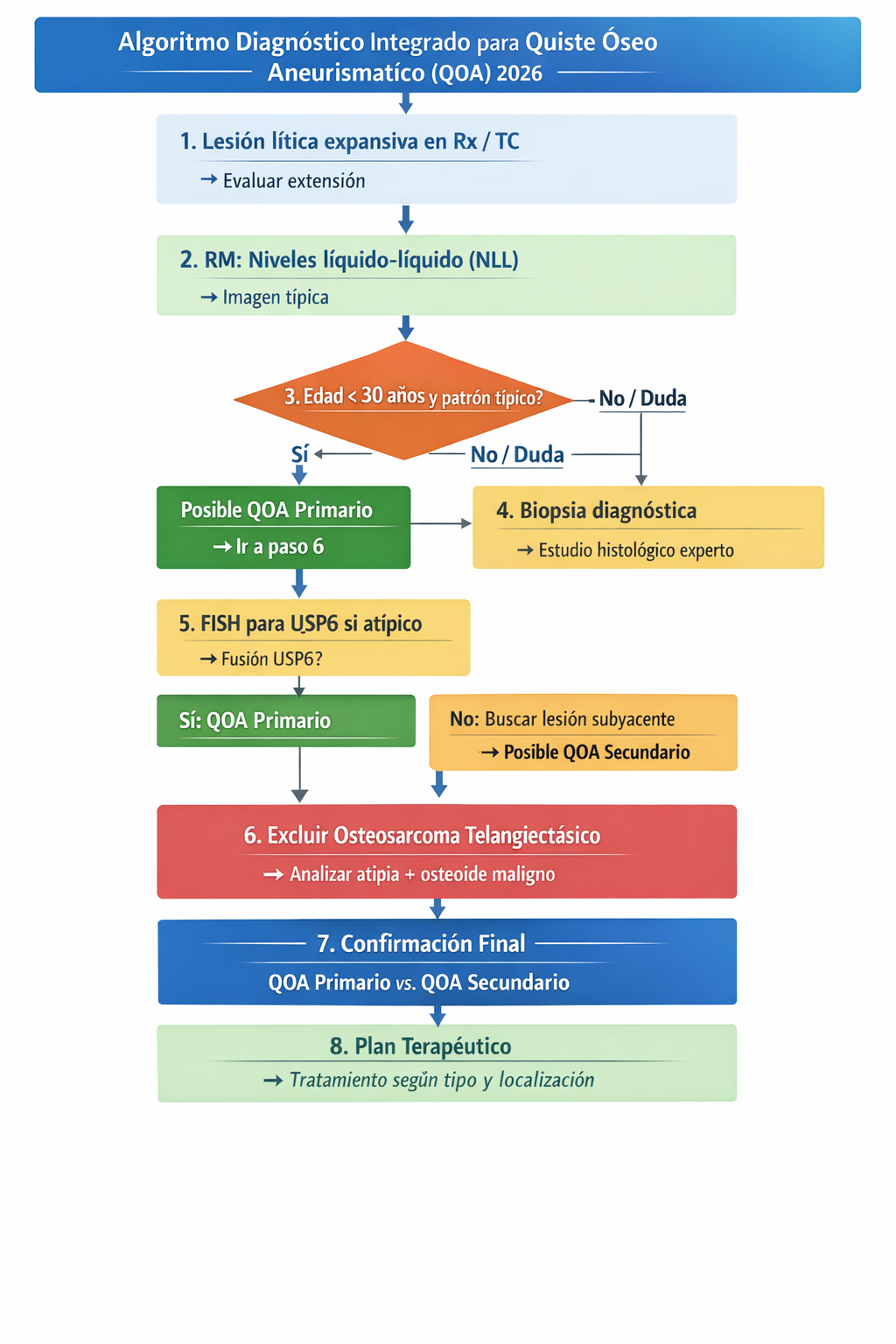
7) Tratamiento (estándar)
7.1 Principio general
Objetivo: control local definitivo con la menor morbilidad. Dada la recidiva (≈10–30%), se recomienda técnica intralesional agresiva desde la primera intervención cuando proceda.
7.2 Curetaje extendido + adyuvantes + relleno
- Curetaje intralesional agresivo hasta hueso sano.
- Fresado de alta velocidad.
- Adyuvantes locales según centro (argón, fenol, crioterapia, cemento con efecto térmico).
- Relleno con injerto/sustituto/cemento según defecto y carga.
7.3 Opciones selectivas
- ✅ Escleroterapia percutánea (p. ej., polidocanol; doxiciclina según protocolos).
- ✅ Embolización arterial selectiva (especialmente pelvis/columna).
- ✅ Denosumab (off-label) en casos agresivos/recurrentes seleccionados, con vigilancia de efectos.
- ✅ Radioterapia: generalmente evitada; solo situaciones excepcionales no resecables.
7.4 Resección en bloque
Indicaciones: recidivas múltiples, lesión muy agresiva, o localización “expendable”.
7.5 QOA secundario
El tratamiento debe dirigirse a la lesión primaria subyacente.
8) Seguimiento (práctico)
8.1 Esquema sugerido
| Periodo | Estudios | Frecuencia |
|---|---|---|
| 0–2 años | Rx (± RM si duda clínica/radiológica) | Cada 3–4 meses (según riesgo/localización) |
| 2–5 años | Rx | Anual |
| >5 años | Según síntomas / hallazgos | No rutinario |
La mayoría de recidivas aparecen en los primeros 24 meses.
9) Pronóstico
- ✅ Recidiva local: ~10–30% (mayor riesgo en pelvis/columna, pacientes muy jóvenes, lesiones grandes o técnica insuficiente).
- ✅ Metástasis: no característica del QOA. Si se sospecha, replantear diagnóstico (p. ej., OST).
- ✅ Transformación maligna: excepcional (clásicamente asociada a radioterapia previa u otra entidad).
- ✅ Resultado funcional: generalmente excelente si control local; vigilar deformidad/alteraciones de crecimiento si afecta fisis.
Mimicker crítico: el osteosarcoma telangiectásico. Ante lesión quística hemorrágica con agresividad, la prioridad es excluir OST con biopsia representativa y patología experta.
Resumen para la práctica clínica
📌 Indicaciones
- ✅ Lesión lítica expansiva “soplante” metafisaria en paciente joven.
- ✅ Niveles líquido–líquido en RM con realce de septos (en contexto compatible).
- ✅ Lesiones en pelvis/columna o con síntomas neurológicos (planificación compleja).
- ✅ Paciente >30 años o hallazgos atípicos → sospechar QOA secundario y buscar lesión primaria.
🔧 Técnica
- 🔧 Rx + RM con contraste para caracterización y extensión; TC si pelvis/columna.
- 🔧 Biopsia si agresividad marcada, masa de partes blandas, edad atípica o duda con OST.
- 🔧 Si QOA típico: curetaje extendido + fresa alta velocidad ± adyuvante local + relleno.
- 🔧 Si localización compleja o recidiva: considerar embolización/escleroterapia/estrategia individualizada.
- 🔧 Si QOA secundario: tratar la lesión primaria subyacente.
⚠️ Riesgos
- ⚠️ Recidiva local (principal riesgo), especialmente pelvis/columna o curetaje incompleto.
- ⚠️ Fractura perioperatoria o tardía según defecto y carga.
- ⚠️ Daño articular/subcondral si lesión yuxtaarticular.
- ⚠️ Error diagnóstico: confundir OST con QOA o no reconocer QOA secundario.
- ⚠️ Complicaciones de reconstrucción (injerto/cemento/osteosíntesis) según defecto.
✅ Resultados
- ✅ Control local alto con técnica intralesional extendida bien realizada.
- ✅ Función preservada en la mayoría de localizaciones de extremidad.
- ✅ Recidivas habitualmente tratables con reintervención o técnicas alternativas.
- ✅ No metastatiza (si hay metástasis, replantear diagnóstico).
- ✅ Seguimiento más estrecho los primeros 24 meses.
10) Bibliografía (selección útil)
Clasificación y genética
- 📄 WHO Classification of Tumours Editorial Board. Soft Tissue and Bone Tumours. 5th ed. IARC; 2020.
- 📄 Agaram NP, et al. USP6 gene rearrangements in aneurysmal bone cyst: FISH study. Mod Pathol. 2021.
- 📄 Ameline B, et al. USP6 rearrangement in osteoblastoma and aneurysmal bone cyst: FISH/NGS. Genes Chromosomes Cancer. 2022.
Manejo y tratamiento
- 📄 Deventer N, et al. Aneurysmal bone cyst: review and current treatment concepts. J Orthop Surg Res. 2023.
- 📄 Brosjö O, et al. Sclerotherapy with polidocanol for aneurysmal bone cysts: systematic review. Acta Orthop. 2022.
- 📄 Kurucu N, et al. Denosumab treatment in aneurysmal bone cyst: multicenter retrospective study. Pediatr Blood Cancer. 2024.
Diagnóstico diferencial
- 📄 Righi A, et al. Telangiectatic osteosarcoma versus aneurysmal bone cyst. Skeletal Radiol. 2021.
- 📄 Freitas PS, et al. Fluid-fluid levels in musculoskeletal tumors: systematic review. Radiol Bras. 2023.
