Última revisión:
Biopsia
La biopsia es el paso que transforma una sospecha por imagen en un diagnóstico útil para decidir tratamiento. En oncología musculoesquelética no es un "trámite": una biopsia mal planificada puede contaminar compartimentos, dificultar márgenes quirúrgicos y obligar a cirugías más agresivas. La regla práctica es sencilla: la biopsia se planifica como si fuera el primer gesto de la cirugía definitiva.
Si buscas una explicación más sencilla y orientada a pacientes y familias sobre pruebas, biopsia, tratamiento y seguimiento, consulta nuestras preguntas frecuentes para pacientes.
1) Objetivos reales de la biopsia
- Confirmar naturaleza tumoral y descartar procesos que simulan tumor (infección, fractura por estrés, necrosis, etc.).
- Clasificar la lesión (benigna / intermedia / maligna) y, cuando es posible, identificar el subtipo histológico.
- Definir grado en sarcomas cuando el material lo permite (impacta en radioterapia y tratamiento sistémico).
- Aportar material para técnicas actuales: inmunohistoquímica, FISH, PCR/NGS, y bancos de tejido si procede.
La biopsia no es solo "sacar un trozo": es el eslabón entre la imagen y el tratamiento.
2) Cuándo biopsiar / cuándo no
📌 Cuándo biopsiar
En términos prácticos, se biopsia cuando el resultado puede cambiar decisiones o cuando la imagen no permite un diagnóstico suficientemente fiable. En sarcoma sospechado, la biopsia suele ser obligatoria:
- ⚠️ Lesiones agresivas en Rx/TC/RM (destrucción cortical, masa de partes blandas, permeación medular, periostitis agresiva).
- ⚠️ Masa de partes blandas profunda o >5 cm, o cualquier masa que crece o provoca síntomas.
- ⚠️ Lesiones atípicas para benignidad o con discordancia clínica-radiológica.
- ⚠️ Antes de tratamientos que comprometen el diagnóstico (embolización, radiofrecuencia, curetaje "a ciegas").
⛔ Cuándo NO biopsiar (o hacerlo con cautela)
Hay escenarios en los que biopsiar sin una estrategia clara aumenta riesgos o da muestras no representativas. En lesiones con patrón benigno clásico y correlación clínica, puede evitarse:
- ✓ Lesiones benignas "de libro" con correlación clínica e imagen típica (según criterio del equipo).
- ! Lesiones muy vasculares sin preparación: riesgo de sangrado (valorar RM dinámica, angio-TC, embolización previa si procede).
- ! Zona necrótica o quística predominante: alto riesgo de "biopsia no diagnóstica" (hay que dirigir a componente sólido viable).
3) Principios de planificación
Regla de oro: el trayecto de la biopsia debe poder resecarse en bloque con el tumor en la cirugía definitiva.
✅ Imprescindible
- Plan conjunto con el cirujano que operaría el caso (o con el equipo de sarcomas).
- Entrada directa a la lesión evitando atravesar múltiples compartimentos, articulaciones, vainas tendinosas o paquetes neurovasculares.
⚠️ Crítico
- Evitar hematomas: un hematoma puede comportarse como "siembra" tumoral y expandir el campo contaminado.
- Marcar trayecto cuando sea incisional o compleja (según protocolo del centro).
Recomendación: Idealmente, la biopsia debe realizarse en el centro donde se llevará a cabo el tratamiento definitivo, o bajo protocolos consensuados con dicho centro.
4) Tipos de biopsia
Comparativa de técnicas basada en guías actuales y práctica clínica recomendada. La elección depende de la localización, el tamaño, la sospecha diagnóstica y la experiencia del centro.
| Técnica | Ventajas | Limitaciones / riesgos |
|---|---|---|
| Biopsia con aguja gruesa (core) | Alta rentabilidad diagnóstica (>90%), mínimamente invasiva, guiada por imagen, baja morbilidad. Permite estudios IHQ y moleculares. | Muestra limitada; si el tumor es heterogéneo puede infraestimar grado; requiere buena selección del sitio (evitar necrosis). |
| PAAF (punción aspiración con aguja fina) | Rápida, útil en recidiva/metástasis conocidas o ganglios; menor invasividad. Permite estudios citológicos y moleculares básicos. | En sarcomas primarios suele ser insuficiente para arquitectura y grado; depende mucho del citopatólogo. No se recomienda como primera opción en tumores primarios sospechosos. |
| Biopsia incisional | Más tejido, útil si core fue no diagnóstica o si se necesita arquitectura amplia. Permite estudios diagnósticos completos. | Más morbilidad, riesgo de contaminación si se hace mal; el abordaje debe ser "quirúrgico oncológico" (trayecto resecable). Requiere quirófano. |
| Biopsia excisional | Puede ser definitiva en lesiones pequeñas y superficiales claramente benignas (lipoma, ganglión). | Peligrosa si se usa en tumores sospechosos: puede dejar margen intralesional ("whoops surgery") y contaminar planos. |
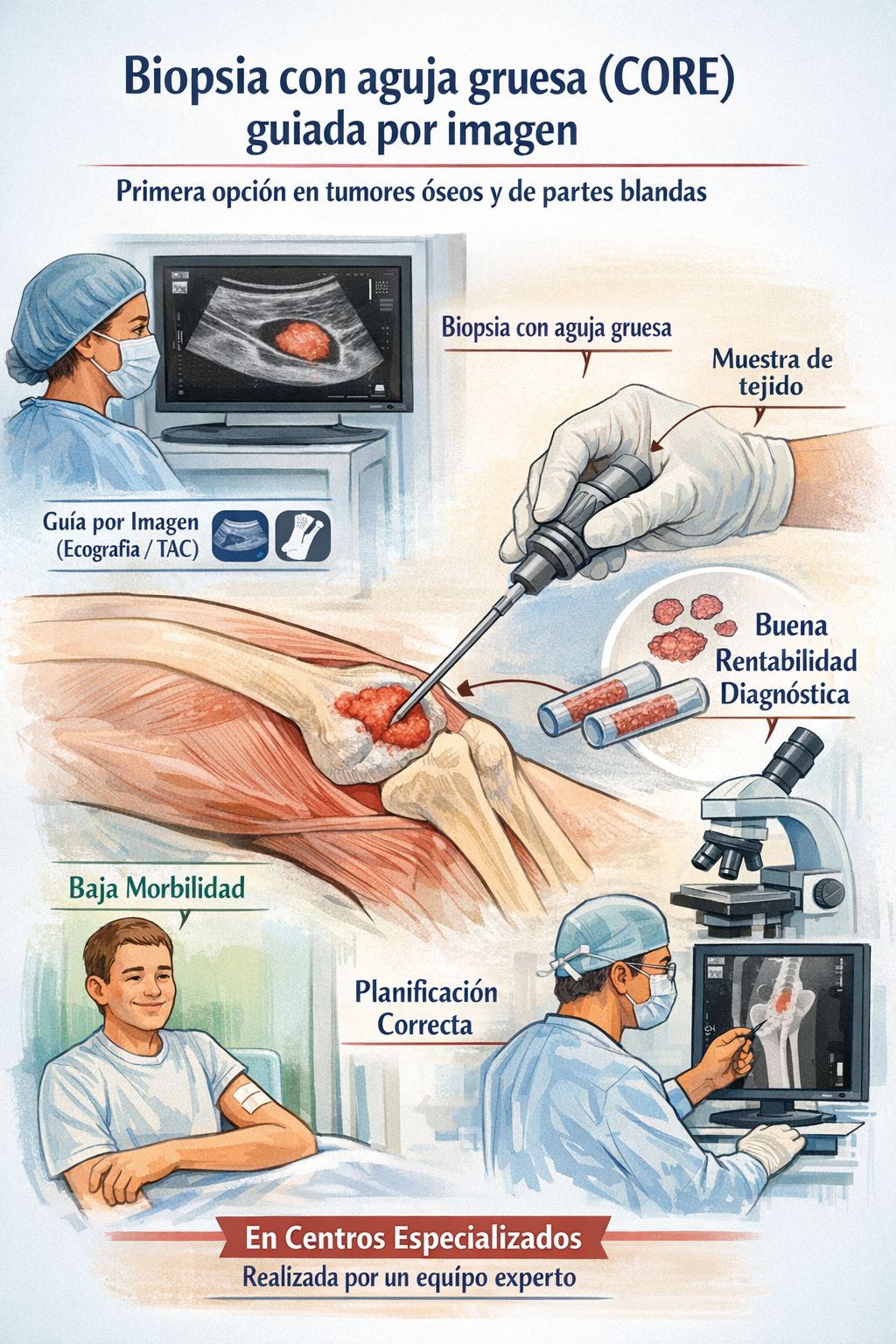
Recomendación actual: En centros especializados, la biopsia con aguja gruesa (core) guiada por imagen es la primera opción en la mayoría de tumores óseos y de partes blandas, porque combina buena rentabilidad diagnóstica con baja morbilidad, siempre que la planificación sea correcta.
5) Biopsia guiada por imagen
Ecografía
Ideal en masas superficiales; permite evitar vasos y dirigir a áreas sólidas; rápida, sin radiación y con alta precisión para lesiones de partes blandas.
Tomografía (TC)
Muy útil en hueso y en lesiones profundas; permite trayectorias seguras y control del material óseo. Es la técnica de elección para lesiones óseas y masas profundas con estructuras óseas adyacentes.
Resonancia (RM)
Guía menos frecuente por logística, pero excelente para elegir zonas viables cuando la lesión es compleja o con áreas necróticas/hemorrágicas. Ideal para planificar el trayecto en relación con estructuras nobles.
Truco práctico: En tumores grandes y heterogéneos, suele ser mejor obtener varios cilindros en zonas distintas del componente sólido, evitando necrosis/hemorragia. La colaboración con radiología intervencionista es clave.
6) Qué debe incluir el informe
El informe ideal integra clínica + imagen + anatomía patológica. En sarcomas, además del subtipo, interesa el grado cuando es posible, la presencia de necrosis, y la propuesta de panel inmunohistoquímico. En la práctica moderna, algunos diagnósticos requieren estudios moleculares (translocaciones, amplificaciones, mutaciones).
📌 Lista útil para el día a día (clic para desplegar)
- ✅ Diagnóstico más probable y diferenciales relevantes.
- ✅ Grado (si es evaluable) y comentario de limitaciones por tamaño de muestra.
- ✅ Panel inmunohistoquímico recomendado/realizado.
- ✅ Si procede: recomendación de estudio molecular (FISH, NGS) o remisión a centro de referencia.
- ✅ Concordancia o discordancia con imagen (muy importante).
Comunicación esencial: La correlación radio-patológica debe ser bidireccional. El radiólogo debe saber qué se ha biopsiado, y el patólogo debe conocer los hallazgos de imagen para contextualizar la muestra.
7) Errores frecuentes y cómo evitarlos
Lo más peligroso: resecar "por sorpresa" un sarcoma (cirugía intralesional) o hacer una biopsia con trayecto imposible de resecar en la cirugía definitiva.
❌ Errores frecuentes
- Tomar muestra de zonas necróticas o hemorrágicas.
- Contaminar compartimentos (atravesar articulaciones, vainas tendinosas, paquetes neurovasculares).
- Tratar antes de diagnosticar (curetaje, ablación sin confirmación histológica).
- No correlacionar con imagen: biopsiar sin conocer la extensión real de la lesión.
✅ Soluciones
- Dirigir a borde viable con guía de imagen (evitar necrosis).
- Trayecto corto, directo y planificado con el cirujano (resecable en bloque).
- Siempre biopsiar antes de cualquier tratamiento definitivo.
- Comunicación activa con radiología y patología (correlación clínico-radiológica).
Dato: Hasta un 20% de las biopsias mal planificadas pueden comprometer la cirugía conservadora y obligar a amputaciones o resecciones más amplias de lo necesario.
Resumen para la práctica clínica
Indicaciones
- ✓ Toda lesión ósea o masa de partes blandas con criterios de agresividad o crecimiento progresivo.
- ✓ Masas profundas o mayores de 5 cm, o lesiones con discordancia clínica-radiológica.
- ✓ Antes de cualquier tratamiento que pueda distorsionar la anatomía patológica (curetaje, ablación, embolización).
Técnica
- 🔧 Planificar la biopsia con el equipo que realizará el tratamiento definitivo; elegir un trayecto resecable en bloque.
- 🔧 Preferir biopsia con aguja gruesa guiada por imagen; obtener varios cilindros de áreas sólidas viables.
- 🔧 Enviar material para histología e inmunohistoquímica; considerar biología molecular cuando sea relevante.
Riesgos
- ⚠️ Contaminación del trayecto y compartimentos si la biopsia está mal planificada.
- ⚠️ Muestra no diagnóstica si se pincha necrosis/hemorragia; posible necesidad de repetir biopsia.
- ⚠️ Sangrado/hematoma, especialmente en tumores muy vascularizados.
Resultados
- ✅ Diagnóstico histológico y, cuando procede, grado y panel inmuno/molecular orientado a confirmar subtipo.
- ✅ Definición de estrategia terapéutica (cirugía, radioterapia, tratamiento sistémico) basada en subtipo y estadificación.
- ✅ Mejor planificación quirúrgica al conocer extensión y al asegurar un trayecto de biopsia resecable.
Bibliografía y lecturas recomendadas
Soft Tissue and Bone Tumours. 5th ed. IARC; 2020.
Soft Tissue Sarcoma / Bone Cancer. Version 2.2026.
Soft tissue and visceral sarcomas; Bone sarcomas. Ann Oncol. 2021.
The hazards of biopsy in patients with malignant primary bone and soft-tissue tumors. J Bone Joint Surg Am. 1982;64(8):1121-1127.
The hazards of the biopsy, revisited. J Bone Joint Surg Am. 1996;78(5):656-663.
Revisiones actuales sobre estrategia de biopsia en sarcomas y consensos sobre "whoops surgery".
