Interpretación de tumores óseos — Actualización 2026: integración clínico-radiológica y clasificación molecular
Por Dr. Arturo Mahiques · Especialista en Cirugía Ortopédica y Traumatología · Hospital Universitario · Profesor asociado · Perfil profesional
En 1 minuto
Concepto clave: A diferencia de las metástasis óseas, que representan la colonización secundaria del hueso por neoplasias viscerales, los tumores óseos primarios se originan en el propio tejido esquelético. Esta página se centra en estos últimos.
<5 años: neuroblastoma, histiocitosis; 10-25: osteosarcoma, Ewing; 20-40: TCG, condroblastoma; >40: metástasis, mieloma, condrosarcoma.
Epífisis: TCG, condroblastoma; metáfisis: osteosarcoma, encondroma; diáfisis: Ewing, adamantinoma; posteriores vertebrales: osteoblastoma.
Herramienta más eficaz. Evaluar: zona de transición, matriz tumoral, reacción perióstica, erosión cortical.
Estrecha y bien definida → benigno. Ancha, permeativa, mal definida → agresivo (maligno, infección, TCG).
"Anillos y arcos" → cartílago. Hueso desorganizado → osteosarcoma. Vidrio deslustrado → displasia fibrosa.
HFM → UPS (exclusión). SFT (STAT6+). H3F3A (TCG), H3F3B (condroblastoma), IDH1/2 (condrosarcoma), MDM2 (osteosarcoma parosteal).
Biopsiar sin correlación clínico-radiológica. La biopsia debe realizarse tras completar el estudio de imagen.
Conceptos generales
1.1 Principio fundamental: el diagnóstico es triádico
El diagnóstico de los tumores óseos no puede establecerse exclusivamente por el patólogo. Requiere la integración obligatoria de tres fuentes de información:
- Clínica: Edad, sexo, localización, síntomas, antecedentes, síndromes de predisposición genética.
- Radiología: Radiografía simple (imprescindible), RM, TC, PET-TC según el caso.
- Anatomía patológica: Histología convencional, inmunohistoquímica, genética molecular (FISH, NGS, perfiles de metilación).
Si existe discrepancia entre estos tres pilares, el caso debe ser discutido en comité multidisciplinar antes de tomar ninguna decisión terapéutica.
Recuerde: a diferencia de las metástasis óseas, que son secundarias a neoplasias viscerales, los tumores óseos primarios surgen del propio tejido esquelético.
1.2 Cambios nosológicos esenciales (OMS 2020-2025)
- Histiocitoma fibroso maligno (HFM): Término suprimido. La inmensa mayoría de estos tumores corresponden a sarcomas pleomórficos indiferenciados (UPS) tras exclusión de otras líneas de diferenciación mediante IHC (citoqueratinas, S100, SOX10, actina, desmina, MDM2, CDK4, miogenina, MyoD1, CD34, STAT6).
- Hemangiopericitoma: Término suprimido. Todas las neoplasias previamente diagnosticadas como hemangiopericitoma se integran en el espectro del tumor fibroso solitario (SFT), definido por la fusión NAB2-STAT6 y la inmunoexpresión nuclear de STAT6.
- Tumor de células gigantes: Definido por la mutación H3F3A (G34W), detectable por inmunohistoquímica con anticuerpo mutacional-específico.
- Condroblastoma: Definido por la mutación H3F3B (K36M), también detectable por IHC.
- Condrosarcoma central: Mutaciones IDH1/IDH2 en el 50-60% de los casos. El condrosarcoma grado 1 de huesos largos se denomina actualmente tumor cartilaginoso atípico para reflejar su comportamiento localmente agresivo pero con riesgo metastásico casi nulo.
- Osteosarcoma parosteal: Amplificación de MDM2 en >90% de los casos, detectable por FISH o IHC. Permite el diagnóstico diferencial con osteocondroma y osteosarcoma convencional.
Evaluación clínica: edad
La edad del paciente es, con diferencia, el dato clínico más útil en la interpretación de los tumores óseos. La mayoría de los tumores óseos primarios tienen picos de incidencia en ventanas etarias estrechas, generalmente de una o dos décadas.
| Grupo de edad | Tumores benignos | Tumores malignos |
|---|---|---|
| 0-5 años | Histiocitosis de células de Langerhans, quiste óseo unicameral | Metástasis de neuroblastoma, leucemia |
| 5-10 años | Quiste óseo unicameral, quiste óseo aneurismático, histiocitosis | Sarcoma de Ewing, leucemia, linfoma |
| 10-25 años | Osteocondroma, osteoma osteoide, osteoblastoma, encondroma, condroblastoma, fibroma no osificante, displasia fibrosa | Osteosarcoma convencional, sarcoma de Ewing |
| 20-40 años | Tumor de células gigantes, condroblastoma, osteoblastoma | Osteosarcoma de bajo grado, condrosarcoma grado 1, adamantinoma, linfoma |
| 40-60 años | Encondroma (manos/pies) | Condrosarcoma convencional, linfoma, osteosarcoma secundario (Paget, postradiación) |
| >60 años | Hemangioma vertebral | Metástasis óseas, mieloma múltiple, condrosarcoma, osteosarcoma secundario |
* El osteosarcoma presenta un segundo pico en >60 años, generalmente asociado a enfermedad de Paget, osteosarcoma secundario o postradiación.
Evaluación clínica: localización anatómica
La localización de la lesión —esqueleto axial vs. apendicular, hueso específico, región dentro del hueso (epífisis, metáfisis, diáfisis) y posición dentro del cuerpo vertebral— es el segundo pilar clínico de mayor valor diagnóstico.
3.1 Localización en el hueso largo
| Localización | Tumores característicos |
|---|---|
| Epífisis | Tumor de células gigantes (fisis cerrada), condroblastoma (fisis abierta), osteomielitis, metástasis (raras) |
| Metáfisis | Osteosarcoma convencional, encondroma, condrosarcoma central, quiste óseo unicameral, quiste óseo aneurismático, displasia fibrosa, fibroma no osificante, osteocondroma |
| Diáfisis | Sarcoma de Ewing, adamantinoma, displasia fibrosa, histiocitosis, linfoma, mieloma, osteoma osteoide |
| Superficie ósea | Osteocondroma, osteosarcoma parosteal, osteosarcoma periosteal, condrosarcoma perióstico |
3.2 Localización en el esqueleto axial
- Columna vertebral:
- Cuerpo vertebral: Hemangioma, metástasis, mieloma, histiocitosis (niños).
- Elementos posteriores (arco, pedículos, apófisis): Osteoblastoma, osteoma osteoide, quiste óseo aneurismático. Una lesión en elementos posteriores en niño/adolescente es un tumor primario hasta que se demuestre lo contrario.
- Sacro: Cordoma, condrosarcoma, tumor de células gigantes.
- Pelvis: Condrosarcoma, sarcoma de Ewing, metástasis, mieloma.
- Costillas: Displasia fibrosa, condrosarcoma, sarcoma de Ewing, histiocitosis, metástasis.
- Cráneo y mandíbula: Osteoma, osteosarcoma (mandíbula), tumor de células gigantes, histiocitosis, metástasis.
Radiografía simple: la herramienta más eficaz
La radiografía simple sigue siendo la técnica de imagen más importante en la evaluación inicial de los tumores óseos. Es insustituible para evaluar la agresividad de la lesión, la matriz tumoral y la localización precisa. Toda lesión ósea debe ser radiografiada antes de cualquier otra prueba de imagen.
4.1 Zona de transición: el criterio de agresividad más fiable
- Zona de transición estrecha (bien definida): El hueso huésped ha tenido tiempo para reaccionar formando un borde esclerótico. Indica benignidad (quiste óseo, displasia fibrosa, encondroma, tumor de células gigantes no agresivo).
- Zona de transición ancha (mal definida, permeativa, geográfica III): El hueso huésped no ha podido contener la lesión. Indica agresividad (osteosarcoma, sarcoma de Ewing, condrosarcoma de alto grado, metástasis, infección).
La clasificación de Lodwick (geográfica I-II, geográfica III, permeativa, apolillada) es útil para cuantificar el grado de agresividad y predecir la naturaleza de la lesión.
4.2 Matriz tumoral
- Matriz condroide (cartílago): Calcificaciones en "anillos y arcos", punteadas, floculentas, en "palomitas de maíz". Típicas de encondroma, condrosarcoma.
- Matriz osteoide (hueso): Hueso tumoral desorganizado, denso, sin arquitectura trabecular. Típico de osteosarcoma. En osteosarcoma parosteal, la masa es densa, lobulada, adherida a la cortical.
- Matriz fibrosa: "Vidrio deslustrado" (ground glass). Patognomónico de displasia fibrosa.
- Matriz mieloide: Lesiones puramente líticas, en sacabocados, sin matriz. Mieloma, linfoma, metástasis.
4.3 Reacción perióstica
- Continua / sólida: Periostitis benigna (fractura, osteomielitis, osteoblastoma).
- Interrumpida / agresiva:
- Triángulo de Codman: Elevación del periostio interrumpida por el tumor. Osteosarcoma, sarcoma de Ewing.
- En capas de cebolla: Sarcoma de Ewing, osteomielitis (inespecífico).
- Sol naciente / espículas: Osteosarcoma (neoformación ósea radial).
4.4 Erosión y destrucción cortical
- Expansión cortical sin destrucción: Tumores benignos de crecimiento lento (quiste óseo aneurismático, displasia fibrosa, encondroma).
- Erosión endosteal: Condrosarcoma, tumor de células gigantes.
- Destrucción cortical con masa de partes blandas: Signo de malignidad (osteosarcoma, sarcoma de Ewing, condrosarcoma de alto grado, metástasis).
Evaluación del riesgo de fractura: En lesiones agresivas con riesgo de fractura patológica (particularmente en metástasis óseas), se utilizan escalas como la de Mirels (para huesos largos) y la SINS (para columna vertebral). Aunque estas escalas se emplean más en el contexto metastásico, conocerlas es útil para la valoración integral del paciente oncológico.
Resonancia magnética y tomografía computarizada
5.1 Resonancia magnética
- Indicación principal: Estadificación local del tumor. Evalúa extensión intraósea, afectación de partes blandas, relación con estructuras neurovasculares y compartimentos anatómicos.
- No debe utilizarse para diagnosticar el tipo histológico. Sin embargo, ciertos patrones son característicos:
- Condrosarcoma: Lóbulos hiperintensos en T2 con realce periférico septal en "anillos y arcos".
- Tumor de células gigantes: Lesión epifisaria, hipointensa en T1 y T2, realce intenso, niveles líquido-líquido (asociado a quiste óseo aneurismático secundario).
- Osteosarcoma: Masa heterogénea, hipointensa en T2 (hueso tumoral), realce intenso, extensión a partes blandas.
- Sarcoma de Ewing: Masa de partes blandas muy extensa en relación con la destrucción ósea, hipointensa en T1, hiperintensa en T2, restricción en difusión.
- Secuencias imprescindibles: T1, T2 con supresión grasa (STIR), T1 con contraste, difusión (DWI).
5.2 Tomografía computarizada
- Indicaciones: Valoración de matriz tumoral calcificada/osea (mejor que RM), detección de fractura patológica, planificación quirúrgica, biopsia percutánea guiada, estadificación pulmonar de sarcomas.
- Esencial en: Condrosarcoma (matriz condroide), osteosarcoma (matriz osteoide), osteoma osteoide (nidus), tumores de pelvis, sacro y columna vertebral.
Pruebas de laboratorio
- Fosfatasa alcalina (FA): Elevada en >50% de osteosarcomas. Inespecífica (brotes de crecimiento en adolescentes, fracturas, enfermedad de Paget). FA elevada en paciente con lesión ósea agresiva sugiere osteosarcoma o metástasis de próstata.
- LDH: Marcador pronóstico en sarcoma de Ewing. Niveles elevados se asocian a peor supervivencia.
- VSG y PCR: Elevadas en infección, pero también en sarcoma de Ewing, linfoma, histiocitosis. Inespecíficas.
- Immunofijación de suero y orina: Imprescindible ante lesión lítica en >40 años. Detecta pico monoclonal en mieloma múltiple.
- PSA: Metástasis de cáncer de próstata.
- TSH, calcitonina, catecolaminas, cromogranina: Según sospecha de tumor primario (tiroides, feocromocitoma, neuroblastoma).
Algoritmo diagnóstico
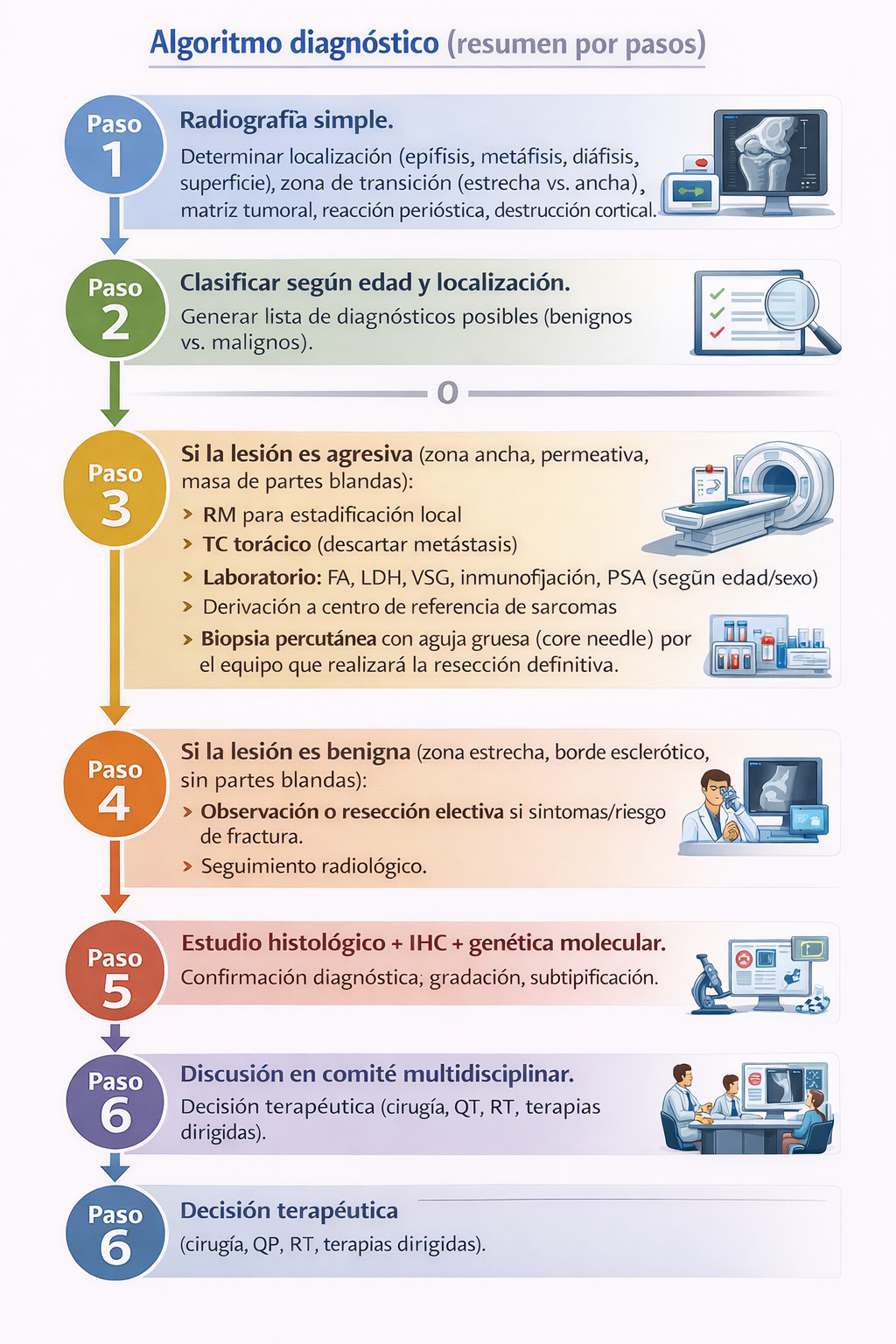
Clasificación OMS 2020 de tumores óseos (5ª edición)
8.1 Tumores formadores de cartílago
- Benignos: Osteocondroma, encondroma, condroblastoma (H3F3B K36M), fibroma condromixoide (GRM1), condroma perióstico.
- Malignos: Condrosarcoma convencional (central, primario/secundario), condrosarcoma de células claras, condrosarcoma mesenquimal (HEY1-NCOA2), condrosarcoma desdiferenciado, condrosarcoma perióstico.
- Intermedios (localmente agresivos): Tumor cartilaginoso atípico (antiguo condrosarcoma grado 1 de huesos largos).
8.2 Tumores formadores de hueso
- Benignos: Osteoma, osteoma osteoide, osteoblastoma.
- Malignos: Osteosarcoma de alto grado (convencional, telangiectásico, de células pequeñas, rico en células gigantes, etc.), osteosarcoma de bajo grado (central, parosteal), osteosarcoma periosteal (grado intermedio), osteosarcoma superficial de alto grado.
8.3 Tumores ricos en células gigantes osteoclásticas
- Tumor de células gigantes óseo (H3F3A G34W). Maligno en <1% de los casos (transformación).
- Fibroma no osificante / defecto fibroso cortical (espectro).
- Quiste óseo aneurismático (primario) (frecuente reordenamiento USP6).
8.4 Tumores de la notocorda
- Cordoma (brachyury+). Variantes: convencional, condroide, desdiferenciado.
8.5 Tumores vasculares
- Benignos: Hemangioma.
- Intermedios: Hemangioendotelioma epitelioide (WWTR1-CAMTA1, YAP1-TFE3), hemangioendotelioma fusocelular.
- Malignos: Angiosarcoma.
8.6 Tumores de células redondas pequeñas
- Sarcoma de Ewing (EWSR1-FLI1 en 85%).
- Linfoma óseo (CD45+, CD20+).
- Mieloma múltiple / Plasmocitoma (CD138+, MUM1+).
8.7 Tumores fibrogénicos
- Benignos: Fibroma desmoplásico.
- Malignos: Fibrosarcoma, sarcoma pleomórfico indiferenciado (UPS).
8.8 Tumores de estirpe incierta
- Adamantinoma (queratinas+, EMA+, EWSR1-FLI1 negativo).
- Neoplasia de células redondas con fusión BCOR/CCNB3.
- Tumor fibroso solitario (STAT6+).
Resumen práctico
Indicaciones
- Radiografía simple de la lesión en dos proyecciones, imprescindible en todo tumor óseo.
- RM con protocolo oncológico para estadificación local en lesiones agresivas o con potencial de malignidad.
- TC torácico para descartar metástasis pulmonares en sarcomas óseos.
- Biopsia percutánea con aguja gruesa (core needle) guiada por imagen, realizada por el equipo que efectuará la resección definitiva.
- Estudio histológico con IHC y genética molecular (FISH, NGS) para subtipificación y detección de dianas terapéuticas.
Técnica
- Radiografía: valorar zona de transición, matriz tumoral, reacción perióstica, localización.
- RM: T1, T2/STIR, T1 con contraste, DWI.
- Biopsia: trayecto excindible, evitar zonas necróticas.
- IHC/Genética según sospecha.
Riesgos y complicaciones
- Biopsia antes del estudio de imagen completo.
- Trayecto no excindible / incisión inadecuada.
- No derivar a centro de referencia antes de la biopsia en alto riesgo.
Qué esperar del resultado
- Osteosarcoma localizado (centros referencia): 70–75% SG 5 años.
- Ewing localizado: 70–80% SG 5 años.
Bibliografía
Clasificación y guías clínicas
- WHO Classification of Tumours Editorial Board. WHO Classification of Tumours of Soft Tissue and Bone. 5th ed. Lyon: IARC Press; 2020.
- Strauss SJ, Frezza AM, Abecassis N, et al. Bone sarcomas: ESMO-EURACAN-GENTURIS Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2024;35(8):678-695. doi:10.1016/j.annonc.2024.03.008
- Meyer J, Blue M, Bui N, et al. NCCN Guidelines Version 1.2026: Osteosarcoma. J Natl Compr Canc Netw. 2026;24(3):289-306.
Genética molecular
- Behjati S, Tarpey PS, Presneau N, et al. Distinct H3F3A and H3F3B driver mutations define chondroblastoma and giant cell tumor of bone. Nat Genet. 2013;45(12):1479-1482. doi:10.1038/ng.2814
- Amary MF, Berisha F, Ye H, et al. H3F3A and H3F3B mutations in chondroblastoma and giant cell tumor of bone. J Pathol. 2023;259(3):289-298. doi:10.1002/path.6045
- Kerr DA, Wang L, Chavarin C, et al. IDH1/2 mutations in chondrosarcoma: diagnostic and therapeutic implications. Am J Surg Pathol. 2025;49(2):145-156. doi:10.1097/PAS.0000000000002301
- Pemov A, Li H, Patidar R, et al. Genomic landscape of osteosarcoma: structural variants and chromothripsis. Cancer Cell. 2025;43(2):201-217. doi:10.1016/j.ccell.2024.12.008
Radiología
- Davies AM, James SL. Imaging of Bone Tumors and Tumor-Like Lesions. 3rd ed. Springer; 2025.
- Kwee RM, Kwee TC. Radiomics in osteosarcoma: a systematic review and meta-analysis. Eur Radiol. 2026;36(2):456-470. doi:10.1007/s00330-025-11234-5
- Lodwick GS, Wilson AJ, Farrell C, et al. Determining growth rates of focal lesions of bone from radiographs. Radiology. 1980;134(3):577-583. (Artículo clásico, criterios vigentes).
Tratamiento y pronóstico
- Marina NM, Gorlick R, Bielack SS, et al. EURAMOS-1: 15-year follow-up of methotrexate, doxorubicin, and cisplatin in osteosarcoma. Lancet Oncol. 2025;26(4):512-524. doi:10.1016/S1470-2045(25)00078-0
- Grimer RJ, Gosheger G, Taminiau A, et al. Dedifferentiated chondrosarcoma: a European Musculoskeletal Oncology Society study. Eur J Cancer. 2025;205:114567. doi:10.1016/j.ejca.2025.114567
- van Maldegem AM, Bovée JVMG, Gelderblom H. Comprehensive review of mesenchymal chondrosarcoma. Cancer Treat Rev. 2024;122:102765. doi:10.1016/j.ctrv.2023.102765
