Metástasis óseas — Actualización 2026: abordaje práctico y actualizado
Por Dr. Arturo Mahiques · Especialista en Cirugía Ortopédica y Traumatología · Hospital Universitario · Profesor asociado · Perfil profesional
En 1 minuto
Concepto clave: A diferencia de los tumores óseos primarios, las metástasis óseas son implantes tumorales secundarios procedentes de carcinomas (mama, próstata, pulmón, etc.) y constituyen la neoplasia maligna más frecuente del esqueleto.
Primarios más frecuentes: próstata (36%), mama (32%), pulmón (14%), riñón (8%), tiroides (5%). Afectan sobre todo al esqueleto axial (columna, pelvis, costillas, cráneo).
Dolor óseo persistente (nocturno, que no cede con reposo), fractura patológica, compresión medular, hipercalcemia. Hasta un 20% pueden debutar como primera manifestación de un cáncer oculto.
Radiografía: lítica (riñón, pulmón, tiroides), blástica (próstata) o mixta (mama). Gammagrafía ósea: alta sensibilidad. PET/TC (FDG, PSMA) según tumor. RM en columna para descartar compresión.
Hormonoterapia (mama, próstata), quimioterapia, terapias dirigidas, inmunoterapia. Antirresortivos: bifosfonatos (zoledronato) o denosumab reducen eventos esqueléticos.
Paliativa (dosis única 8 Gy) o estereotáxica (SBRT) para control local. Radiofármacos: Ra-223 (próstata resistente a castración), Lu-177-PSMA en progresión.
Fijación profiláctica (Mirels ≥9), fractura patológica, inestabilidad espinal o compresión medular. Reconstrucciones duraderas (clavos, prótesis) ante expectativas de supervivencia prolongada.
Conceptos generales
1.1 Relevancia clínica
Las metástasis óseas superan en frecuencia a cualquier tumor óseo primario. Su impacto en la calidad de vida es enorme: dolor, fracturas, compresión neurológica e hipercalcemia. El ortopeda desempeña un papel clave no solo en el tratamiento de las fracturas, sino en la prevención y en el diagnóstico del primario desconocido.
Con los avances en terapias sistémicas (hormonoterapia, inmunoterapia, terapias dirigidas) la supervivencia de ciertos pacientes se ha alargado, lo que exige reconstrucciones quirúrgicas duraderas.
1.2 Vías de diseminación
- Hematógena: Principal vía; los émbolos tumorales alcanzan la médula ósea por circulación arterial.
- Plexo venoso de Batson: Sistema venoso paravertebral sin válvulas que comunica tórax, abdomen y pelvis con el esqueleto axial. Explica la alta frecuencia de metástasis vertebrales en próstata, mama y pulmón.
- Extensión directa: Por contigüidad desde un tumor de partes blandas (raro).
Fisiopatología de la enfermedad ósea metastásica
2.1 El círculo vicioso
Las células tumorales secretan factores que estimulan los osteoclastos (PTHrp, IL-6, RANKL), activando la resorción ósea. Esto libera factores de crecimiento (TGF-β, IGF) almacenados en la matriz, que a su vez estimulan la proliferación tumoral. Se establece así un círculo vicioso que perpetúa la destrucción ósea.
2.2 Tipos según respuesta ósea
- Osteolíticas: riñón, pulmón, tiroides, gastrointestinal. Mayor riesgo de fractura.
- Osteoblásticas: próstata; también mama, linfoma, seminoma, vejiga. Aunque el hueso parece denso, puede ser mecánicamente frágil.
- Mixtas: mama frecuentemente.
Nicho premetastásico y exosomas: El tumor primario libera factores y vesículas (exosomas) que modifican el microambiente óseo antes de la llegada de las células tumorales, creando un terreno fértil para la metástasis.
Clínica: ¿qué debemos sospechar?
3.1 Síntomas cardinales
- Dolor óseo: continuo, progresivo, de predominio nocturno y que no cede con el reposo. Es el síntoma más frecuente.
- Dolor mecánico: empeora con la carga (fémur, húmero), sugiere riesgo de fractura.
- Fractura patológica: complicación tardía que empeora el pronóstico funcional.
- Síntomas neurológicos: dolor radicular, debilidad, parestesias, incontinencia (compresión medular).
- Hipercalcemia: poliuria, polidipsia, estreñimiento, náuseas, confusión.
3.2 Síntomas según localización
- Columna: dolor dorsal o lumbar, rigidez, contractura. Si hay compresión, déficit motor/sensitivo o esfinteriano.
- Pelvis y fémur: dolor en ingle, muslo, cojera; dificultad para apoyar.
- Húmero: dolor al mover el brazo, pérdida de fuerza.
- Costillas: dolor con la respiración profunda.
Urgencias oncológicas: Ante cualquier déficit neurológico o incontinencia asociado a dolor de espalda, solicitar RM de columna urgente. Dolor mecánico intenso en fémur o húmero con imposibilidad de carga requiere valoración ortopédica inmediata.
Diagnóstico por imagen
4.1 Radiografía simple
- Primera prueba, accesible. Detecta lesiones cuando hay >30-50% de pérdida ósea.
- Patrones: lítico (riñón, pulmón, tiroides), blástico (próstata), mixto (mama).
- Útil para valorar riesgo de fractura (destrucción cortical, tamaño).
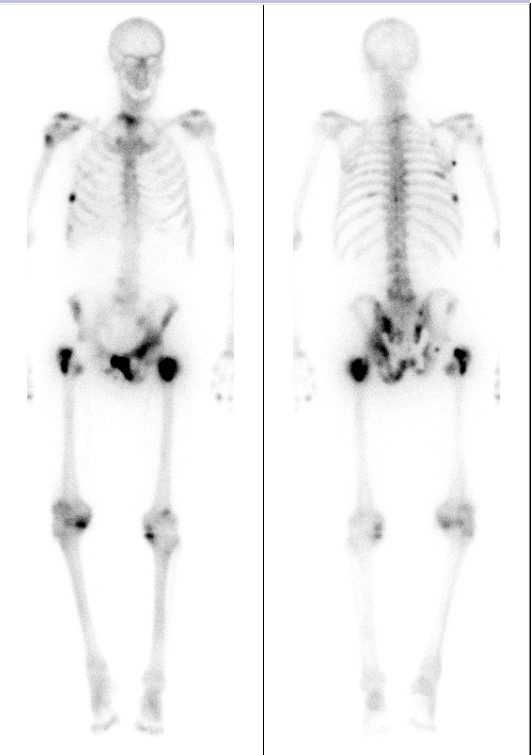
4.2 Gammagrafía ósea (99mTc-MDP)
- Alta sensibilidad para detectar lesiones metastásicas (osteoblásticas y mixtas).
- Especificidad limitada: se correlaciona con otras técnicas (SPECT/TC mejora la especificidad).
- El “superscan” (captación difusa intensa) indica afectación extensa (próstata, mama).
4.3 Tomografía computarizada (TC)
- Evalúa con precisión la destrucción cortical, extensión a partes blandas y planificación quirúrgica.
- TC toracoabdominopélvico es esencial para buscar el primario y estadificar.
4.4 Resonancia magnética (RM)
- Técnica de elección en columna vertebral (compresión medular, infiltración del canal).
- Útil en pelvis y lesiones con extensión a partes blandas.
- La RM de cuerpo entero (WB-MRI) con difusión es una alternativa sin radiación en centros especializados.
4.5 PET/TC
- FDG-PET/TC: útil en muchos tumores (pulmón, mama, linfoma). Detecta enfermedad extracraneal.
- PSMA PET/CT: en cáncer de próstata, ofrece alta sensibilidad y especificidad para metástasis óseas y ganglionares. Cuando está disponible, es la técnica de elección en próstata.
4.6 Biopsia
- Indicada si el primario es desconocido, la lesión es única o hay discordancia clínico-radiológica.
- Guiada por TC, con aguja gruesa (14-16G). En lesiones hipervasculares (riñón, tiroides), valorar embolización previa.
- Planificar el trayecto para que sea excindible en caso de cirugía posterior.
Marcadores bioquímicos
- Calcio sérico: ante sospecha de hipercalcemia tumoral (suele ser corregido con albúmina).
- Fosfatasa alcalina (FA): puede estar elevada en metástasis osteoblásticas (próstata) y en algunas líticas con reacción perióstica.
- PSA: imprescindible en varones para descartar cáncer de próstata.
- Proteinograma + inmunofijación: obligatorio ante lesiones líticas en >40 años para descartar mieloma múltiple.
- Otros marcadores: CEA (colon, mama), CA 15.3 (mama), CA 19.9 (páncreas, vía biliar), tiroglobulina (tiroides), etc., según contexto.
Cáncer de mama
Es el que con mayor frecuencia metastatiza a hueso (50-85% de las pacientes con enfermedad avanzada). Patrón predominantemente lítico o mixto. El tratamiento sistémico incluye hormonoterapia (según receptores), quimioterapia, anti-HER2, inhibidores de CDK4/6, y siempre antirresortivos (zoledronato/denosumab) para reducir eventos esqueléticos. La radioterapia paliativa es muy eficaz para el dolor. La cirugía profiláctica o reconstructiva debe considerar la larga supervivencia de algunos subgrupos.
Cáncer de próstata
El 50-70% de los pacientes desarrollan metástasis óseas, casi siempre osteoblásticas. La imagen de elección hoy es la PSMA PET/CT (si disponible), que supera a la gammagrafía convencional. El tratamiento incluye hormonoterapia, quimioterapia (docetaxel, cabazitaxel), nuevos agentes hormonales (abiraterona, enzalutamida), y radiofármacos como Ra-223 (para pacientes con metástasis óseas sintomáticas sin vísceras) y Lu-177-PSMA en progresión post-quimioterapia. Los antirresortivos también están indicados.
Cáncer de pulmón
Alrededor del 30-50% de los pacientes presentan metástasis óseas, generalmente líticas. El subtipo histológico (adenocarcinoma, escamoso, microcítico) y las alteraciones moleculares (EGFR, ALK, ROS1, PD-L1) guían el tratamiento sistémico (inhibidores de tirosina quinasa, inmunoterapia). La radioterapia es clave para el dolor y la compresión. La cirugía está indicada en fracturas o inestabilidad, pero la supervivencia suele ser limitada.
Cáncer renal (células claras)
Las metástasis óseas son líticas, frecuentemente hipervasculares, y pueden presentarse años después del diagnóstico. La embolización preoperatoria reduce el sangrado en cirugías de lesiones grandes. El tratamiento sistémico actual incluye inhibidores de tirosina quinasa (sunitinib, pazopanib) e inmunoterapia (nivolumab, ipilimumab). La radioterapia convencional tiene menor tasa de respuesta que en otros tumores; la SBRT puede ser más efectiva. La cirugía de la metástasis única o de lesiones sintomáticas mejora la calidad de vida.
Cáncer tiroideo
Las metástasis óseas son más frecuentes en los subtipos folicular y de células de Hürthle. Suelen ser líticas, bien vascularizadas, y pueden ser de crecimiento lento. La supervivencia puede ser prolongada, por lo que las indicaciones quirúrgicas deben considerar reconstrucciones duraderas. El tratamiento incluye yodo radiactivo (si el tumor capta), terapias dirigidas (lenvatinib, sorafenib) y radioterapia externa. La embolización preoperatoria puede ser útil.
Tratamiento multidisciplinar
7.1 Tratamiento sistémico
- Hormonoterapia: en tumores hormonosensibles (mama, próstata).
- Quimioterapia: según el tipo y línea de tratamiento.
- Terapias dirigidas: anti-HER2, inhibidores de tirosina quinasa (EGFR, ALK, etc.), inhibidores de mTOR, etc.
- Inmunoterapia: anti-PD-1/PD-L1 en pulmón, riñón, melanoma, etc.
- Antirresortivos: ácido zoledrónico o denosumab, asociados siempre a calcio y vitamina D (previa valoración dental). Reducen el riesgo de fracturas y la necesidad de radioterapia/cirugía.
7.2 Radioterapia
- Radioterapia paliativa: dosis única de 8 Gy o esquemas fraccionados (20 Gy/5 sesiones, 30 Gy/10 sesiones). Alivia el dolor en 60-80% de los pacientes.
- Radioterapia estereotáxica corporal (SBRT): dosis ablativas en pocas fracciones, indicada en oligometástasis, rescate tras radioterapia previa o lesiones radioresistentes (riñón, melanoma). Requiere inmovilización precisa y control de imagen.
- Radiofármacos: Ra-223 (para metástasis osteoblásticas de próstata resistente a castración sintomáticas, sin metástasis viscerales); Lu-177-PSMA (para próstata metastásica progresiva).
7.3 Tratamiento quirúrgico
- Fractura patológica establecida: osteosíntesis o reemplazo protésico según localización y expectativa de vida.
- Fijación profiláctica: basada en la escala de Mirels (ver más abajo).
- Metástasis solitaria resecable: en algunos primarios (riñón, tiroides) con buen control sistémico, la resección amplia puede ofrecer larga supervivencia.
- Cirugía de columna: descompresión y estabilización en compresión medular o inestabilidad.
- Reconstrucciones: clavos endomedulares, prótesis modulares, cementoplastia, etc. Elegir técnicas que permitan carga inmediata y sean duraderas.
7.4 Escala de Mirels (fijación profiláctica)
Evalúa el riesgo de fractura patológica en huesos largos (fémur, húmero) mediante 4 variables (localización, dolor, tipo de lesión, tamaño). Puntuación de 4 a 12:
- ≤7: bajo riesgo → tratamiento conservador.
- 8: riesgo intermedio → considerar radioterapia y reevaluar.
- ≥9: alto riesgo → indicación de fijación profiláctica.
Más detalles en nuestra página específica sobre fracturas patológicas.
7.5 Manejo de la columna vertebral: SINS y NOMS
SINS (Spine Instability Neoplastic Score): clasifica la estabilidad vertebral (0-18 puntos).
- 0-6: estable
- 7-12: potencialmente inestable (valorar cirugía)
- 13-18: inestable (indicación quirúrgica)
NOMS (Neurologic, Oncologic, Mechanical, Systemic): marco de decisión que integra el estado neurológico, la radiosensibilidad del tumor, la estabilidad mecánica y el estado sistémico del paciente.
7.6 Antirresortivos: aspectos prácticos
- Zoledronato: 4 mg IV cada 3-4 semanas (o cada 12 semanas en mantenimiento según estudios). Vigilar función renal y calcio sérico.
- Denosumab: 120 mg sc cada 4 semanas. No requiere ajuste renal, pero mayor riesgo de hipocalcemia. Obligatorio suplementar calcio y vitamina D.
- Prevención de osteonecrosis mandibular: examen dental antes de iniciar, mantener higiene bucal, evitar procedimientos invasivos durante el tratamiento.
Algoritmo diagnóstico

Resumen práctico
Indicaciones
- Radiografía simple de la lesión en dos proyecciones.
- Gammagrafía ósea de cuerpo entero con SPECT/TC (o PET/TC específico según tumor).
- TC toracoabdominopélvico con contraste (si no contraindicado).
- RM de columna completa si hay dolor o síntomas neurológicos.
- Laboratorio: calcio, FA, PSA (varones), proteinograma, LDH, marcadores específicos.
- Biopsia percutánea en caso de primario desconocido o lesión única discordante.
- Valoración por equipo multidisciplinar.
Técnica
- Radiografía: proyecciones AP y lateral incluyendo articulaciones vecinas.
- Gammagrafía: 99mTc-MDP 20-25 mCi, imágenes a las 2-4 h; SPECT/TC opcional.
- PET/TC: ayuno 6 h, glucosa <150 mg/dL; adquisición 60 min tras 18F-FDG (o según trazador).
- Biopsia: guiada por TC, aguja gruesa (14-16G), 3-5 muestras, evitar necrosis.
- TC TAP: cortes finos, fases según protocolo.
Riesgos y complicaciones
- No sospechar metástasis ante lesión ósea en >40 años.
- Biopsiar sin estudio de imagen completo.
- Omitir la determinación de PSA y proteinograma.
- No evaluar riesgo de fractura (Mirels) antes de decidir radioterapia/cirugía.
- Iniciar antirresortivos sin evaluar salud dental ni suplementar calcio/vitamina D.
- No considerar embolización preoperatoria en tumores hipervasculares.
- En columna, no valorar la estabilidad (SINS) y el estado neurológico (NOMS).
Qué esperar del resultado
- Radioterapia paliativa: alivio del dolor en 60-80% de los pacientes, con efecto completo en 4-6 semanas.
- Antirresortivos: reducción de eventos esqueléticos (fracturas, necesidad de RT/cirugía) en torno al 30-40%.
- Fijación profiláctica con Mirels ≥9 disminuye la incidencia de fracturas patológicas y mejora la función.
- La supervivencia global depende del tipo de tumor primario, biomarcadores y respuesta al tratamiento sistémico.
Bibliografía
Guías clínicas
- Coleman R, Hadji P, Body JJ, et al. Bone health in cancer: ESMO Clinical Practice Guidelines. Ann Oncol. 2020;31(12):1650-1663. doi:10.1016/j.annonc.2020.07.019
- Van Poznak C, Somerfield MR, Barlow WE, et al. Role of Bone-Modifying Agents in Metastatic Breast Cancer: ASCO Guideline Update. J Clin Oncol. 2017;35(35):3978-3986.
- Saylor PJ, Rumble RB, Tagawa S, et al. Bone Health and Bone-Targeted Therapies for Prostate Cancer: ASCO Rapid Recommendation. J Clin Oncol. 2020;38(22):2597-2600.
- Lutz S, Balboni T, Jones J, et al. Palliative radiation therapy for bone metastases: ASTRO guideline. Pract Radiat Oncol. 2024;14(5):377-397.
Fisiopatología y biomarcadores
- Weilbaecher KN, Guise TA, McCauley LK. Cancer to bone: a fatal attraction. Nat Rev Cancer. 2011;11(6):411-425.
- Coleman RE, Croucher PI, Padhani AR, et al. Bone metastases. Nat Rev Dis Primers. 2020;6(1):83.
Marcos de decisión (columna)
- Fisher CG, DiPaola CP, Ryken TC, et al. A novel classification system for spinal instability in neoplastic disease. Spine. 2010;35(22):E1221-9.
- Laufer I, Rubin DG, Lis E, et al. The NOMS framework: approach to the treatment of spinal metastatic tumors. Oncologist. 2013;18(6):744-751.
Cirugía y Mirels
- Mirels H. Metastatic disease in long bones: A proposed scoring system for diagnosing impending pathologic fractures. Clin Orthop Relat Res. 1989;(249):256-264.
- Marco RA, Sheth DS, Boland PJ, et al. Functional and oncological outcome of acetabular reconstruction for the treatment of metastatic disease. J Bone Joint Surg Am. 2000;82(5):642-651.
Radiofármacos
- Sartor O, de Bono J, Chi KN, et al. Lutetium-177–PSMA-617 for Metastatic Castration-Resistant Prostate Cancer. N Engl J Med. 2021;385(12):1091-1103.
- Parker C, Nilsson S, Heinrich D, et al. Alpha emitter radium-223 and survival in metastatic prostate cancer. N Engl J Med. 2013;369(3):213-223.
¿Todavía con dudas?
consulta nuestras preguntas frecuentes para pacientes.
