Fracturas Patológicas — Evaluación del Riesgo y Manejo Multidisciplinar 2026
Fractura que ocurre en un hueso previamente debilitado por una condición patológica (neoplásica, metabólica, infecciosa o displásica) tras un traumatismo de baja energía o durante la actividad normal. Su prevención y manejo óptimo requieren un enfoque proactivo, multidisciplinar y basado en la evaluación objetiva del riesgo para reducir la morbilidad y mejorar la calidad de vida del paciente.
En 1 minuto
Fractura por fragilidad ósea debido a enfermedad subyacente (cáncer, osteoporosis, etc.).
Prevención. La fijación profiláctica tiene mejores resultados que el tratamiento de la fractura establecida.
Adulto con cáncer conocido (mama, próstata, pulmón, riñón, mieloma) y dolor óseo mecánico/localizado.
Fémur proximal (cuello y región pertrocanterea), diáfisis femoral, húmero proximal, columna (cuerpos vertebrales).
Score de Mirels modificado + criterios clínicos (dolor funcional) + imagen avanzada (TC/RM) para cuantificar.
Equipo multidisciplinar. Estabilización quirúrgica profiláctica si riesgo alto, seguida de radioterapia adyuvante y tratamiento sistémico específico.
Definición y contexto clínico
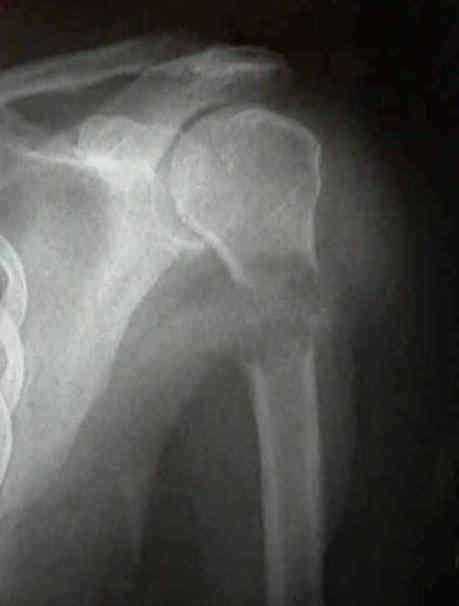
Impacto clínico
- Morbilidad significativa: Dolor intenso, pérdida de movilidad, deterioro funcional.
- Complicaciones: Retraso en el tratamiento oncológico sistémico, complicaciones de la inmovilización (tromboembolismo, úlceras por presión).
- Pronóstico: La fractura patológica establecida se asocia a peor calidad de vida, mayor estancia hospitalaria y coste, y cirugía más compleja que la profiláctica.
¿Por qué prevenir es clave?
- Procedimiento quirúrgico más sencillo y predecible.
- Rehabilitación más rápida y restauración de la función.
- Permite radioterapia adyuvante temprana y eficaz.
- Control del dolor más inmediato y menor morbilidad global.
Estrategia: Enfoque proactivo y multidisciplinar
El cirujano ortopédico oncólogo debe integrarse en el equipo oncológico desde el diagnóstico de enfermedad ósea. El objetivo es identificar proactivamente a los pacientes en riesgo y ofrecer estabilización antes de la fractura.
| Aspecto | Fijación Profiláctica (Prevención) | Tratamiento de Fractura Establecida |
|---|---|---|
| Complejidad quirúrgica | Menor. Planificación electiva, hueso más íntegro. | Mayor. Reducción de fragmentos, pérdida ósea, inestabilidad. |
| Tasa de complicaciones | Más baja | Más alta (infección, no unión, fallo del implante) |
| Recuperación funcional | Más rápida y completa | Más lenta, a menudo con limitaciones residuales |
| Control del dolor postoperatorio | Más eficaz e inmediato | Puede ser difícil por daño tisular previo |
| Impacto en el tratamiento oncológico | Mínimo. Permite continuar/quimio/radioterapia pronto. | Puede retrasar o suspender el tratamiento sistémico. |
Evaluación del Riesgo de Fractura Patológica — Factores Clave 2026
1. Dolor (Factor Clínico Fundamental)
- Dolor en reposo: Sugiere crecimiento tumoral/edema.
- Dolor mecánico / con la carga (FUNCIONAL): Es el predictor clínico más importante de debilidad estructural e fractura inminente.
- Dolor que persiste tras radioterapia: Indica fracaso del tratamiento local y riesgo alto.
Interpretación: El dolor funcional tiene una correlación alta con riesgo de fractura. No ignorarlo.
2. Características Radiológicas de la Lesión
- Tamaño: Lesión >2.5-3 cm de diámetro. Compromiso >50% del diámetro cortical (vista en TC).
- Localización: Alto riesgo: Fémur proximal (cuello, subtrocantérea), diáfisis femoral, húmero proximal. Riesgo extremo: Lesiones pertrocantéreas y subtrocantéreas.
- Naturaleza: Lesiones líticas puras son más débiles que las blásticas o mixtas. Las blásticas alteran la rigidez pero también son de riesgo.
3. Tipo de Tumor y Respuesta al Tratamiento
- Tumores radioresistentes (cáncer renal, tiroideo, melanoma): Mayor riesgo de progresión y fractura tras radioterapia.
- Respuesta a tratamiento sistémico: Lesiones que no responden a quimioterapia/hormonoterapia/bifosfonatos mantienen el riesgo.
- Historia de radioterapia local: Puede causar osteorradionecrosis y fragilidad ósea tardía.
4. Actividad y Expectativas del Paciente
- Pacientes ambulatorios activos vs. pacientes encamados.
- Expectativa de vida >1 mes (umbral para considerar cirugía).
- Estado general y comorbidities.
Score de Mirels — Sistema de Puntuación (Revisión Práctica 2026)
Sistema semicuantitativo que combina 4 factores clínico-radiológicos. Sigue siendo la herramienta más utilizada y validada para la toma de decisiones. Se recomienda su uso junto al criterio clínico.
| Variable | 1 punto | 2 puntos | 3 puntos |
|---|---|---|---|
| Localización | Miembro superior | Miembro inferior (excepto peritrocanterea) | Región peritrocanterea / cuello femoral |
| Dolor | Leve / ocasional | Moderado / con actividad | Severo / en reposo / funcional (con la carga) |
| Carácter de la lesión | Blástica | Mixta | Lítica pura |
| Tamaño de la lesión* | < 1/3 del diámetro cortical | 1/3 a 2/3 del diámetro cortical | > 2/3 del diámetro cortical |
Interpretación y Recomendaciones 2026
- ≤ 7 puntos: Riesgo bajo. Tratamiento oncológico conservador (radioterapia, bifosfonatos). Observación ortopédica.
- 8 puntos: Riesgo intermedio (15-30%). Individualizar. Si hay dolor funcional o tumor radioresistente, considerar cirugía. Seguimiento estrecho.
- ≥ 9 puntos: Riesgo alto (>30%). Indicación de estabilización quirúrgica profiláctica (previo a fractura).
Limitaciones y Consideraciones
- Tamaño: Difícil de medir con precisión en radiografía simple. Usar TC para cuantificar el compromiso cortical (%).
- Subjetividad del dolor: Valorar siempre en contexto.
- No aplica bien a: Columna, pelvis, costillas. Para columna, usar criterios de inestabilidad (SINS score).
- Complementar siempre con juicio clínico y características del tumor.
*Nota sobre el tamaño: La medición debe hacerse en la vista donde la lesión parezca más grande y evaluando el compromiso cortical en porcentaje, preferiblemente con TC. Una destrucción cortical >50% (Fidler) o lesión que ocupe >2/3 del diámetro (Mirels) son indicadores fuertes de riesgo alto.
Algoritmo práctico de evaluación y manejo inicial
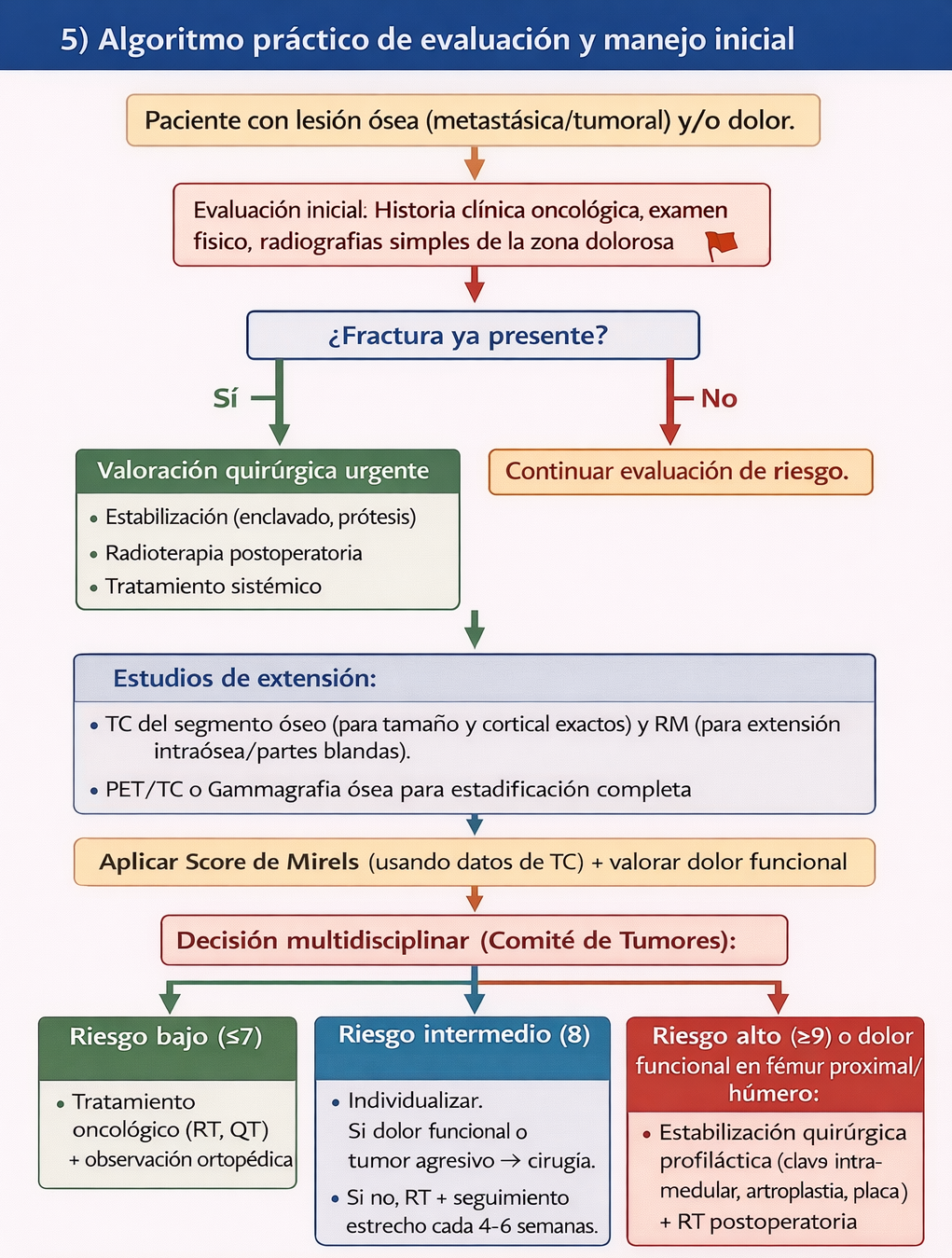
- Paciente con lesión ósea (metastásica/tumoral) y/o dolor.
- Evaluación inicial: Historia clínica oncológica, examen físico, radiografías simples de la zona dolorosa.
- ¿Fractura ya presente?
- SÍ → Valoración quirúrgica urgente. Estabilización (enclavado, prótesis) + radioterapia postoperatoria + tratamiento sistémico.
- NO → Continuar evaluación de riesgo.
- Estudios de extensión: TC del segmento óseo (para tamaño y cortical exactos) y RM (para extensión intraósea/partes blandas). PET/TC o Gammagrafía ósea para estadificación completa.
- Aplicar Score de Mirels (usando datos de TC) + valorar dolor funcional.
- Decisión multidisciplinar (Comité de Tumores):
- Riesgo bajo (≤7): Tratamiento oncológico (RT, QT) + observación ortopédica.
- Riesgo intermedio (8): Individualizar. Si dolor funcional o tumor agresivo → cirugía. Si no, RT + seguimiento estrecho cada 4-6 semanas.
- Riesgo alto (≥9) o dolor funcional en fémur proximal/húmero: Estabilización quirúrgica profiláctica (clavo intramedular, artroplastia, placa) + RT postoperatoria.
- Seguimiento: Reevaluación clínica y radiológica periódica según el plan establecido.
Estudio del paciente con sospecha de fractura patológica
Laboratorio (orientación diagnóstica)
- Hemograma, VSG/Proteína C Reactiva: Anemia (mieloma, metástasis), infección.
- Calcio sérico, fosfatasas alcalinas: Hipercalcemia maligna, metástasis osteoblásticas.
- Proteinograma e inmunofijación: Para mieloma múltiple.
- PSA (hombres), marcadores tumorales: Según sospecha.
- Función renal/hepática: Para planificar tratamiento.
Estudios de Imagen (Protocolo 2026)
- Radiografía simple: Estudio inicial. Buscar lesión lítica/blástica, destrucción cortical, fractura.
- Tomografía Computarizada (TC): Obligatoria para cuantificar riesgo. Mide con precisión el tamaño, compromiso cortical (%) y destrucción trabecular. Ideal para planificar cirugía/biopsia.
- Resonancia Magnética (RM): Evalúa extensión intraósea (edema), invasión de partes blandas, compresión medular (en columna). Diferenciar tumor de fractura benigna.
- PET/TC con 18F-FDG o 18F-NaF: Estándar para estadificación sistémica. Identifica lesiones adicionales y actividad metabólica.
- Gammagrafía ósea: Útil si no hay PET, especialmente para metástasis osteoblásticas (próstata). Menor sensibilidad en lesiones puramente líticas.
Biopsia
Regla: Toda lesión ósea solitaria sospechosa en un paciente sin diagnóstico oncológico conocido debe biopsiarse antes del tratamiento definitivo (excepción: patrón típico de lesión benigna).
- Biopsia con aguja gruesa (Tru-Cut) guiada por TC: Método de elección. Alta precisión diagnóstica.
- Biopsia abierta: Si la percutánea no es diagnóstica o se necesita más tejido para estudios moleculares.
- Cultivo: Siempre enviar muestra si hay sospecha de infección (osteomielitis).
Principales etiologías (Diagnóstico Diferencial)
1. Enfermedad Metastásica (Causa más frecuente en adultos)
- Cánceres primarios: Mama, próstata, pulmón, riñón, tiroides.
- Características: Múltiples lesiones frecuentes. Líticas, blásticas o mixtas.
2. Tumores Primarios Malignos
- Mieloma Múltiple: Lesiones líticas "perforadas" muy frecuentes.
- Sarcoma de Ewing, Osteosarcoma, Condrosarcoma: En pacientes más jóvenes.
3. Lesiones Benignas Agresivas / Tumor-like
- Tumor de Células Gigantes: Subarticular, lítico expansivo.
- Quiste Óseo Simple (Unicameral), Quiste Aneurismático.
- Fibroma No Osificante / Defecto Fibroso Cortical (grandes).
- Displasia Fibrosa, Enfermedad de Paget.
4. Enfermedades Metabólicas / Sistémicas
- Osteoporosis severa (la causa más común global).
- Osteomalacia / Raquitismo.
- Osteogénesis Imperfecta.
- Hiperparatiroidismo (tumor pardo).
- Osteopetrosis, Enfermedad de Gaucher.
5. Infección
- Osteomielitis crónica: Puede debilitar el hueso y provocar fractura patológica.
6. Otras
- Osteorradionecrosis: Fractura en hueso previamente irradiado (riesgo años después).
- Infarto óseo.
Tratamiento multidisciplinar integral
A) Tratamiento Quirúrgico (Principios)
Objetivo: Estabilidad inmediata y duradera que permita carga y alivio del dolor.
- Fijación Interna con Injerto/ Sustituto: Para fracturas o lesiones en riesgo en huesos largos. Enclavado intramedular bloqueado (fémur, tibia, húmero) es el patrón oro. Permite estabilizar todo el hueso (lesiones múltiples).
- Artroplastia (Prótesis): Indicada en fracturas/lesiones articulares (cabeza femoral, humeral, cóndilos) o con gran destrucción de la metáfisis. Proporciona estabilidad inmediata y permite carga completa.
- Resección en Bloque + Reconstrucción: Para tumores primarios (benignos agresivos o malignos) en pacientes seleccionados.
- Vertebroplastia / Cifoplastia: Para fracturas vertebrales dolorosas sin inestabilidad ni compresión medular.
- Cirugía de la columna: Descompresión y estabilización instrumentada para metástasis con compresión medular o inestabilidad (score SINS alto).
B) Radioterapia (RT)
Objetivo: Control local del tumor, alivio del dolor, promover la re-ossificación.
- RT Externa: Adyuvante postquirúrgica estándar (30-35 Gy en 10-15 fracciones). Disminuye la progresión local y el dolor.
- RT preoperatoria: Menos común (riesgo de complicaciones de cicatrización). Se prefiere postoperatoria.
- RT estereotáxica corporal (SBRT): Para lesiones únicas, radioresistentes o en localizaciones complejas (columna). Dosis alta y precisa.
- RT paliativa: Para fracturas no operables o metástasis múltiples.
C) Tratamiento Sistémico Oncológico
- Quimioterapia / Hormonoterapia / Terapia Dirigida / Inmunoterapia: Según el tumor primario. Esencial para el control de la enfermedad global.
- Radiofármacos (Ra-223, Sm-153): Para metástasis óseas dolorosas múltiples (especialmente de próstata).
D) Terapia Ósea Adyuvante
- Bifosfonatos (ácido zoledrónico) / Denosumab (Xgeva®): Estándar de cuidado. Reducen eventos esqueléticos (fracturas patológicas, necesidad de RT o cirugía), retrasan la progresión de las metástasis y alivian el dolor óseo.
- Calcio y Vitamina D: Suplementación en todos los pacientes, salvo contraindicación.
E) Ablación Percutánea (Radiología Intervencionista)
Alternativa o adyuvante para lesiones pequeñas (<3 cm) o en pacientes no candidatos a cirugía.
- Ablación por Radiofrecuencia (RF) / Crioablación: Destruye el tumor y alivia el dolor. Puede consolidar la lesión.
- Cemento óseo (vertebroplastia): Para lesiones vertebrales o en huesos planos.
Novedades y perspectivas futuras (2026)
Evaluación del riesgo
- Análisis de Imagen por IA (Radiómica): Algoritmos que analizan TC/RM para predecir el riesgo de fractura con mayor precisión que el ojo humano, integrando textura ósea, microarquitectura y carga tumoral.
- Modelos biomecánicos personalizados (FEA - Análisis de Elementos Finitos): A partir de TC, calculan la resistencia ósea residual y predicen el riesgo de fractura. En investigación, promete mayor objetividad.
- Biomarcadores en suero: Marcadores de remodelado óseo (CTX, PINP) y relacionados con el tumor para estratificar el riesgo dinámicamente.
Tratamiento
- Implantes mejorados: Prótesis y clavos con recubrimientos antitumorales o que permiten la administración local de quimioterapia/radiofármacos.
- Cirugía guiada por navegación y robótica: Mayor precisión en la colocación de implantes, especialmente en columna y pelvis.
- Terapias sistémicas de nueva generación: Nuevos inhibidores de RANKL, conjugados anticuerpo-fármaco (ADCs), y combinaciones de inmunoterapia que mejoran el control óseo.
- Terapias focales de alta precisión: Mayor uso de SBRT y terapia con protones para un control tumoral local más duradero con menos toxicidad.
Referencias clave (2020–2026)
Evaluación del riesgo y score de Mirels
- Mirels H. Metastatic disease in long bones. A proposed scoring system for diagnosing impending pathologic fractures. Clin Orthop Relat Res. 1989. [Clásico, aún vigente].
- Howard EL, et al. A systematic review and meta-analysis of the Mirels score for predicting impending pathologic fractures. J Bone Oncol. 2022.
- van der Linden YM, et al. Comparative effectiveness of different radiotherapy fractionation schedules for bone metastases: A systematic review and network meta-analysis. Lancet Oncol. 2021.
- Ruggieri P, et al. The need for a multidisciplinary approach in bone metastasis management: The orthopaedic surgeon's role. J Orthop Traumatol. 2023.
Tratamiento y guías de práctica clínica
- NCCN Guidelines. Survival, Symptom, and Quality of Life Management (Version 2.2025). Sección de Cuidados de Soporte: Manejo de Metástasis Óseas.
- ESMO Guidelines. Management of bone health in patients with solid tumours. Ann Oncol. 2022 (actualización).
- American College of Radiology (ACR) Appropriateness Criteria. Management of Metastatic Bone Disease. 2023.
- Society for Surgical Oncology (SSO) / Musculoskeletal Tumor Society (MSTS). Consensus guidelines on the surgical management of metastatic bone disease. Ann Surg Oncol. 2024.
Terapia ósea adyuvante y sistémica
- Coleman R, et al. Bone health in cancer: ESMO Clinical Practice Guidelines. Ann Oncol. 2020.
- Smith MR, et al. Denosumab for the prevention of skeletal complications in metastatic castration-resistant prostate cancer: comparison of skeletal-related events and symptomatic skeletal events. Ann Oncol. 2023.
- Lipton A, et al. Zoledronic acid and survival in patients with metastatic bone disease from solid tumors and elevated bone resorption. Cancer. 2021.
Nuevas tecnologías e investigación
- Eggermont F, et al. CT-based finite element models can be used to estimate clinically relevant fracture risk indices in patients with metastatic bone disease. Bone. 2022.
- Jhaveri PM, et al. Stereotactic body radiotherapy for de novo spinal metastases: systematic review and international practice patterns. Neurosurgery. 2023.
- Deschamps F, et al. Thermal ablation of bone metastases: a systematic review and meta-analysis. Int J Hyperthermia. 2021.
Resumen para la práctica clínica
📌 Indicaciones
- ✓ Paciente con lesión ósea metastásica o primaria que causa dolor mecánico/funcional.
- ✓ Evaluación de riesgo de fractura patológica en huesos largos (especialmente fémur proximal y húmero).
- ✓ Planificación de estabilización quirúrgica profiláctica en lesiones de alto riesgo.
- ✓ Manejo multidisciplinar de fractura patológica ya establecida.
🔧 Técnica
- 🔧 Radiografía simple y TC para cuantificar tamaño y compromiso cortical.
- 🔧 RM para evaluar extensión intraósea y partes blandas.
- 🔧 Score de Mirels (con TC) + valoración de dolor funcional.
- 🔧 Biopsia guiada por imagen si no hay diagnóstico oncológico previo.
- 🔧 Estabilización quirúrgica (enclavado, artroplastia) según localización y grado de destrucción.
- 🔧 Radioterapia adyuvante postquirúrgica (30-35 Gy).
- 🔧 Terapia ósea adyuvante (bifosfonatos/denosumab) y tratamiento sistémico oncológico.
⚠️ Riesgos
- ⚠️ Fractura patológica inminente con deterioro funcional y dolor severo.
- ⚠️ Complicaciones quirúrgicas (infección, fallo de implante, no unión).
- ⚠️ Retraso en el tratamiento oncológico sistémico por la fractura.
- ⚠️ Metástasis a distancia no controladas.
- ⚠️ Mala respuesta a radioterapia en tumores radioresistentes.
✅ Resultados
- ✅ Prevención de fractura en >90% de los casos tratados profilácticamente.
- ✅ Mejor control del dolor y calidad de vida con estabilización quirúrgica precoz.
- ✅ Rehabilitación más rápida y menor estancia hospitalaria en comparación con fractura establecida.
- ✅ Seguimiento periódico para detectar progresión y nuevos eventos.
