Lesiones radiolucentes del hueso — Actualización 2026: enfoque sistemático basado en el patrón de destrucción, la edad, la localización y la matriz
Las lesiones radiolucentes del hueso constituyen uno de los hallazgos más frecuentes y a la vez más desafiantes en la práctica traumatológica, radiológica y oncológica. A diferencia de las lesiones esclerosas, que indican un proceso de crecimiento lento, las lesiones líticas abarcan un espectro que va desde procesos benignos autolimitados (fibroma no osificante, quiste óseo solitario) hasta neoplasias altamente agresivas con potencial metastásico (osteosarcoma, sarcoma de Ewing, metástasis). La clave para una interpretación correcta reside en un enfoque sistemático basado en cuatro pilares: el patrón de destrucción ósea (geográfico, apolillado, permeativo), la edad del paciente, la localización anatómica (epífisis, metáfisis, diáfisis) y las características de la matriz tumoral. Esta ficha, actualizada a 2026, desarrolla el clásico nemotécnico FOGMACHINES y lo jerarquiza en un algoritmo diagnóstico moderno que incorpora los avances en resonancia magnética funcional, la reclasificación OMS 2020-2025 de tumores óseos y los criterios actualizados de derivación a centros de referencia. Se eliminan aproximaciones puramente memorísticas sin contexto clínico-radiológico, sustituyéndolas por una sistemática de razonamiento basada en probabilidades pretest según grupos de edad y patrones radiológicos.
En 1 minuto
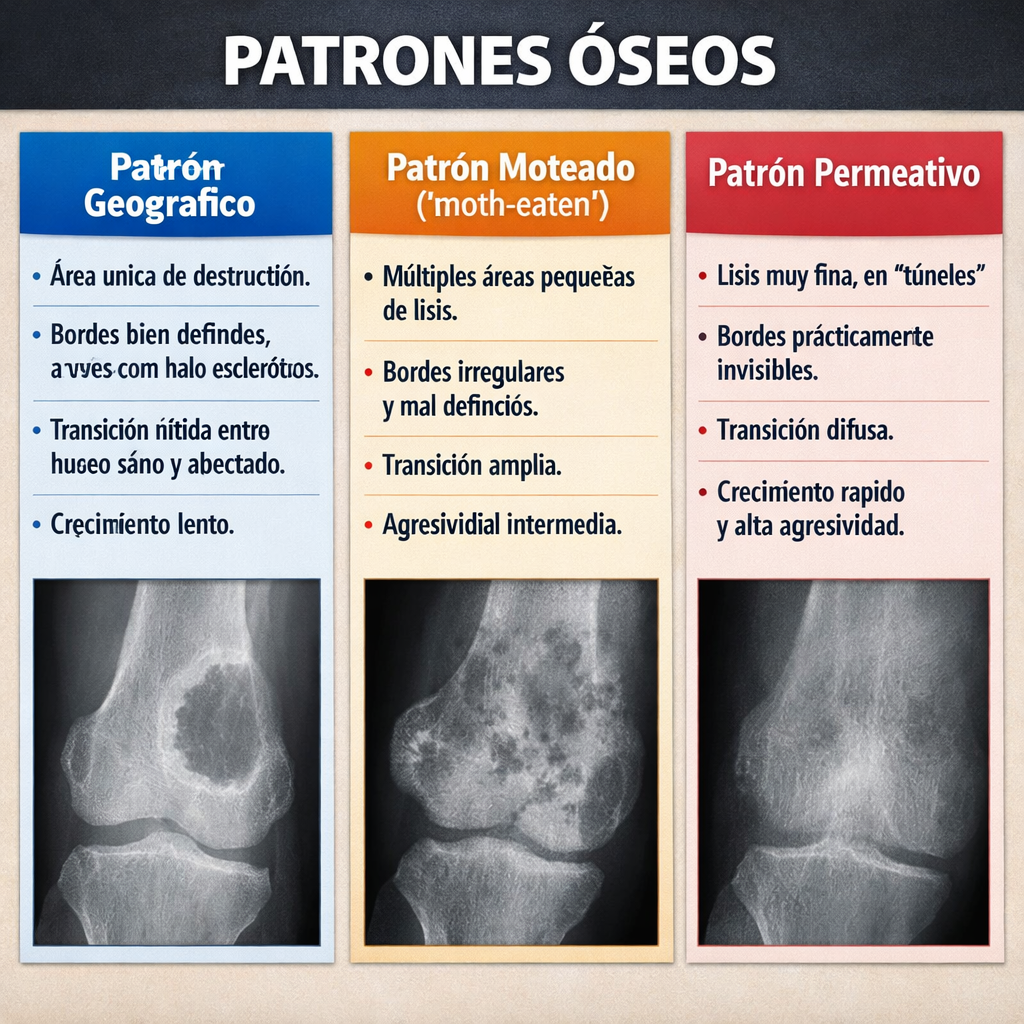
El patrón de destrucción ósea refleja la velocidad de crecimiento. A mayor agresividad, peor definición del margen.
Geográfico (benigno), apolillado (agresivo), permeativo (muy agresivo).
<10a: neuroblastoma, histiocitosis, Ewing. 10-25a: osteosarcoma, Ewing. 20-40a: TCG, displasia fibrosa. >40a: metástasis, mieloma.
Epífisis: TCG, condroblastoma. Metáfisis: osteosarcoma, encondroma. Diáfisis: Ewing, adamantinoma.
Nemotecnia para lesión única. Aplicar con filtro de edad y localización.
FEMHI: Fibrosa, Eosinófilo/Encondroma, Metástasis/Mieloma, Hiperparatiroidismo, Infección.
Conceptos generales
1.1 Fisiopatología de la osteólisis
El hueso se destruye exclusivamente por acción de los osteoclastos. Las células tumorales no destruyen la matriz ósea directamente; secretan factores (RANKL, PTHrp, IL-6, IL-11, TNF-α) que activan los osteoclastos, produciendo lagunas de resorción. La velocidad de destrucción determina la capacidad del hueso huésped para reaccionar:
- Crecimiento lento: El hueso tiene tiempo para formar un borde esclerótico de contención. → Patrón geográfico con esclerosis.
- Crecimiento moderado: El hueso solo puede retirarse, sin formar esclerosis. → Patrón geográfico sin esclerosis.
- Crecimiento rápido: No hay tiempo para una retirada ordenada. → Patrón apolillado o permeativo.
1.2 Estrategia diagnóstica: cuatro preguntas clave
- ¿Cuál es el patrón de destrucción? ¿Geográfico (con/sin esclerosis), apolillado o permeativo?
- ¿Cuál es la edad del paciente? El dato clínico más rentable.
- ¿Cuál es la localización precisa? ¿Epífisis, metáfisis, diáfisis? ¿Hueso específico? ¿Región del hueso?
- ¿Hay matriz tumoral calcificada? ¿Condroide (anillos y arcos) u osteoide (denso, algodonoso)?
Patrones de destrucción ósea (clasificación de Lodwick)
2.1 Patrón geográfico (tipo I)
- Definición: Lesión única, bien delimitada, con bordes definidos. Corresponde a un crecimiento lento (benigno o de bajo grado).
- Tipo IA: Borde esclerótico grueso y bien definido. Benigno inactivo (quiste óseo, fibroma no osificante, encondroma).
- Tipo IB: Borde bien definido sin esclerosis. Benigno activo (tumor de células gigantes, condroblastoma, osteoblastoma).
- Tipo IC: Borde mal definido, lobulado, parcialmente esclerótico. Agresividad local (tumor de células gigantes agresivo, condrosarcoma grado 1, displasia fibrosa).
2.2 Patrón apolillado (tipo II)
- Definición: Múltiples lucencias pequeñas (2-5 mm) coalescentes, que confluyen formando áreas más grandes. Bordes mal definidos.
- Significado: Crecimiento rápido, agresivo. El hueso huésped no ha tenido tiempo de reaccionar.
- Diagnósticos: Osteosarcoma, condrosarcoma de alto grado, metástasis, linfoma, osteomielitis.
2.3 Patrón permeativo (tipo III)
- Definición: Innumerables lucencias puntiformes (<2 mm) que se extienden a lo largo del hueso, respetando inicialmente la cortical. Transición imperceptible entre hueso normal y patológico.
- Significado: Crecimiento muy rápido, altamente agresivo.
- Diagnósticos: Sarcoma de Ewing, linfoma, metástasis de células redondas, osteomielitis aguda. También puede verse en histiocitosis y leucemia.
- Clave: El patrón permeativo con reacción perióstica en capas de cebolla es sarcoma de Ewing hasta que se demuestre lo contrario.
2.4 Imagen: patrones de destrucción
Los patrones radiológicos clásicos (geográfico, apolillado, permeativo) son la herramienta más rentable para predecir la agresividad biológica y deben ser evaluados en toda radiografía simple antes de solicitar RM o TC.
FOGMACHINES: diagnóstico diferencial de lesión lítica única
El nemotécnico FOGMACHINES ha sido utilizado durante décadas en radiología musculoesquelética. Sin embargo, debe aplicarse con criterio clínico-radiológico, no como una lista mecánica. A continuación se presenta actualizado con la nomenclatura OMS 2020-2025 y los criterios radiológicos clave.
| Nemotecnia | Entidad | Edad típica | Localización | Clave radiológica |
|---|---|---|---|---|
| F | Displasia fibrosa | 10-30 años | Metáfisis-diáfisis, costillas, cráneo | Vidrio deslustrado, matriz sin calcificación, expansión, deformidad en cayado de pastor |
| O | Osteoblastoma | 20-40 años | Elementos posteriores vertebrales, metáfisis | >2 cm, lítico-expansivo, matriz osteoide variable, esclerosis marginal |
| G | Tumor de células gigantes (TCG) | 20-40 años | Epífisis, fisis cerrada, rodilla, extremo distal radio | Lítico, geográfico sin esclerosis, excéntrico, hasta el cartílago articular |
| M | Metástasis / Mieloma | >40 años | Columna, pelvis, costillas, cráneo | Múltiples o única, permeativo/apolillado, sin matriz, VSG elevada, proteinograma |
| A | Quiste óseo aneurismático (QOA) | 10-20 años | Metáfisis, elementos posteriores vertebrales | Expansivo, tabiques, niveles líquido-líquido (RM), pueden ser secundarios |
| C | Condroblastoma / Fibroma condromixoide | 10-25 años (Condroblastoma) 10-30 años (Fibroma condromixoide) |
Epífisis (Condroblastoma) Metáfisis tibia (Fibroma condromixoide) |
Condroblastoma: lítico epifisario, calcificaciones, esclerosis. Fibroma condromixoide: excéntrico, lobulado, esclerosis |
| H | Hiperparatiroidismo (tumor pardo) / Hemangioma | >40 años / Cualquiera | Mandíbula, pelvis, costillas / Vértebras, cráneo | Tumor pardo: PTH elevada, osteopenia, otras lesiones. Hemangioma: vértebra en panal, cráneo en rueda de carro |
| I | Infección (osteomielitis) | Cualquiera | Metáfisis | Clínica, secuestro, tractos sinuosos, reacción perióstica sólida |
| N | Fibroma no osificante (FNO) | 10-20 años | Metáfisis, cortical, excéntrico | Lesión lítica excéntrica, multiseptada, esclerosis marginal, respeta epífisis |
| E | Granuloma eosinófilo (Histiocitosis) / Encondroma | 5-15 años / 20-50 años | Diáfisis, cráneo / Metáfisis, manos | Granuloma: permeativo, botón a botón, secuestro. Encondroma: matriz condroide, expansión endóstica |
| S | Quiste óseo solitario (QOS) | 5-15 años | Metáfisis proximal húmero, fémur | Central, geográfico, esclerosis, signo de la gota (fragmento óseo en declive) |
Edad del paciente: el dato clínico más rentable
La edad es el factor predictivo más potente en el diagnóstico de tumores óseos. Según Edeiken, aproximadamente el 80% de los tumores óseos malignos pueden diagnosticarse correctamente en base a la edad y la localización. La tabla siguiente ha sido actualizada según las series del Rizzoli, Mayo Clinic y los registros SEER 2020-2025.
| Grupo de edad | Tumores benignos frecuentes | Tumores malignos frecuentes |
|---|---|---|
| 0-5 años | Histiocitosis de células de Langerhans, quiste óseo unicameral | Metástasis de neuroblastoma, leucemia |
| 5-10 años | Quiste óseo unicameral, quiste óseo aneurismático, histiocitosis | Sarcoma de Ewing (huesos tubulares), leucemia, linfoma |
| 10-25 años | Osteocondroma, osteoma osteoide, osteoblastoma, encondroma, condroblastoma, fibroma no osificante, displasia fibrosa | Osteosarcoma convencional, sarcoma de Ewing (huesos planos) |
| 20-40 años | Tumor de células gigantes, condroblastoma, osteoblastoma, fibroma condromixoide | Osteosarcoma de bajo grado, condrosarcoma grado 1, adamantinoma, linfoma |
| 40-60 años | Encondroma (manos/pies) | Condrosarcoma convencional, linfoma, osteosarcoma secundario (Paget, postradiación) |
| >60 años | Hemangioma vertebral | Metástasis óseas, mieloma múltiple, condrosarcoma, osteosarcoma secundario |
* En pacientes >40 años, una lesión lítica única o múltiple es metástasis o mieloma hasta que se demuestre lo contrario. El condrosarcoma es la excepción.
Localización anatómica
5.1 Localización en el hueso largo
- Epífisis:
- Fisis abierta: Condroblastoma (casi exclusivo). Osteomielitis.
- Fisis cerrada: Tumor de células gigantes (patognomónico). También: encondroma, quiste óseo aneurismático (raro).
- Metáfisis:
- Localización más frecuente de la mayoría de tumores óseos: osteosarcoma, encondroma, quiste óseo solitario, quiste óseo aneurismático, fibroma no osificante (excéntrico), displasia fibrosa, osteoblastoma, condrosarcoma central.
- La osteomielitis también es metafisaria.
- Diáfisis:
- Sarcoma de Ewing, adamantinoma (tibia), displasia fibrosa, histiocitosis, linfoma, mieloma, osteoma osteoide (cortical).
- Las metástasis también pueden ser diafisarias.
- Localización excéntrica (cortical): Fibroma no osificante, osteoma osteoide, adamantinoma, metástasis (raro).
- Localización central (medular): Quiste óseo solitario, encondroma, displasia fibrosa, tumor de células gigantes.
5.2 Localización en el esqueleto axial
- Columna vertebral:
- Cuerpo vertebral: Hemangioma, metástasis, mieloma, histiocitosis (niños), enfermedad de Paget, linfoma.
- Elementos posteriores (arco, pedículos, apófisis): Osteoblastoma, osteoma osteoide, quiste óseo aneurismático. Una lesión en elementos posteriores en niño/adolescente es un tumor primario hasta que se demuestre lo contrario.
- Pelvis: Condrosarcoma, sarcoma de Ewing, metástasis, mieloma, tumor de células gigantes.
- Costillas: Displasia fibrosa, condrosarcoma, sarcoma de Ewing, histiocitosis, metástasis.
- Cráneo y mandíbula: Histiocitosis, osteoma, tumor de células gigantes, quiste óseo aneurismático, displasia fibrosa, metástasis.
- Esternón: Las lesiones líticas del esternón deben considerarse malignas hasta que se demuestre lo contrario (condrosarcoma, metástasis, linfoma).
5.3 Equivalentes epifisarios
Ciertos huesos y apófisis son equivalentes epifisarios a efectos del diagnóstico diferencial: la rótula, el calcáneo, el olecranon, el trocánter mayor y la cabeza del peroné. Las lesiones líticas en estas localizaciones deben incluir las mismas entidades que las lesiones epifisarias: condroblastoma, tumor de células gigantes y quiste óseo aneurismático.
Matriz tumoral
La matriz es el material producido por las células tumorales. Para ser visible en radiografía simple, debe estar calcificada. La identificación del tipo de matriz permite clasificar el tumor en una de tres categorías: productor de cartílago, productor de hueso u otro (sin matriz calcificada).
6.1 Matriz condroide (cartilaginosa)
- Aspecto radiológico: Calcificaciones punteadas, curvilíneas, en anillos y arcos, en palomitas de maíz. Son calcificaciones distróficas del cartílago hialino.
- Entidades: Encondroma, condrosarcoma, condroblastoma (10-30%), fibroma condromixoide, osteocondroma (calcificación del capuchón).
- Clave: La presencia de matriz condroide en una lesión lítica metafisaria/diafisaria es un encondroma hasta que el tamaño, la erosión cortical y el dolor sugieran condrosarcoma.
6.2 Matriz osteoide (ósea)
- Aspecto radiológico: Densidad algodonosa, nubosa, en puré de patatas. Hueso tumoral desorganizado, sin arquitectura trabecular.
- Entidades: Osteosarcoma convencional, osteoblastoma (20-30%), osteoma osteoide (nidus ± calcificación central).
- Clave: La matriz osteoide en una lesión metafisaria agresiva en un adolescente es osteosarcoma hasta que se demuestre lo contrario.
6.3 Sin matriz calcificada
- Lesiones puramente líticas: Tumor de células gigantes, quiste óseo solitario, quiste óseo aneurismático, fibroma no osificante, displasia fibrosa (puede tener vidrio deslustrado, no calcificaciones), sarcoma de Ewing, linfoma, mieloma, metástasis.
- Clave: La ausencia de matriz no excluye malignidad. De hecho, la mayoría de las metástasis, el mieloma y el sarcoma de Ewing no tienen matriz calcificada.
Reacción perióstica
- Sólida, continua: Periostitis benigna (fractura en consolidación, osteoma osteoide, osteoblastoma, osteomielitis crónica).
- Lamellada (en capas de cebolla): Tradicionalmente asociada a sarcoma de Ewing, pero es inespecífica (osteomielitis, linfoma, histiocitosis).
- Espiculada (sol naciente, en barba): Osteosarcoma (neoformación ósea radial).
- Triángulo de Codman: Elevación del periostio interrumpida por el tumor. Osteosarcoma, sarcoma de Ewing, infección agresiva.
- Compleja/amorfa: Tumores agresivos.
Lesiones líticas múltiples
El diagnóstico diferencial de las lesiones líticas múltiples es completamente diferente al de las lesiones únicas. Muchas entidades de FOGMACHINES no tienen sentido en forma múltiple. El nemotécnico recomendado es FEMHI.
| Nemotecnia | Entidad | Claves diagnósticas |
|---|---|---|
| F | Displasia fibrosa poliostótica | Vidrio deslustrado, deformidades, asimetría, manchas café con leche (síndrome de McCune-Albright) |
| E | Granuloma eosinófilo (Histiocitosis) / Encondromatosis | Granuloma: vértebra plana, lesión en botón a botón. Encondromatosis: matriz condroide, enfermedad de Ollier/Maffucci |
| M | Metástasis / Mieloma múltiple | >40 años, lesiones punteadas, sacabocados. Mieloma: proteinograma, inmunofijación. Metástasis: PSA, CA 15.3, antecedente |
| H | Hiperparatiroidismo (tumores pardos) / Hemangiomatosis | Tumor pardo: PTH elevada, osteopenia, resorción subperióstica. Hemangiomatosis: lesiones esclerosas/líticas mixtas |
| I | Infección (osteomielitis multifocal) | Clínica, secuestros, fístulas, cultivo |
Algoritmo diagnóstico integrado
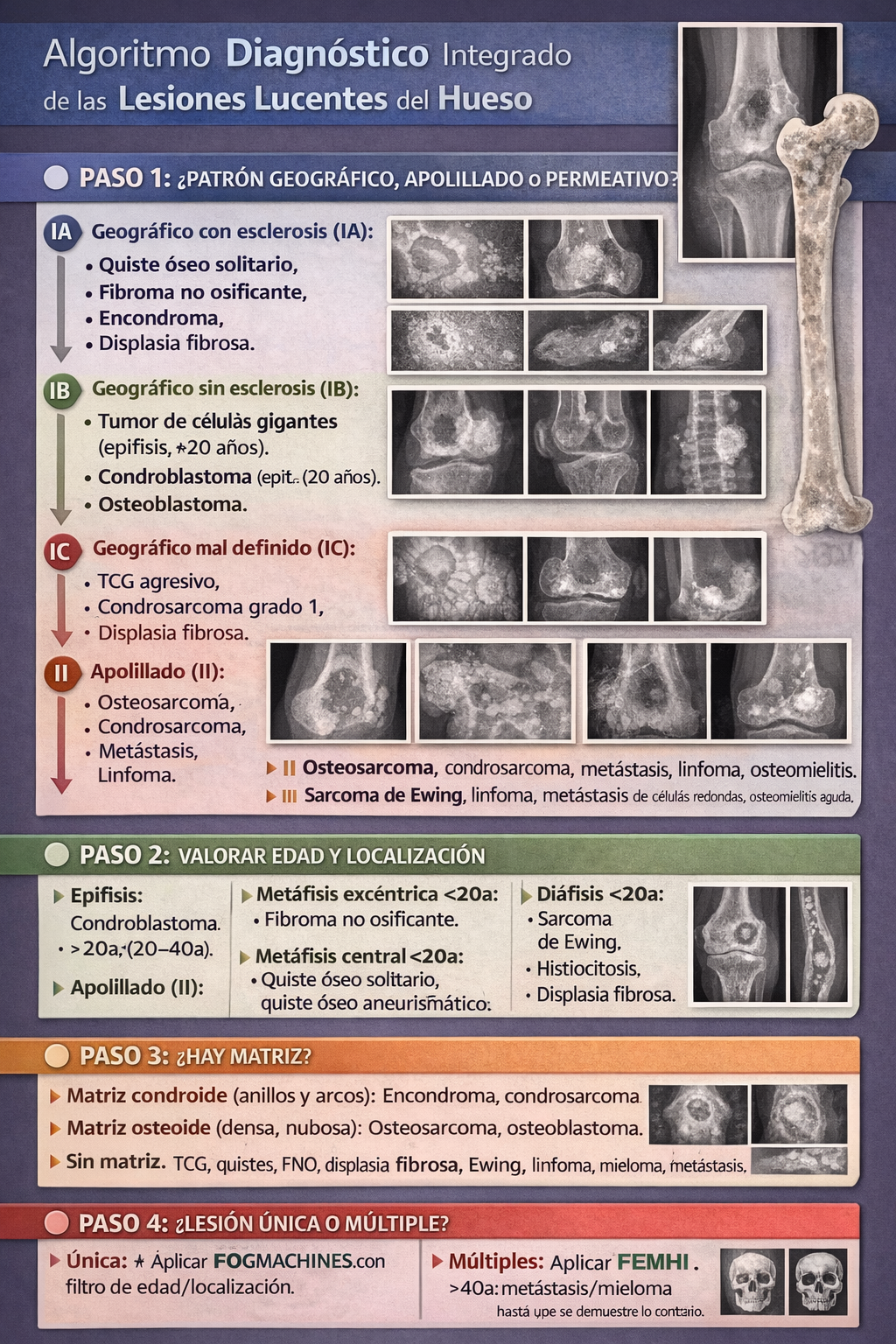
Aserciones útiles en la práctica diaria
- Con una lesión larga en un hueso largo, piense en displasia fibrosa.
- El quiste óseo solitario, el encondroma y la displasia fibrosa pueden ser radiológicamente indistinguibles. Cuando piense en uno, incluya los otros dos.
- Los tumores de células gigantes casi siempre ocurren cerca de una superficie articular. Si una lesión lítica epifisaria no toca el cartílago articular, probablemente no es un TCG.
- Las lesiones líticas del esternón deben considerarse malignas hasta que se demuestre lo contrario. Condrosarcoma, metástasis, linfoma.
- Las descripciones clásicas de los tumores óseos se aplican a lesiones no tratadas. La cirugía, quimioterapia, radioterapia o crioterapia modifican drásticamente la apariencia radiológica. Siempre pregunte por tratamientos previos.
- La RM y la TC son herramientas maravillosas para la estadificación, pero inespecíficas para el diagnóstico histológico. La radiografía simple sigue siendo la prueba más rentable para el diagnóstico diferencial.
- No biopsiar sin un estudio de imagen completo (RM). Una biopsia mal planificada puede comprometer la cirugía preservadora de la extremidad.
- Todo paciente con una lesión lítica agresiva debe ser derivado a un centro de referencia de sarcomas antes de la biopsia.
Resumen práctico
Indicaciones
- Radiografía simple en dos proyecciones: imprescindible, es la prueba más rentable para el diagnóstico diferencial.
- RM con protocolo oncológico (T1, T2/STIR, T1 con contraste, DWI): estadificación local, extensión intraósea y de partes blandas.
- TC torácico: obligatorio en lesiones agresivas y sospecha de sarcoma (metástasis pulmonares).
- TC de la lesión: valoración de matriz tumoral calcificada, erosión cortical, planificación quirúrgica.
- Laboratorio: hemograma, VSG, PCR, FA, LDH, calcio, fósforo, proteinograma (si >40 años), PSA (varones >40 años), CA 15.3 (mujeres con sospecha de metástasis).
- Biopsia percutánea con aguja gruesa (core needle) guiada por imagen, realizada por el equipo que realizará la resección definitiva.
Técnica
- Radiografía: técnica de alta sensibilidad para patrón de destrucción, matriz y reacción perióstica.
- RM: secuencias T1, T2/STIR, T1 con contraste, DWI. Campo de visión amplio incluyendo todo el compartimento anatómico.
- TC: cortes finos (1-2 mm), reconstrucción multiplanar. Útil para detectar matriz condroide/osteoide y nidus (osteoma osteoide).
- Biopsia: aguja 14-16G, 3-5 pases, trayecto excindible, marcaje con clip. Evitar áreas necróticas.
Riesgos y complicaciones
- Asumir que una lesión lítica en paciente >40 años es benigna sin descartar metástasis o mieloma.
- Confundir un tumor de células gigantes (epífisis) con un osteosarcoma (metáfisis).
- Realizar biopsia antes del estudio de imagen completo (especialmente RM).
- Biopsia por equipo no especializado, con trayecto no excindible o incisión transversa.
- No derivar a centro de referencia antes de la biopsia en lesiones de alto riesgo.
Qué esperar del resultado
- Fibroma no osificante: involuciona espontáneamente, no requiere tratamiento.
- Quiste óseo solitario: curación tras fractura o tratamiento percutáneo (80%).
- Tumor de células gigantes: control local con legrado + adyuvantes (80-90%), riesgo de metástasis pulmonares (1-3%).
- Osteosarcoma: supervivencia global a 5 años 70-80% (centros de referencia).
- Sarcoma de Ewing: supervivencia global a 5 años 70-80% (localizado), 30% (metastásico).
- Condrosarcoma grado 1: supervivencia >90% (metástasis excepcionales).
Resumen para la práctica clínica
📌 Indicaciones
- ✓ Radiografía simple en dos proyecciones: imprescindible, es la prueba más rentable para el diagnóstico diferencial.
- ✓ RM con protocolo oncológico (T1, T2/STIR, T1 con contraste, DWI): estadificación local, extensión intraósea y de partes blandas.
- ✓ TC torácico: obligatorio en lesiones agresivas y sospecha de sarcoma (metástasis pulmonares).
- ✓ TC de la lesión: valoración de matriz tumoral calcificada, erosión cortical, planificación quirúrgica.
- ✓ Laboratorio: hemograma, VSG, PCR, FA, LDH, calcio, fósforo, proteinograma (si >40 años), PSA (varones >40 años), CA 15.3 (mujeres con sospecha de metástasis).
- ✓ Biopsia percutánea con aguja gruesa (core needle) guiada por imagen, realizada por el equipo que realizará la resección definitiva.
🔧 Técnica
- 🔧 Radiografía: técnica de alta sensibilidad para patrón de destrucción, matriz y reacción perióstica.
- 🔧 RM: secuencias T1, T2/STIR, T1 con contraste, DWI. Campo de visión amplio incluyendo todo el compartimento anatómico.
- 🔧 TC: cortes finos (1-2 mm), reconstrucción multiplanar. Útil para detectar matriz condroide/osteoide y nidus (osteoma osteoide).
- 🔧 Biopsia: aguja 14-16G, 3-5 pases, trayecto excindible, marcaje con clip. Evitar áreas necróticas.
⚠️ Riesgos
- ⚠️ Asumir que una lesión lítica en paciente >40 años es benigna sin descartar metástasis o mieloma.
- ⚠️ Confundir un tumor de células gigantes (epífisis) con un osteosarcoma (metáfisis).
- ⚠️ Realizar biopsia antes del estudio de imagen completo (especialmente RM).
- ⚠️ Biopsia por equipo no especializado, con trayecto no excindible o incisión transversa.
- ⚠️ No derivar a centro de referencia antes de la biopsia en lesiones de alto riesgo.
✅ Resultados
- ✅ Fibroma no osificante: involuciona espontáneamente, no requiere tratamiento.
- ✅ Quiste óseo solitario: curación tras fractura o tratamiento percutáneo (80%).
- ✅ Tumor de células gigantes: control local con legrado + adyuvantes (80-90%), riesgo de metástasis pulmonares (1-3%).
- ✅ Osteosarcoma: supervivencia global a 5 años 70-80% (centros de referencia).
- ✅ Sarcoma de Ewing: supervivencia global a 5 años 70-80% (localizado), 30% (metastásico).
- ✅ Condrosarcoma grado 1: supervivencia >90% (metástasis excepcionales).
Bibliografía
Clásicos y sistemas de gradación
- Lodwick GS, Wilson AJ, Farrell C, et al. Determining growth rates of focal lesions of bone from radiographs. Radiology. 1980;134(3):577-583. doi:10.1148/radiology.134.3.6928321 (Sistema de Lodwick, aún vigente).
- Madewell JE, Ragsdale BD, Sweet DE. Radiologic and pathologic analysis of solitary bone lesions. Part I: internal margins. Radiol Clin North Am. 1981;19(4):715-748. PMID: 6976024
- Edeiken J, Hodes PJ. Roentgen diagnosis of diseases of bone. 3rd ed. Williams & Wilkins; 1983. (Clásico, base de la correlación edad-tumor).
Clasificación OMS y guías actuales
- WHO Classification of Tumours Editorial Board. WHO Classification of Tumours of Soft Tissue and Bone. 5th ed. Lyon: IARC Press; 2020.
- Strauss SJ, Frezza AM, Abecassis N, et al. Bone sarcomas: ESMO-EURACAN-GENTURIS Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2024;35(8):678-695. doi:10.1016/j.annonc.2024.03.008
- Meyer J, Blue M, Bui N, et al. NCCN Guidelines Version 1.2026: Bone Cancer. J Natl Compr Canc Netw. 2026;24(3):289-306.
Diagnóstico por imagen
- Davies AM, Sundaram M, James SL. Imaging of Bone Tumors and Tumor-Like Lesions. 3rd ed. Springer; 2025.
- Miller TT. Bone tumors and tumor-like conditions: analysis with conventional radiography. Radiology. 2024;310(3):e232156. doi:10.1148/radiol.232156
- Kwee RM, Kwee TC. Radiomics in bone tumors: a systematic review and meta-analysis. Eur Radiol. 2026;36(2):456-470. doi:10.1007/s00330-025-11234-5
- Theodorou DJ, Theodorou SJ, Kakitsubata Y. Sclerotic versus lytic bone lesions: a systematic approach to differential diagnosis. AJR Am J Roentgenol. 2025;224(4):789-802. doi:10.2214/AJR.24.31245
Entidades específicas
- Chakarun CJ, Forrester DM, Gottsegen CJ, et al. Giant cell tumor of bone: review, mimics, and new developments in treatment. Radiographics. 2023;43(2):e220098. doi:10.1148/rg.220098
- Murphey MD, Carroll JF, Flemming DJ, et al. Benign bone tumors and tumor-like lesions. Radiol Clin North Am. 2025;63(1):45-68. doi:10.1016/j.rcl.2024.09.005
- Zheng K, Yu X, Xu M, et al. Chondroblastoma: clinical characteristics, radiological features, and treatment outcomes. Bone Joint J. 2026;108-B(2):234-242. doi:10.1302/0301-620X.108B2.BJJ-2025-0892.R1