Lesiones seudotumorales del tejido blando: procesos reactivos que simulan sarcomas
Las lesiones “tumor-like” del tejido blando, en particular la fascitis nodular y la fascitis proliferativa, son proliferaciones benignas de fibroblastos/miofibroblastos que pueden crecer en semanas y mostrar histología hipercelular con mitosis, lo que genera un reto diagnóstico y el riesgo de sobretratamiento. La actualización 2026 refuerza un enfoque práctico: correlación clínica + imagen + anatomía patológica, usando inmunohistoquímica y, cuando aporta valor, pruebas moleculares (p. ej., reordenamientos de USP6 en fascitis nodular).
En 1 minuto
- Qué son: fascitis nodular y proliferativa son proliferaciones benignas (reactivas / autolimitadas) de fibroblastos/miofibroblastos.
- Por qué confunden: pueden crecer rápido, ser hipercelulares y tener mitosis (sin atipia marcada).
- Claves prácticas: tamaño pequeño (a menudo 1–3 cm), evolución corta (semanas), localización superficial/subcutánea y correlación con imagen.
- Apoyo patológico: SMA+ suele apoyar diferenciación miofibroblástica; reordenamientos USP6 pueden apoyar fascitis nodular en casos seleccionados.
- Manejo: escisión marginal/biopsia-exéresis si es accesible; si hay sospecha real de sarcoma, seguir circuito de sarcomas.
Conceptos generales
- Crecimiento rápido: semanas (esto es típico y orienta).
- Histología “alarmante” pero benigna: hipercelularidad y mitosis sin mitosis atípicas/necrosis extensa típicas de alto grado.
- Objetivo: evitar sobretratamiento (resecciones amplias, radioterapia) cuando una escisión marginal es curativa.
Fascitis nodular
2.1 Definición y epidemiología
Proliferación benigna de fibroblastos/miofibroblastos, rápida, que puede simular sarcoma. Frecuente en adultos jóvenes, aunque puede aparecer a cualquier edad.
- Edad: típica 20–40 años.
- Localización: subcutáneo/fascial, frecuente en antebrazo; también tronco y extremidad inferior.
- Clínica: nódulo de crecimiento rápido (días/semanas), a veces doloroso.
2.2 Imagen
- Ecografía: masa hipoecoica, a veces vascularizada.
- RM: señal variable; suele realzar; puede verse “signo de la fascia” (extensión lineal adyacente).
- La imagen no es patognomónica: sirve para evaluar profundidad, tamaño y relación anatómica.
2.3 Histopatología / IHQ / genética
- Microscopía: células fusiformes en fascículos cortos, estroma mixoide, extravasación de hematíes; mitosis posibles pero no atípicas.
- IHQ orientativa: SMA+ frecuente; desmina−, S100−, CD34− (en general; interpretar según patrón y contexto).
- Molecular (apoyo selectivo): reordenamientos de USP6 (p. ej., MYH9::USP6) descritos en fascitis nodular y pueden ayudar en casos difíciles.
Fascitis proliferativa
3.1 Definición y epidemiología
Lesión benigna relacionada con el espectro de fascitis, con células “ganglion-like” basófilas prominentes, que puede confundirse con sarcoma pleomórfico.
- Edad: más frecuente 40–70 años.
- Localización: antebrazo, muslo, tronco.
- Clínica: nódulo subcutáneo, crecimiento rápido, a veces doloroso.
3.2 Imagen / histología
- Imagen: inespecífica; RM puede ser heterogénea.
- Histología: estroma mixoide + fibroblastos fusiformes y células grandes basófilas (ganglion-like); mitosis ocasionales.
- IHQ: SMA puede ser positiva en el componente fusiforme; marcadores de línea muscular/neuronal típicamente negativos (interpretación caso a caso).
Diagnóstico diferencial
Diferencial clave con sarcomas y con lesiones benignas frecuentes:
Con sarcomas
- UPS (sarcoma pleomórfico indiferenciado): pleomorfismo marcado, necrosis, mitosis atípicas; suele ser más grande y profundo.
- Fibrosarcoma / otros sarcomas fibroblásticos: infiltración, patrón más “monótono” y persistente, evolución menos “explosiva”.
Con benignas
- Fibromatosis desmoide: más infiltrativa, fascículos largos, curso más persistente (si tienes: ver desmoide).
- Mixoma: hipocelular, mixoide, mitosis raras.
- Miositis osificante: patrón zonal/“cáscara de huevo” (si tienes: ver miositis osificante).
Claves prácticas
- Evolución: semanas + pequeño/superficial → orienta a fascitis.
- Atipia/necrosis/mitosis atípicas: si aparecen, subir el nivel de alerta.
- Correlación clínico-patológica: imprescindible; en duda, segunda opinión experta.
Manejo
- Lesión pequeña y accesible: escisión marginal/biopsia-exéresis suele ser curativa.
- Si hay duda razonable de sarcoma: no hacer resección “a ciegas”. Recomendar circuito de sarcomas (imagen adecuada + biopsia planificada + comité).
- Recidiva: rara; suele relacionarse con resección incompleta.
Algoritmo de manejo
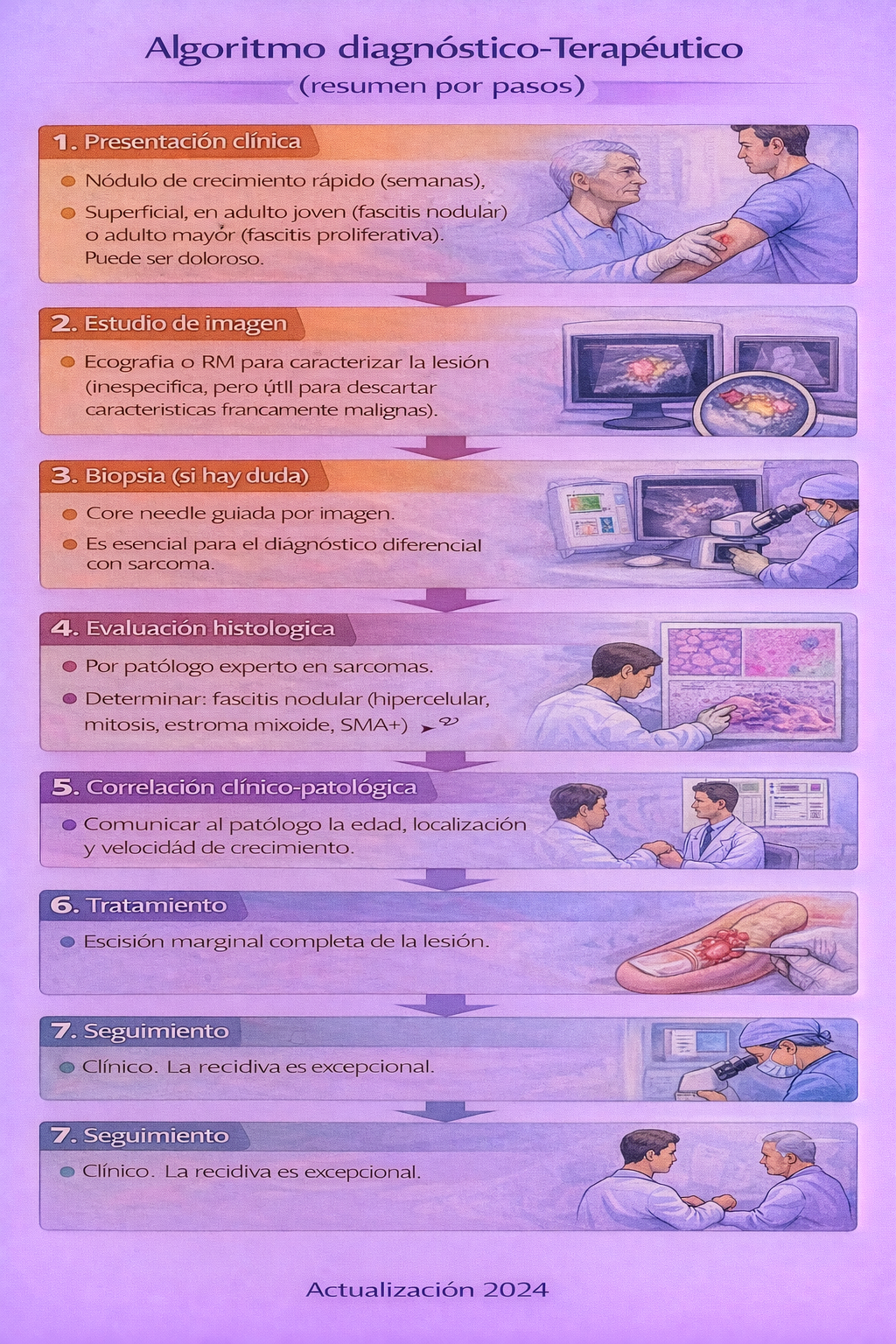
📌 Resumen para la práctica clínica
Indicaciones
- ✓ Lesión pequeña y superficial con crecimiento rápido compatible con fascitis: escisión marginal/biopsia-exéresis.
- ✓ Biopsia core planificada si hay duda diagnóstica o si la lesión es profunda/grande.
- ✓ Segunda opinión de patología de sarcomas si el diagnóstico no cuadra con la clínica.
Técnica
- 🔧 Escisión marginal completa evitando fragmentación.
- 🔧 Informe anatomopatológico con correlación clínica; IHQ selectiva.
- 🔧 Seguimiento clínico.
Riesgos
- ⚠️ Sobretratamiento si se confunde con sarcoma.
- ⚠️ Recidiva rara, habitualmente por resección incompleta.
Resultados
- ✅ Curación en la gran mayoría; pronóstico excelente.
Bibliografía
Soft Tissue and Bone Tumours. 5th ed. IARC; 2020.
Proliferative fasciitis. Cancer. 1975;36(4):1450-1458.
Nodular fasciitis: analysis of 250 patients. Pathology. 1984;16(2):161-166.
Nodular fasciitis: MYH9–USP6 gene fusion. Lab Invest. 2011;91(10):1427-1433.
