Osteosarcoma Extraesquelético — Actualización 2026: una entidad clínica y terapéuticamente distinta del osteosarcoma óseo
El osteosarcoma extraesquelético (EOO, por sus siglas en inglés) es un sarcoma de partes blandas extremadamente raro, que representa menos del 1-2% de todos los sarcomas de tejidos blandos y aproximadamente el 4% de todos los osteosarcomas. Se define por la producción de matriz osteoide por células tumorales malignas, sin conexión con el esqueleto subyacente. Afecta predominantemente a adultos mayores (mediana de edad 50-60 años), con localización preferente en extremidades inferiores y retroperitoneo. La Actualización 2026 enfatiza su consideración como una entidad clínica y terapéuticamente distinta del osteosarcoma óseo: a diferencia de este último, el osteosarcoma extraesquelético responde mal a los regímenes de quimioterapia basados en antraciclinas (tasa de respuesta <20%) y su tratamiento debe seguir las pautas de los sarcomas de partes blandas de alto grado, con cirugía como pilar fundamental y papel limitado de la quimioterapia. El pronóstico es adverso, con supervivencia a 5 años del 40-50% incluso en enfermedad localizada, debido a la alta tasa de metástasis (principalmente pulmonares) y recidiva local.
En 1 minuto
Sarcoma de partes blandas de alto grado, productor de matriz osteoide, sin conexión con el hueso. <1-2% de sarcomas de partes blandas.
Masa de crecimiento lento en tejidos profundos, indolora inicialmente. Localización: extremidades inferiores, retroperitoneo. Edad media 50-60 años.
Masa con calcificaciones amorfas, desorganizadas, centrales. RM: heterogénea, con áreas de baja señal (calcificaciones). Demostrar ausencia de conexión ósea es crucial.
Miositis osificante (osificación periférica), sarcoma sinovial, condrosarcoma extraesquelético, osteosarcoma yuxtacortical.
Cirugía R0 (pilar). RT (neo)adyuvante en casos seleccionados. QT con antraciclinas tiene baja respuesta (<20%); reservada para metastásico.
Pitfall: El error más grave es confundir el osteosarcoma extraesquelético con miositis osificante o con un osteosarcoma yuxtacortical (parosteal/periosteal). Una biopsia mal dirigida o una interpretación radiológica incorrecta pueden llevar a un tratamiento inadecuado. Es obligatorio demostrar la ausencia de conexión con el hueso mediante imagen (RM/TC) y realizar una biopsia que incluya la zona de osificación activa (evitando áreas necróticas o puramente calcificadas). Además, no debe tratarse con protocolos de osteosarcoma óseo (quimioterapia neoadyuvante intensiva), pues la respuesta es pobre y se retrasa la cirugía curativa.
Conceptos
1.1 Definición y criterios diagnósticos
💡 El osteosarcoma extraesquelético se define como un sarcoma de partes blandas productor de matriz osteoide (hueso inmaduro) por parte de células tumorales malignas, que no presenta conexión con el esqueleto (ni con hueso ni con periostio). Los criterios diagnósticos originales de Allan y Soule (1971) siguen vigentes:
- ✅ Presencia de una masa de tejidos blandos sin unión al hueso o al periostio.
- ✅ Producción de matriz osteoide por células tumorales malignas (puede haber componente condroblástico o fibroblástico, pero la osteogénesis sarcomatosa debe ser identificable).
- ✅ Exclusión de otras neoplasias productoras de osteoide (como el osteosarcoma óseo con extensión a partes blandas).
La clasificación de la OMS de 2020 lo incluye dentro de los sarcomas de partes blandas con diferenciación osteogénica.
1.2 Epidemiología: un tumor de adultos mayores
- 📈 Incidencia: Extremadamente baja. Representa 1-2% de todos los sarcomas de partes blandas y aproximadamente el 4% de todos los osteosarcomas.
- 📈 Edad: Pico de incidencia en la 5ª-6ª década de la vida (media 54 años). Excepcional en niños y adolescentes.
- 📈 Sexo: Ligero predominio masculino (1,2:1) en la mayoría de las series.
- 📈 Localización: Predominio en extremidades inferiores (muslo, región glútea, pierna) y retroperitoneo. También se han descrito casos en mama, pulmón, tiroides, riñón, vejiga, próstata y mediastino, aunque son excepcionales.
- 📈 Factores de riesgo: La mayoría son idiopáticos. Se han descrito casos post-radioterapia (osteosarcoma radioinducido extraesquelético) con latencia de 10-20 años.
1.3 Puntos prácticos (Actualización 2026)
- ⚠️ Entidad distinta del osteosarcoma óseo: Esta es la premisa más importante. A diferencia del osteosarcoma esquelético, el EOO no responde bien a la quimioterapia neoadyuvante basada en MAP (metotrexato, doxorrubicina, cisplatino). La tasa de respuesta objetiva es <20% y la respuesta patológica completa es excepcional (<5%). Por tanto, el tratamiento debe seguir las guías de sarcomas de partes blandas, no las de sarcomas óseos.
- ⚠️ Papel de la radioterapia: Dado el alto riesgo de recidiva local, la radioterapia (neo)adyuvante debe considerarse en tumores profundos, >5 cm, de localización anatómica desfavorable (retroperitoneo, cabeza y cuello) o con márgenes quirúrgicos comprometidos.
- ⚠️ Genética molecular: El EOO muestra cariotipos complejos, con alteraciones en TP53, RB1 y amplificaciones de MDM2 (en algunos casos). No presenta las translocaciones características de otros sarcomas de partes blandas. La presencia de amplificación de MDM2 puede ayudar en el diagnóstico diferencial con el osteosarcoma parosteal (que también la presenta), pero la clave es la localización.
- ⚠️ Centralización obligada: Al igual que otros sarcomas, el manejo debe centralizarse en unidades de referencia con experiencia en sarcomas de partes blandas y óseos, con discusión multidisciplinar pretratamiento.
Clínica
La presentación clínica del osteosarcoma extraesquelético es inespecífica y similar a la de otros sarcomas de partes blandas profundos.
| Síntoma/Signo | Frecuencia | Comentario clínico |
|---|---|---|
| Masa palpable | >90% | Crecimiento lento y progresivo durante meses. Consistencia firme, a veces pétrea si muy calcificada. Profunda (fascial o muscular). |
| Dolor local | 30-50% | Suele aparecer tardíamente por compresión de estructuras vecinas. Menos frecuente que en el osteosarcoma óseo. |
| Síntomas compresivos | Variable | En localizaciones retroperitoneales: dolor abdominal, sensación de plenitud, hidronefrosis, edema en miembros inferiores. |
| Limitación funcional | 20-30% | En extremidades, por efecto masa o afectación neuromuscular. |
Imagen
La imagen es fundamental para la sospecha diagnóstica y para demostrar la ausencia de conexión con el hueso.
3.1 Radiografía simple
- 💡 Masa de partes blandas con calcificaciones u osificaciones amorfas, irregulares y desorganizadas, localizadas predominantemente en el centro de la lesión.
- 💡 Patrón en "nubes" o "algodonoso", similar a la matriz osteoide del osteosarcoma óseo.
- 💡 No hay unión a la cortical ósea adyacente (puede haber erosión por compresión, pero no infiltración directa).
- 💡 Puede ser visible una pseudocápsula radiolúcida que separa la masa del hueso.
3.2 Tomografía computarizada (TC)
- 💡 Masa de densidad heterogénea, con áreas de alta atenuación correspondientes a la matriz osteoide calcificada.
- 💡 Demuestra con precisión la falta de continuidad con el esqueleto, criterio esencial para el diagnóstico.
- 💡 Puede mostrar áreas de necrosis hipodensas y realce periférico tras contraste.
- 💡 Útil para planificación quirúrgica y para detectar metástasis (TC torácico obligatorio).
3.3 Resonancia magnética (RM)
- 💡 T1: Señal predominantemente baja a intermedia (similar al músculo). Las áreas de calcificación/ osificación son hipointensas.
- 💡 T2: Señal heterogénea, predominantemente alta (tejido tumoral viable) con áreas de baja señal (calcificaciones).
- 💡 Tras contraste: Realce heterogéneo, con áreas de necrosis que no realzan.
- 💡 Demostración de pseudocápsula: Anillo periférico hipointenso que no constituye una barrera real (infiltración microscópica presente).
- 💡 Relación con estructuras vecinas: Fundamental para planificar la cirugía (paquete vasculonervioso, compartimentos).
3.4 PET-TC
- 💡 El EOO es típicamente FDG-ávido (SUVmax elevado). Puede ser útil para detectar metástasis ocultas o valorar respuesta a tratamiento, aunque no es rutinario.
Hallazgo radiológico característico
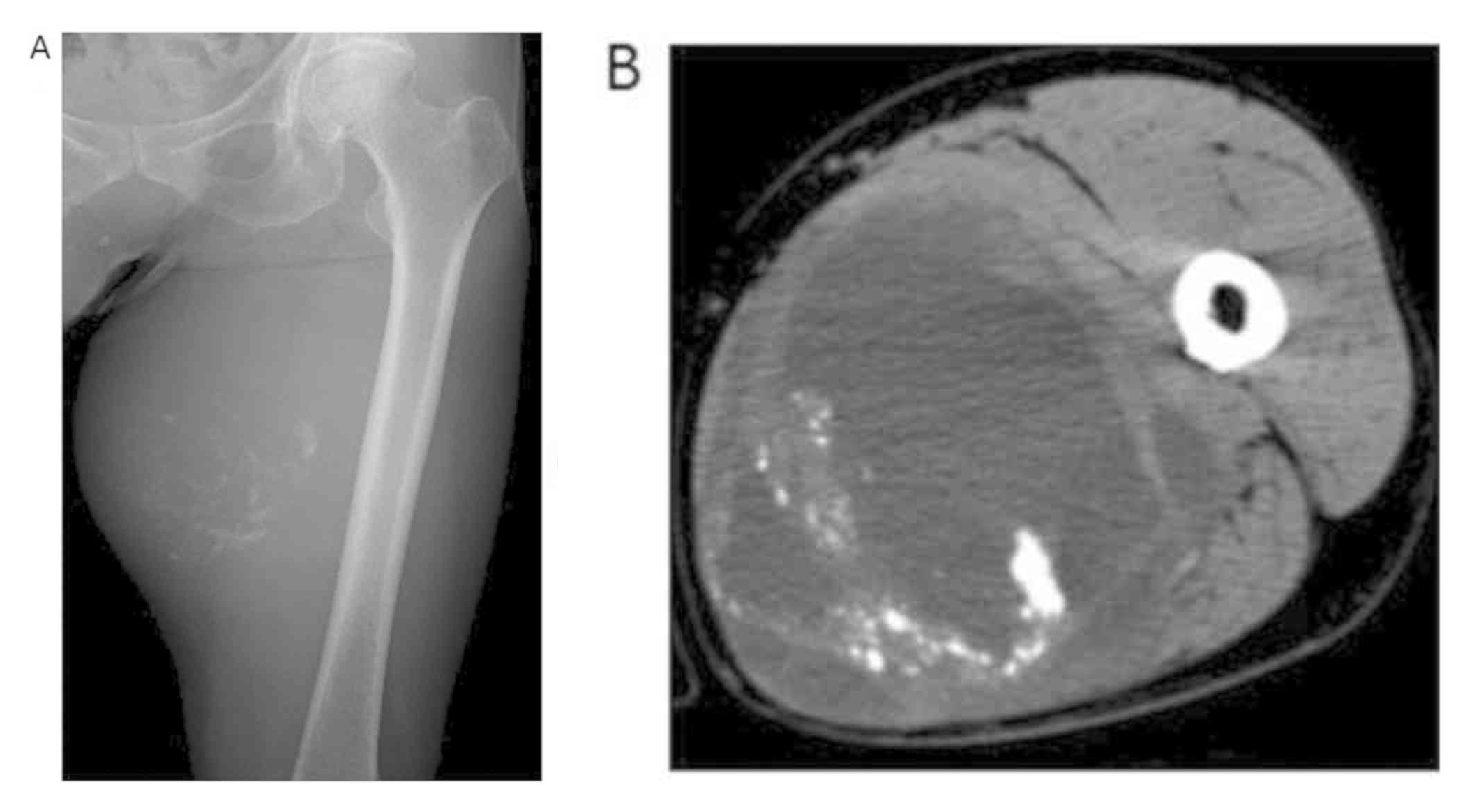
3.5 Estadificación metastásica
- ⚠️ TC torácico: OBLIGATORIO. El pulmón es el sitio predominante de metástasis (70-80%). Hasta el 15-20% de los pacientes tienen metástasis sincrónicas detectables.
- ⚠️ TC abdominopélvico: Indicado en localizaciones retroperitoneales o pélvicas.
Diagnóstico y diagnóstico diferencial
Confirmación diagnóstica: Requiere biopsia con aguja gruesa (core needle) guiada por imagen, preferiblemente realizada en centro de referencia. La biopsia debe dirigirse a las áreas sólidas y viables (evitando necrosis y calcificaciones puras) y debe incluir tejido tumoral suficiente para demostrar la producción de osteoide.
- 🔬 Histología (HE): Idéntica a la del osteosarcoma óseo convencional. Proliferación de células fusiformes y pleomórficas con producción directa de matriz osteoide (eosinófila, densa, amorfa). Puede haber áreas condroblásticas, fibroblásticas o de células gigantes. Alto grado citológico, mitosis atípicas, necrosis.
- 🧪 Inmunohistoquímica: No hay marcador específico. SATB2 (sensible pero no específico) puede ser positivo. La IHC es útil para el diagnóstico diferencial (ver más abajo).
- 🧬 Genética molecular: Cariotipo complejo, sin alteraciones específicas. Amplificación de MDM2 en algunos casos (similar al osteosarcoma parosteal, con el que hay que hacer diferencial).
Diagnóstico diferencial (entidades a excluir sistemáticamente):
Radiológico:
- 🔹 Miositis osificante: Clave: osificación periférica (zona), patrón en "concha de huevo" o laminar. Historia de trauma en 50%. La lesión madura con el tiempo. En fases tempranas puede confundirse, pero nunca produce osteoide tumoral.
- 🔹 Sarcoma sinovial: Calcificaciones en 25% (puntiformes o amorfas), pero rara osificación. Localización preferente cerca de articulaciones (tobillo, rodilla). Pacientes más jóvenes. IHQ: TLE1+, citoqueratinas+ focales, EMA+, SS18-SSX (translocación).
- 🔹 Condrosarcoma extraesquelético: Calcificaciones en anillos o arcos (típicas de cartílago). Nunca produce hueso. IHQ: S100+, SOX9+.
- 🔹 Liposarcoma con osificación: Se identifica tejido adiposo en imagen (TC/RM) y en histología. La osificación suele ser más organizada. Amplificación MDM2 en liposarcoma bien diferenciado/desdiferenciado.
- 🔹 Tumor óseo pseudomaligno de tejidos blandos (seudomalignant osseous tumor): Raro, probablemente reactivo. Histología benigna.
- 🔹 Osteosarcoma yuxtacortical (parosteal, periosteal): Están adosados al hueso, con base de implantación en la cortical. El parosteal suele ser de bajo grado. Demostrar la falta de unión al hueso es crucial.
- 🔹 Calcinosis tumoral: Masas calcificadas lobuladas, a menudo periarticulares, sin matriz osteoide. Asociada a hiperfosfatemia.
Patológico:
- 🔹 Condrosarcoma extraesquelético: Matriz condroide, no osteoide.
- 🔹 Miositis osificante: Patrón zonal (maduración centrípeta), ausencia de atipia citológica.
- 🔹 Osteosarcoma parosteal/periosteal: Si la muestra es pequeña y no se puede evaluar la relación con el hueso, puede ser indistinguible. Requiere correlación radiológica.
- 🔹 Tumor fibroso solitario / Hemangiopericitoma: Puede tener hueso metaplásico (periférico, maduro), no osteoide tumoral. STAT6+, CD34+.
Tratamiento
Premisa fundamental: El osteosarcoma extraesquelético debe tratarse siguiendo las guías de los sarcomas de partes blandas de alto grado, no las del osteosarcoma óseo.
5.1 Cirugía
- 💡 Resección amplia (R0): Estándar de tratamiento. Requiere margen de tejido sano de al menos 1-2 cm en plano radial y profundo, o fascia intacta como barrera. La resección intralesional o marginal se asocia a tasas de recidiva local >50%.
- 💡 Cirugía preservadora de extremidad: Posible en la mayoría de los casos de extremidades, gracias a la combinación con RT. La amputación queda reservada para casos con infiltración neurovascular masiva.
- 💡 Biopsia previa: Debe ser realizada por el mismo equipo quirúrgico que hará la resección definitiva, con trayecto excindible.
5.2 Radioterapia (RT)
- 💡 Indicaciones: Tumores profundos, >5 cm, alto grado, márgenes positivos o cercanos, localización anatómica desfavorable (retroperitoneo, cabeza y cuello).
- 💡 Neoadyuvante: Preferible en tumores grandes y borderline resecables. Dosis: 50 Gy. Reduce el volumen tumoral y facilita márgenes negativos.
- 💡 Adyuvante: Indicada cuando no se administró RT preoperatoria y hay factores de riesgo. Dosis: 60-66 Gy sobre lecho quirúrgico. Reduce tasa de recidiva local.
5.3 Quimioterapia (QT)
- 💡 Evidencia actual: La QT basada en antraciclinas (doxorrubicina) tiene una baja tasa de respuesta en EOO. El estudio de Ahmad et al. (2002) mostró una tasa de respuesta global del 19% (2 respuestas completas, 3 parciales en 27 pacientes), con solo una respuesta patológica completa (6%) en 18 pacientes tratados con QT que luego fueron intervenidos.
- 💡 Neoadyuvante/adyuvante: No hay evidencia de beneficio en supervivencia. No se recomienda de forma rutinaria. Puede considerarse en casos seleccionados de muy alto riesgo (tumores >10 cm, irresecables, metastásicos) tras discusión multidisciplinar, pero con expectativas realistas de respuesta baja.
- 💡 Enfermedad metastásica: Primera línea: doxorrubicina sola o en combinación (ifosfamida). Segunda línea: opciones limitadas (pazopanib, gemcitabina + docetaxel, trabectedina), con eficacia modesta.
| Opción | Indicación principal | Comentario / Nivel de evidencia |
|---|---|---|
| Cirugía R0 | Todo EOO localizado resecable | Estándar absoluto. La supervivencia a 5 años es del 50-60% si márgenes negativos; cae drásticamente si márgenes positivos. Nivel IA. |
| RT (neo)adyuvante | Tumores >5 cm, profundos, localización compleja, márgenes + | Mejora control local. Evidencia extrapolada de sarcomas de partes blandas. Nivel IIA. |
| QT (doxorrubicina ± ifosfamida) | 1ª línea metastásico; casos seleccionados de alto riesgo | Baja tasa de respuesta (19%). No recomendada de forma rutinaria en adyuvancia. Nivel IIB (estudios retrospectivos, series pequeñas). |
| Pazopanib | 2ª línea metastásico (fracaso a antraciclinas) | Aprobado en sarcomas de partes blandas, pero eficacia limitada en EOO. Nivel IIB. |
Pronóstico y seguimiento
- 📈 Pronóstico general: El EOO tiene un pronóstico adverso. La supervivencia global a 5 años para enfermedad localizada es del 40-50% en series contemporáneas. Los factores pronósticos independientes son:
- 🔹 Tamaño tumoral: >5 cm se asocia a peor pronóstico.
- 🔹 Profundidad: Profundo vs superficial.
- 🔹 Márgenes quirúrgicos: Resección R0 es esencial.
- 🔹 Localización: Retroperitoneo tiene peor pronóstico que extremidades.
- 📈 Recidiva local: A pesar de tratamiento adecuado, la tasa de recurrencia local a 5 años es del 15-20%, más alta que en otros sarcomas de partes blandas.
- 📈 Metástasis a distancia: Principal causa de muerte. El 30-50% de los pacientes desarrollarán metástasis, predominantemente pulmonares (70-80%).
- 📈 Seguimiento sugerido (similar a sarcomas de partes blandas de alto grado):
- 🔹 Primeros 2-3 años: RM/TC de la región primaria cada 3-4 meses. TC torácico cada 3-6 meses. Exploración física dirigida.
- 🔹 Hasta 5 años: Cada 6 meses con imagen local y TC torácico.
- 🔹 Hasta 10 años: Anual.
Algoritmo diagnóstico-terapéutico
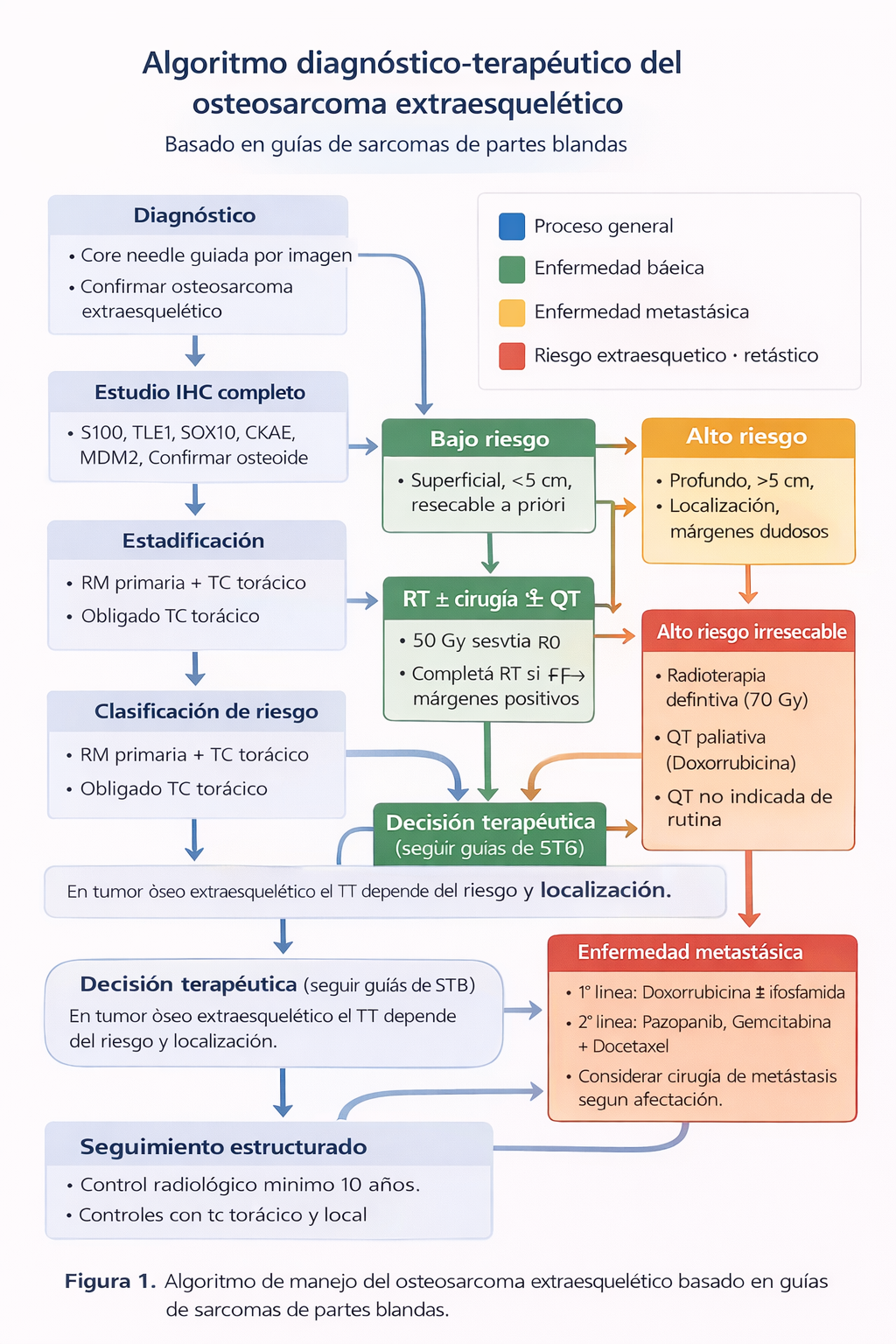
Resumen para la práctica clínica
📌 Indicaciones
- ✅ Resección quirúrgica amplia con márgenes negativos (R0) en todo EOO localizado.
- ✅ Radioterapia (neo)adyuvante en tumores de alto riesgo: profundos, >5 cm, márgenes comprometidos o localización anatómica desfavorable.
- ✅ Quimioterapia con antraciclinas en primera línea de enfermedad metastásica o irresecable (con expectativas de respuesta bajas).
🔧 Técnica
- 🔧 Cirugía: resección En bloc con margen de 1-2 cm o fascia intacta. Planificación conjunta con radioterapia.
- 🔧 Radioterapia: IMRT o protonterapia según localización. Neoadyuvante: 50 Gy; adyuvante: 60-66 Gy.
- 🔧 Biopsia: siempre por equipo quirúrgico que realizará la resección definitiva, con trayecto excindible.
⚠️ Riesgos
- ⚠️ Recidiva local (15-20% a 5 años con tratamiento óptimo).
- ⚠️ Metástasis a distancia, especialmente pulmonares (30-50% de los pacientes).
- ⚠️ Confusión diagnóstica con miositis osificante u osteosarcoma yuxtacortical.
- ⚠️ Mala respuesta a quimioterapia (tasa de respuesta <20%).
✅ Resultados
- ✅ Supervivencia global a 5 años: 40-50% (enfermedad localizada).
- ✅ Supervivencia libre de recidiva local a 5 años: 80-85% tras cirugía R0 + RT.
- ✅ Supervivencia libre de metástasis a 5 años: 50-60%.
Bibliografía
Referencias clave (actualizadas)
- 📄 Ahmad SA, Patel SR, Ballo MT, et al. Extraosseous osteosarcoma: response to treatment and long-term outcome. J Clin Oncol. 2002;20(2):521-527. doi:10.1200/JCO.2002.20.2.521
- 📄 Allan CJ, Soule EH. Osteogenic sarcoma of the somatic soft tissues. Clinicopathologic study of 26 cases and review of literature. Cancer. 1971;27(5):1121-1133.
- 📄 Chung EB, Enzinger FM. Extraskeletal osteosarcoma. Cancer. 1987;60(5):1132-1142.
- 📄 Lee JS, Fetsch JF, Wasdhal DA, et al. A review of 40 patients with extraskeletal osteosarcoma. Cancer. 1995;76(11):2253-2259.
- 📄 WHO Classification of Tumours Editorial Board. WHO Classification of Tumours of Soft Tissue and Bone. 5th ed. Lyon: IARC Press; 2020.
- 📄 NCCN Clinical Practice Guidelines in Oncology: Soft Tissue Sarcoma, Version 2.2025. (Sección sobre sarcomas de partes blandas, incluye extraskeletal osteosarcoma como subtipo).
- 📄 ESMO Guidelines Committee. Soft tissue and visceral sarcomas: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021;32(11):1348-1365. (Actualización 2024 en prensa).
- 📄 Riedel RF, et al. Systemic therapy for advanced soft tissue sarcoma. Surg Oncol Clin N Am. 2022;31(3):407-421. doi:10.1016/j.soc.2022.03.005
Diagnóstico por imagen y diferencial
- 📄 Mc Auley G, Jagannathan J, O'Regan K, et al. Extraskeletal osteosarcoma: spectrum of imaging findings. AJR Am J Roentgenol. 2012;198(1):W31-W37. doi:10.2214/AJR.11.7241
- 📄 Kransdorf MJ, Meis JM. From the archives of the AFIP. Extraskeletal osseous and cartilaginous tumors of the extremities. Radiographics. 1993;13(4):853-884. doi:10.1148/radiographics.13.4.8346277
Tratamiento y pronóstico
- 📄 Goldstein-Jackson SY, Gosheger G, Delling G, et al. Extraskeletal osteosarcoma: a European Musculoskeletal Oncology Society study on 266 patients. Eur J Cancer. 2005;41(11):1610-1617. doi:10.1016/j.ejca.2005.04.032
- 📄 Longhi A, Bacci G, Ferrari S, et al. Neoadjuvant chemotherapy for patients with extraskeletal osteosarcoma. J Chemother. 2003;15(3):291-295. doi:10.1179/joc.2003.15.3.291
- 📄 Gronchi A, et al. Neoadjuvant chemotherapy in high-risk soft tissue sarcomas: a clinical practice guideline. Eur J Cancer. 2023;181:160-173. (Revisión de consenso).
