Osteosarcoma — Visión General y Principios de Manejo (Actualización 15/02/2026): conceptos fundamentales, clasificación, pronóstico y estrategia terapéutica multimodal
Última revisión: 15/02/2026
El osteosarcoma es la neoplasia ósea primaria maligna más frecuente (excluyendo las neoplasias hematológicas), caracterizada por la producción de matriz osteoide por parte de las células tumorales. Afecta predominantemente a niños, adolescentes y adultos jóvenes, con un segundo pico en mayores de 60 años (asociado a enfermedad de Paget o transformación postradiación). Su comportamiento biológico es agresivo, con alto potencial metastásico, principalmente pulmonar. El manejo actual del osteosarcoma de alto grado se basa en un enfoque multidisciplinar que combina quimioterapia neoadyuvante (régimen MAP: metotrexato a altas dosis, doxorrubicina, cisplatino), cirugía de resección amplia con preservación de extremidad (posible en >85% de los casos) y quimioterapia adyuvante. El factor pronóstico independiente más potente es la respuesta histológica a la quimioterapia preoperatoria (grado de necrosis tumoral). La Actualización 2026 enfatiza la importancia de la centralización del tratamiento en unidades de sarcomas con experiencia, la tipificación molecular (especialmente en variantes de bajo grado, con amplificación de MDM2), el manejo de la enfermedad metastásica (cirugía de las metástasis pulmonares) y la vigilancia a largo plazo de los efectos tardíos del tratamiento (cardiotoxicidad, nefrotoxicidad, ototoxicidad y segundas neoplasias).
En 1 minuto
Tumor óseo primario maligno más frecuente. Produce matriz osteoide. Pico en 2ª década y en >60 años (Paget/radiación).
Dolor persistente, nocturno, tumefacción. Localización: metáfisis de huesos largos (fémur distal > tibia proximal).
Rx: lesión lítica/blástica, bordes mal definidos, rotura cortical, reacción perióstica agresiva (Codman, sol naciente). RM y TC torácico obligatorios.
Biopsia planificada. Confirmación histológica de osteoide. Gradación 1-4 según celularidad, atipia y mitosis.
Enfoque multimodal: QT neoadyuvante MAP → Cirugía R0 (preservación en >85%) → QT adyuvante. Necrosis >90% = mejor pronóstico.
Pitfall: El error más grave es realizar una biopsia inadecuada o mal planificada. Una biopsia contaminante, con trayecto no excindible, o realizada por un equipo no familiarizado con la cirugía reconstructiva, puede comprometer la posibilidad de cirugía preservadora de la extremidad y empeorar el pronóstico. La biopsia debe ser realizada por el mismo equipo quirúrgico que llevará a cabo la resección definitiva, siguiendo los principios de los centros de sarcomas. Otro error es infraestimar el grado tumoral por una muestra no representativa (zonas reactivas periféricas en lugar de tumor viable).
Conceptos
1.1 Definición y clasificación general
💡 El término "osteosarcoma" engloba una familia de tumores del tejido conjuntivo con diferente potencial maligno, unificados por la característica común de que las células neoplásicas producen matriz osteoide o tejido óseo inmaduro. Se han identificado múltiples subtipos, que se clasifican según:
- 🔹 Localización anatómica: axial vs. apendicular.
- 🔹 Localización en el hueso: central (medular), intracortical, yuxtacortical (superficial).
- 🔹 Origen: primario (idiopático, la mayoría) vs. secundario (Paget, post-radiación, sobre infartos óseos, displasia fibrosa).
- 🔹 Grado histológico: bajo grado (1), grado intermedio (2), alto grado (3-4).
- 🔹 Subtipo histológico específico: convencional (osteoblástico, condroblástico, fibroblástico), telangiectásico, de células pequeñas, de bajo grado central, parosteal, periosteal, superficial de alto grado, etc.
El osteosarcoma extraesquelético (de tejidos blandos) es una entidad aparte, con comportamiento y tratamiento diferente.
1.2 Epidemiología
- 📈 Incidencia: Constituye cerca del 20% de todas las neoplasias malignas primarias del hueso. Representa aproximadamente el 0.2% de todas las neoplasias malignas (alrededor de 100 nuevos casos por año en España). Es el 5% de los tumores de la niñez.
- 📈 Edad: Distribución bimodal: pico principal en la 2ª década de la vida (58% de los casos, coincidiendo con el pico de crecimiento puberal). El 50% de los tumores en esta edad se localizan alrededor de la rodilla. Un segundo pico más pequeño se observa en la 6ª década, generalmente secundario a lesiones óseas preexistentes (Paget, displasia fibrosa, osteocondroma, áreas previamente irradiadas).
- 📈 Sexo: Predominio masculino (60% hombres, 40% mujeres).
1.3 Etiología y factores de riesgo
⚠️ La mayoría de los osteosarcomas son idiopáticos (primarios). Los factores de riesgo conocidos para los osteosarcomas secundarios incluyen:
- 🔹 Enfermedad de Paget ósea: Riesgo de transformación sarcomatosa (~1%).
- 🔹 Radiaciones ionizantes: Osteosarcoma post-irradiación (latencia media 10-20 años).
- 🔹 Infartos óseos.
- 🔹 Displasia fibrosa.
- 🔹 Ingestión de sustancias radioactivas.
- 🔹 Síndromes genéticos: Síndrome de Li-Fraumeni (mutación TP53), retinoblastoma hereditario (mutación RB1).
1.4 Puntos prácticos (Actualización 2026)
- ⚠️ Centralización del tratamiento: Los pacientes con sospecha de osteosarcoma deben ser derivados a un centro de referencia en sarcomas antes de la biopsia. Esto asegura una planificación adecuada y mejora los resultados oncológicos y funcionales.
- ⚠️ Respuesta a QT como guía terapéutica: La evaluación de la necrosis tumoral post-neoadyuvancia (>90% vs <90%) es el factor más potente para predecir el pronóstico y, en algunos protocolos, para modificar la quimioterapia adyuvante.
- ⚠️ Manejo de la enfermedad metastásica: La resección quirúrgica completa de las metástasis pulmonares (metastasectomía) es un pilar fundamental para lograr la supervivencia a largo plazo en estos pacientes.
- ⚠️ Vigilancia de efectos tardíos: Los supervivientes de osteosarcoma requieren seguimiento a largo plazo para detectar y manejar la cardiotoxicidad por antraciclinas, la nefrotoxicidad/ototoxicidad por cisplatino y el riesgo de segundas neoplasias.
Clínica
La presentación clínica del osteosarcoma es variable y depende del tipo, localización y extensión del tumor.
| Síntoma/Signo | Frecuencia | Comentario clínico |
|---|---|---|
| Dolor localizado | >90% | Suele ser el síntoma inicial. Al principio puede ser leve e intermitente, pero progresa a constante y severo, a menudo con predominio nocturno. |
| Tumefacción / Masa palpable | 70-80% | Aparece semanas o meses después del inicio del dolor. Consistencia firme, a veces caliente, con circulación colateral. |
| Limitación funcional / Cojera | 40-60% | Secundaria al dolor o al efecto masa, especialmente en tumores de miembros inferiores o cerca de articulaciones. |
| Fractura patológica | 10-15% | Puede ser la primera manifestación. Más frecuente en osteosarcomas líticos (telangiectásico). No empeora el pronóstico si se trata adecuadamente, pero puede dificultar la cirugía preservadora. |
| Síntomas sistémicos | <10% | Fiebre, pérdida de peso, anorexia. Sugieren enfermedad avanzada o metastásica. |
Imagen
La radiografía simple es la base del diagnóstico. La RM y la TC son imprescindibles para la estadificación local y a distancia.
3.1 Radiografía simple
- 💡 Patrón de destrucción ósea: Lítico, blástico (esclerótico) o mixto, con bordes mal definidos y permeativos (agresivo).
- 💡 Matriz tumoral: Mineralización de la matriz osteoide, con aspecto nuboso, algodonoso o denso.
- 💡 Reacción perióstica: Agresiva: laminar, en "capas de cebolla", en "sol naciente" (espículas perpendiculares) o triángulo de Codman (elevación del periostio con hueso reactivo en los bordes).
- 💡 Masa de partes blandas: A menudo visible, puede contener áreas de mineralización.
3.2 Resonancia magnética (RM) - Extensión local (OBLIGATORIA)
- 💡 Extensión intraósea: Determina la longitud de afectación de la médula ósea (fundamental para planificar el nivel de resección).
- 💡 Skip metástasis: Focos tumorales separados del tumor primario por médula sana. Su presencia (5-10% de casos) contraindica la cirugía preservadora convencional.
- 💡 Extensión a partes blandas: Caracteriza la masa, su relación con el paquete vasculonervioso y los compartimentos musculares.
- 💡 Afectación articular y fisisaria.
3.3 Tomografía computarizada (TC)
- 💡 TC torácico: OBLIGATORIO para detectar metástasis pulmonares (10-20% al diagnóstico). Debe realizarse con cortes finos.
- 💡 TC de la lesión primaria: Útil para valorar la integridad cortical y la mineralización de la matriz, especialmente en áreas complejas como pelvis o sacro.
3.4 Gammagrafía ósea y PET-TC
- 💡 Gammagrafía ósea (Tc99): Detecta metástasis óseas a distancia y lesiones skip. Muy sensible.
- 💡 PET-TC: Útil para valorar respuesta a quimioterapia neoadyuvante (disminución del SUVmax se correlaciona con necrosis). No sustituye a la RM para extensión local ni al TC torácico para metástasis pulmonares.
3.5 Estadificación
- ⚠️ El sistema más utilizado es el de Enneking (Musculoskeletal Tumor Society) y el AJCC, que combinan el grado histológico (bajo/alto), la extensión (intracompartimental/extracompartimental) y la presencia de metástasis.
Diagnóstico y gradación histológica
Confirmación diagnóstica: Requiere biopsia (core needle o incisional) planificada por el equipo quirúrgico. La comunicación entre radiólogo, cirujano y patólogo es esencial. La muestra debe ser representativa, evitando zonas de reacción perióstica o necrosis. La biopsia con aguja fina (PAAF) no es adecuada para el diagnóstico inicial.
- 🔬 Histología (HE): Presencia de células fusiformes malignas que producen matriz osteoide de forma directa. Puede haber otros componentes (condroblástico, fibroblástico).
- 📊 Gradación histológica (sistema de Broder, adaptado): Se basa en la celularidad, atipia celular (pleomorfismo) y actividad mitótica. Es de gran importancia clínica, terapéutica y pronóstica.
- 🔹 Grado 1 (bajo grado): Celularidad ligeramente incrementada, atipia mínima/leve, actividad mitótica baja. Ej: osteosarcoma parosteal, central de bajo grado.
- 🔹 Grado 2 (grado intermedio): Celularidad moderada, atipia moderada, mitosis baja/moderada. Ej: osteosarcoma periosteal.
- 🔹 Grado 3 (alto grado): Celularidad aumentada, atipia moderada/pronunciada, mitosis moderada/alta. Matriz osteoide irregular. Ej: osteosarcoma convencional.
- 🔹 Grado 4 (alto grado): Celularidad marcadamente incrementada, marcado pleomorfismo, alta actividad mitótica. Matriz osteoide abundante e irregular. Ej: osteosarcoma telangiectásico, post-Paget, post-irradiación, multifocales.
| Grado | Celularidad | Atipia celular | Actividad mitótica | Matriz osteoide |
|---|---|---|---|---|
| 1 (Bajo) | Ligeramente ↑ | Mínima o ligera | Baja | Regular |
| 2 (Intermedio) | Moderada | Media o moderada | Baja o moderada | Regular |
| 3 (Alto) | Aumentada | Moderada a pronunciada | Moderada a alta | Irregular |
| 4 (Alto) | Marcadamente ↑ | Marcado pleomorfismo | Alta | Irregular, abundante |
* Los osteosarcomas de bajo grado (1) tienen excelente pronóstico solo con cirugía. Los de grado intermedio (2) tienen pronóstico intermedio. Los de alto grado (3-4) requieren quimioterapia.
Factores pronósticos
- 📈 Respuesta a la quimioterapia neoadyuvante: Es el factor pronóstico independiente más potente. Pacientes con necrosis tumoral ≥90% (buena respuesta) tienen una supervivencia libre de eventos a 5 años del 70-80%, frente al 40-50% en aquellos con necrosis <90% (mala respuesta).
- 📈 Presencia de metástasis al diagnóstico: El 20% de los pacientes tienen metástasis detectables (principalmente pulmonares). La supervivencia a 5 años cae al 20-30%. La resecabilidad completa de las metástasis mejora el pronóstico.
- 📈 Localización del tumor primario: Los tumores de localización axial (pelvis, columna) tienen peor pronóstico que los de extremidades, debido a la dificultad para lograr una resección amplia. Los tumores craneofaciales tienen mejor pronóstico si se resecan completamente.
- 📈 Resecabilidad quirúrgica (márgenes R0): Es el factor pronóstico más importante desde el punto de vista quirúrgico. La resección completa con márgenes negativos es esencial para la curación.
- 📈 Tamaño tumoral: Tumores >10 cm se asocian a peor pronóstico.
- 📈 Skip metástasis: Su presencia (intraóseas, separadas del tumor primario) empeora drásticamente el pronóstico.
- 📈 Niveles de fosfatasas alcalinas y LDH: Elevados al diagnóstico se asocian a peor pronóstico.
- 📈 Subtipo histológico: Los subtipos de bajo grado (parosteal, central de bajo grado) tienen excelente pronóstico. El telangiectásico, post-Paget y post-irradiación (todos grado 4) tienen peor pronóstico.
- 📈 Edad: Los pacientes muy jóvenes (<10 años) y los ancianos (>40 años) pueden tener peor pronóstico, aunque es un factor controvertido.
- 📈 Factores moleculares (en investigación): Expresión de HER2, glicoproteína-P, pérdida de heterocigosidad de RB1 y p53, etc., no han demostrado ser predictores consistentes en la práctica clínica.
Tratamiento
Premisa fundamental: El tratamiento del osteosarcoma de alto grado es multimodal y debe ser llevado a cabo en centros de referencia. La cirugía sola no es suficiente (menos del 20% de supervivencia a largo plazo). La quimioterapia (neoadyuvante y adyuvante) es esencial para el control de la enfermedad micrometastásica.
6.1 Quimioterapia (QT)
- 💡 Régimen estándar: MAP (Metotrexato a altas dosis, Doxorrubicina [Adriamicina], Cisplatino). Se administra tanto en neoadyuvancia (preoperatorio) como en adyuvancia (postoperatorio).
- 💡 Neoadyuvante: Duración aproximada de 10 semanas. Objetivos: tratar micrometástasis, facilitar la cirugía (reducir tumor, mejorar márgenes) y evaluar la respuesta histológica (factor pronóstico).
- 💡 Adyuvante: Se completa tras la cirugía hasta un total de aproximadamente 29 semanas de tratamiento. En algunos protocolos, se modifica el régimen en los malos respondedores (necrosis <90%) a otras combinaciones (ifosfamida/etopósido), aunque el beneficio de este cambio no está sólidamente probado.
- 💡 QT intraarterial: Se ha utilizado en algunos centros, pero no ha demostrado superioridad sobre la QT intravenosa sistémica.
6.2 Cirugía
- 💡 Objetivo: Resección amplia con márgenes negativos (R0).
- 💡 Cirugía preservadora de extremidad: Actualmente posible en >85% de los casos de extremidades. Requiere una planificación meticulosa basada en la RM preoperatoria y la disponibilidad de técnicas de reconstrucción: megaprótesis (endoprótesis), aloinjertos, injertos autólogos vascularizados, artrodesis, colgajos microquirúrgicos, rotacionplastia.
- 💡 Amputación: Indicada cuando no es posible una resección amplia con preservación funcional (infiltración masiva del paquete vasculonervioso, recidiva local extensa, esqueletización del miembro).
- 💡 Manejo de las skip metástasis: Si se detectan, la resección debe incluir todo el hueso afectado (resección segmentaria amplia o amputación).
6.3 Radioterapia (RT)
- 💡 Papel limitado. El osteosarcoma es poco radiosensible. Puede utilizarse en tumores irresecables (pelvis, columna, base de cráneo), en resecciones con márgenes positivos donde no es posible una re-resección, o como tratamiento paliativo de metástasis sintomáticas.
6.4 Tratamiento por escenario clínico
- 💡 Osteosarcoma localizado de alto grado (estándar): QT neoadyuvante MAP → Cirugía de resección amplia R0 (preservación o amputación) → QT adyuvante MAP (ajustada o no según respuesta).
- 💡 Osteosarcoma localizado de bajo grado (parosteal, central de bajo grado, sin invasión medular): Cirugía de resección amplia R0. No requiere QT.
- 💡 Osteosarcoma metastásico al diagnóstico (10-20%): QT neoadyuvante MAP → Cirugía del primario + metastasectomía pulmonar completa (si es posible) → QT adyuvante. El pronóstico es peor, pero la cirugía completa de todas las metástasis es el factor más importante. La supervivencia a largo plazo puede alcanzar el 20-40% en casos seleccionados.
- 💡 Osteosarcoma recurrente: La recidiva más frecuente es pulmonar. La cirugía de las metástasis (metastasectomía) es el pilar si es completa. La QT de segunda línea (ifosfamida, etopósido) tiene actividad limitada (respuestas en ~30%). La recidiva local tiene muy mal pronóstico.
| Escenario | Tratamiento | Pronóstico (SG 5 años) |
|---|---|---|
| Localizado de alto grado | QT neoadyuvante MAP → Cirugía R0 → QT adyuvante MAP | 60-70% |
| Localizado de bajo grado | Cirugía R0 (sola) | >90% |
| Metastásico al diagnóstico (resecable) | QT neoadyuvante MAP → Cirugía R0 + metastasectomía → QT adyuvante | 20-40% |
| Recurrente (solo pulmón, resecable) | Metastasectomía ± QT | 20-30% |
| Recurrente (irresecable / óseo) | QT paliativa (ifosfamida/etopósido), TKI, soporte | <10% |
Pronóstico, seguimiento y efectos tardíos
- 📈 Pronóstico general (alto grado localizado): Supervivencia global a 5 años del 60-70% con tratamiento multimodal.
- 📈 Historia natural sin QT: Menos del 20% de los pacientes con enfermedad localizada tratada solo con cirugía sobreviven libres de recaída. El 80% desarrollan metástasis (principalmente pulmonares) en los primeros 2 años.
- 📈 Seguimiento sugerido:
- 🔹 Primeros 2-3 años: Exploración física y TC torácico de baja dosis cada 2-3 meses. RM de la región primaria cada 3-4 meses.
- 🔹 Hasta 5 años: Cada 4-6 meses con imagen local y TC torácico.
- 🔹 Hasta 10 años: Anual. Riesgo de metástasis tardías y efectos secundarios del tratamiento.
- 📈 Efectos tardíos del tratamiento (seguimiento a largo plazo):
- 🔹 Cardiotoxicidad por antraciclinas (doxorrubicina): 20-50% de los pacientes pueden tener anormalidades cardíacas subclínicas (disfunción sistólica/diastólica). El riesgo aumenta con dosis acumulada >450 mg/m². Requiere monitorización ecocardiográfica periódica.
- 🔹 Nefrotoxicidad por cisplatino e ifosfamida: Disminución de la tasa de filtración glomerular (60% de pacientes con cisplatino a altas dosis). La ifosfamida causa daño tubular (síndrome de Fanconi, hipofosfatemia). Requiere control de función renal y electrolitos.
- 🔹 Ototoxicidad por cisplatino: Pérdida auditiva de alta frecuencia, parcialmente reversible. Audiometrías periódicas.
- 🔹 Segundas neoplasias: Aumento del riesgo de leucemia (relacionado con agentes alquilantes) y de otros tumores sólidos en campos de radiación.
- 🔹 Problemas musculoesqueléticos a largo plazo (después de la cirugía): Relacionados con la cirugía: aflojamiento de prótesis, fractura de aloinjerto, infección, limitación funcional. La rotacionplastia y las resecciones amplias pueden tener secuelas.
- 🔹 Infertilidad: Por QT, especialmente en varones.
- 🔹 Calidad de vida: La mayoría de los estudios muestran buena integración social y laboral, aunque pueden existir limitaciones funcionales. No hay diferencias claras en calidad de vida global entre pacientes amputados y con cirugía preservadora.
Algoritmo diagnóstico-terapéutico
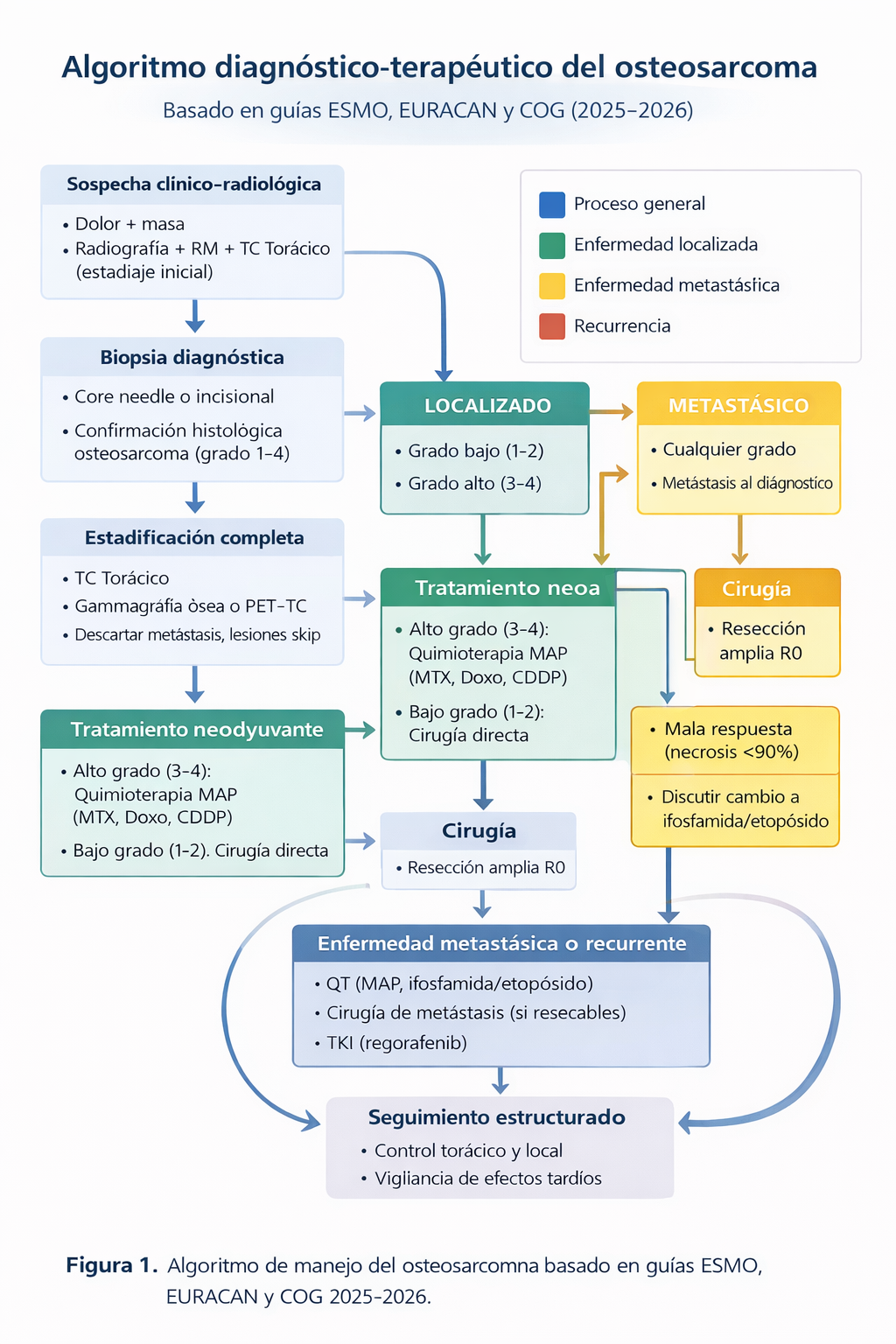
Resumen para la práctica clínica
📌 Indicaciones
- ✅ Quimioterapia neoadyuvante y adyuvante (régimen MAP) en osteosarcoma de alto grado (3-4) localizado.
- ✅ Cirugía de resección amplia (R0) con preservación de extremidad siempre que sea oncológicamente segura y funcionalmente viable.
- ✅ Metastasectomía pulmonar completa en enfermedad metastásica controlada.
🔧 Técnica
- 🔧 Biopsia: por equipo quirúrgico, con trayecto excindible.
- 🔧 Quimioterapia: administración en centros con experiencia en altas dosis de metotrexato y monitorización de niveles.
- 🔧 Cirugía: resección con márgenes de 2-3 cm proximal al tumor (RM preoperatoria). Reconstrucción con megaprótesis, aloinjertos o colgajos según defecto.
⚠️ Riesgos
- ⚠️ Mala respuesta a QT (necrosis <90%).
- ⚠️ Metástasis a distancia, especialmente pulmonares.
- ⚠️ Recidiva local (5-10% con márgenes R0).
- ⚠️ Complicaciones quirúrgicas: infección, aflojamiento de prótesis, fractura de aloinjerto.
- ⚠️ Toxicidad por QT: cardiotoxicidad (doxorrubicina), nefrotoxicidad/ototoxicidad (cisplatino), hepatotoxicidad/mucositis (metotrexato).
- ⚠️ Segundos tumores.
✅ Resultados
- ✅ Supervivencia global a 5 años (alto grado localizado): 60-70%.
- ✅ Supervivencia libre de eventos a 5 años: 70-80% en buenos respondedores vs 40-50% en malos respondedores.
- ✅ Supervivencia a 5 años en enfermedad metastásica resecable: 20-30%.
Bibliografía
Clasificación OMS, epidemiología, guías
- 📄 WHO Classification of Tumours Editorial Board. WHO Classification of Tumours of Soft Tissue and Bone. 5th ed. Lyon: IARC Press; 2020.
- 📄 Casali PG, Bielack S, Abecassis N, et al. Bone sarcomas: ESMO-PaedCan-EURACAN Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2018;29(Suppl 4):iv79-iv95.
- 📄 National Cancer Institute. Osteosarcoma and Undifferentiated Pleomorphic Sarcoma of Bone Treatment (PDQ®) – Health Professional Version. 2025.
Histopatología y gradación
- 📄 Unni KK, Dahlin DC. Grading of bone tumors. Semin Diagn Pathol. 1984;1(3):165-172.
Tratamiento y pronóstico
- 📄 Bielack SS, Kempf-Bielack B, Delling G, et al. Prognostic factors in high-grade osteosarcoma of the extremities or trunk: an analysis of 1,702 patients. J Clin Oncol. 2002;20(3):776-790.
- 📄 Isakoff MS, Bielack SS, Meltzer P, Gorlick R. Osteosarcoma: Current Treatment and a Collaborative Pathway to Success. J Clin Oncol. 2015;33(27):3029-3035.
Efectos tardíos
- 📄 Longhi A, Ferrari S, Bacci G, Specchia S. Long-term follow-up of patients with doxorubicin-induced cardiac toxicity after chemotherapy for osteosarcoma. Anticancer Drugs. 2007;18(6):737-744.
- 📄 Tunn PU, Schmidt-Peter P, Pomraenke D, Hohenberger P. Long-term results and quality of life after treatment of osteosarcoma in children. Chirurg. 1998;69(8):862-869.
