Última revisión:
Estrategias diagnósticas en tumores musculoesqueléticos
El diagnóstico de los tumores musculoesqueléticos exige un enfoque integrado y secuencial, combinando clínica, radiología, estadificación y biopsia planificada.
El objetivo no es solo identificar la lesión, sino hacerlo en el orden correcto, evitando errores frecuentes como biopsias prematuras,
subestimación de masas de partes blandas o asumir lesiones metastásicas sin completar el estudio.
Esta página resume las estrategias diagnósticas más útiles en la práctica: evaluación clínica inicial, interpretación radiológica sistemática,
algoritmos diagnósticos, uso racional de las distintas modalidades de imagen, orientación de metástasis óseas de origen desconocido y principios clave de biopsia.
Navega directamente por apartados:
1) Introducción: enfoque sistemático del diagnóstico
Principios fundamentales del diagnóstico oncológico musculoesquelético:
- • Enfoque sistemático y secuencial: clínica → imagen básica → imagen avanzada → biopsia planificada.
- • Correlación obligada: datos clínicos + hallazgos radiológicos + patología deben concordar.
- • Biopsia como último paso: nunca realizar biopsia sin evaluación imagenológica completa.
- • Derivación temprana: ante duda o sospecha de malignidad, derivar a centro especializado SIN biopsiar.
Puerta diagnóstica correcta: orientación transversal
Antes de pensar en un subtipo, sitúa el caso en su puerta correcta: tumor óseo, masa de partes blandas o lesión articular / tumor-like. A partir de ahí, el eje de trabajo cambia: radiografía y patrón de agresividad en hueso; tamaño, profundidad, ecografía/RM y red flags en partes blandas; y contexto periarticular / sinovial en lesiones articulares.
Empieza por radiografía simple, patrón de destrucción ósea, zona de transición, matriz, reacción perióstica y eventual masa de partes blandas.
La pregunta inicial no es el subtipo histológico, sino si la masa parece banal, indeterminada o sospechosa de sarcoma.
Valora relación con articulación, sinovial, tendón o bursa y distingue lesiones inflamatorias, reactivas, proliferativas y neoplásicas.
Idea práctica: el error más frecuente no es “equivocar el nombre” del tumor, sino entrar por la puerta diagnóstica incorrecta y pedir pruebas o biopsias fuera de secuencia.
Flujo diagnóstico general simplificado
- 1 Sospecha clínica: dolor óseo, masa palpable, síntomas constitucionales.
- 2 Evaluación inicial: historia completa, examen físico, laboratorio básico.
- 3 Imagen básica: radiografía simple de la zona afectada (si hueso) o ecografía (si partes blandas).
- 4 Clasificación inicial: determinar si la lesión parece:
- Benigna típica/no agresiva → seguimiento
- Benigna atípica/agresiva → estudios adicionales
- Probablemente maligna → derivación inmediata
- Metástasis sospechada → búsqueda de primario
- 5 Estudios de extensión: según hallazgos iniciales (TC tórax, RM local, gammagrafía ósea).
- 6 Biopsia planificada: solo si está indicada y tras completar estudios de imagen.
- 7 Integración multidisciplinaria: decisión terapéutica basada en diagnóstico completo.
Qué necesito resolver hoy
| Pregunta clínica | Qué debo resolver | Siguiente paso |
|---|---|---|
| ¿Estoy en hueso o en partes blandas? | Definir el territorio anatómico real de la lesión | Radiografía si hueso; ecografía/RM si masa de partes blandas |
| ¿Parece banal o agresiva? | Estimar agresividad con clínica + imagen | Seguimiento, estudio ampliado o derivación especializada |
| ¿Necesito biopsia? | Decidir si la biopsia cambia conducta y si ya está bien planificada | No biopsiar hasta completar imagen y plan quirúrgico |
| ¿Puede ser metástasis o proceso sistémico? | No asumir tumor primario en adultos con contexto compatible | Búsqueda de primario, extensión y laboratorio dirigido |
| ¿Debo derivar ya? | Reconocer criterios de sospecha oncológica | Derivación precoz a centro especializado |
ERRORES FRECUENTES A EVITAR:
- Realizar biopsia sin estudios de imagen completos.
- Interpretar radiografías aisladas sin contexto clínico.
- Subestimar masas de tejidos blandos >5 cm o profundas.
- No considerar metástasis en pacientes >40 años con lesión lítica.
- Realizar biopsia en consultorio o centro no especializado.
2) Evaluación clínica inicial integral
Historia clínica dirigida en oncología musculoesquelética
| Elemento | Preguntas clave | Significado |
|---|---|---|
| Dolor | Carácter, intensidad, ritmo circadiano, respuesta a AINEs | Dolor nocturno/reposo sugiere agresividad. Mejoría con AINEs puede sugerir osteoma osteoide |
| Masa | Tiempo de evolución, crecimiento, cambios recientes | Crecimiento rápido (> semanas-meses) sugiere agresividad |
| Sistémico | Pérdida de peso, fiebre, sudoración nocturna, astenia | Sugieren malignidad o proceso sistémico (linfoma, metástasis) |
| Antecedentes | Historia oncológica personal/familiar, radiación previa | Metástasis o tumores secundarios a radiación |
| Trauma | Relación temporal con aparición de síntomas | El "trauma recordatorio" es común pero raramente causal |
Examen físico sistemático
- • Inspección: masa visible, cambios cutáneos, circulación colateral, deformidad.
- • Palpación: tamaño, consistencia, movilidad, temperatura, pulsátil, dolor.
- • Función: rango articular, fuerza, marcha, signos neurológicos/vasculares.
- • Examen regional: ganglios regionales, otras masas, contralateral.
- • Examen general: busca signos de enfermedad sistémica o primario oculto.
Estudios de laboratorio iniciales
| Prueba | Indicación principal | Interpretación |
|---|---|---|
| VSG/Proteína C reactiva | Toda lesión sospechosa | Elevada en infección, algunos tumores (Ewing, mieloma, metástasis) |
| Fosfatasa alcalina | Lesiones óseas en niños/adolescentes | Elevada en osteosarcoma, enfermedad de Paget, metástasis óseas |
| Hemograma completo | Sospecha de proceso sistémico | Anemia en mieloma, metástasis; alteraciones en leucemia/linfoma |
| Proteinograma/Immunofijación | Lesiones líticas múltiples >40 años | Pico monoclonal en mieloma múltiple |
| PSA (hombres >50 años) | Lesiones óseas blásticas | Elevado en metástasis de cáncer de próstata |
| Calcio/fósforo/PTH | Lesiones líticas múltiples | Hipercalcemia en metástasis, mieloma; hiperparatiroidismo |
3) Interpretación radiológica sistemática
La radiografía simple es la herramienta más importante en el diagnóstico inicial de tumores óseos. Una interpretación sistemática debe evaluar: localización anatómica, margen de la lesión, patrón de destrucción ósea, reacción perióstica, matriz mineralizada y efectos sobre tejidos blandos.
Sistema de interpretación radiológica (acrónimo FEGNOMASHIC modificado)
| Característica | Pregunta | Interpretación |
|---|---|---|
| F - Focales/múltiples | ¿Es solitaria o múltiple? | Múltiple: metástasis, mieloma, histiocitosis, encondromatosis |
| E - Edad | ¿Edad del paciente? | <20: primarios; 20-40: TCG, condrosarcoma; >40: metástasis, mieloma |
| G - Geografía | ¿Dónde en el hueso? | Epífisis: TCG, condroblastoma; metáfisis: mayoría; diáfisis: Ewing, histiocitosis |
| N - Naturaleza del margen | ¿Bien definido o mal definido? | Margen nítido: benigno/lento; permeativo/mal definido: agresivo/rápido |
| O - Osificación/matrix | ¿Hay matriz mineralizada? | Osificación: osteogénico; calcificación "anillos y arcos": cartilaginoso |
| M - Morfología | ¿Expansión, destrucción cortical? | Expansión con cortical delgada: benigno agresivo; destrucción cortical: maligno |
| A - Agresividad | ¿Reacción perióstica? | Continua/laminar: benigno; interrumpida (Codman, en "sol naciente"): agresivo |
| S - Soft tissue | ¿Masa de partes blandas? | Presencia sugiere agresividad (maligno o benigno agresivo) |
| H - Historia | ¿Cambios con el tiempo? | Comparar con estudios previos si disponibles |
| I - Intensidad gammagráfica | ¿Captación en gammagrafía? | Intensa: activo/agresivo; leve/ausente: latente |
| C - Cambios articulares | ¿Afectación articular? | Raro excepto TCG, sinovitis villonodular, condromatosis |
Zonas de transición: clave para determinar agresividad
| Tipo | Características radiológicas | Interpretación | Ejemplos |
|---|---|---|---|
| IA (Lodwick) | Margen geográfico con esclerosis completa | Lesión no agresiva, crecimiento lento | Quiste óseo simple, fibroma no osificante curado |
| IB (Lodwick) | Margen geográfico sin esclerosis completa | Lesión activa pero típicamente benigna | Quiste óseo aneurismático, tumor de células gigantes |
| IC (Lodwick) | Margen geográfico mal definido | Lesión agresiva localmente | Osteoblastoma agresivo, condrosarcoma grado I |
| II (Lodwick) | Patrón apolillado/permeativo | Lesión maligna o infección | Sarcoma de Ewing, osteosarcoma, osteomielitis |
| III (Lodwick) | Patrón permeativo difuso | Lesión altamente agresiva | Metástasis, linfoma, sarcoma de alto grado |
Patrones de reacción perióstica
- • Continua/laminar ("en capas de cebolla"): lesión benigna agresiva (osteomielitis, quiste óseo aneurismático).
- • Interrumpida ("triángulo de Codman"): lesión que levanta el periostio → sugiere agresividad (maligno o benigno agresivo).
- • Formación de espículas ("sol naciente" o "en punta de hierba"): patognomónico de osteosarcoma convencional.
- • Ausente: lesión intraósea no agresiva o destrucción tan rápida que no da tiempo a reacción.
4) Algoritmos diagnósticos paso a paso
Algoritmo diagnóstico principal: masa ósea solitaria
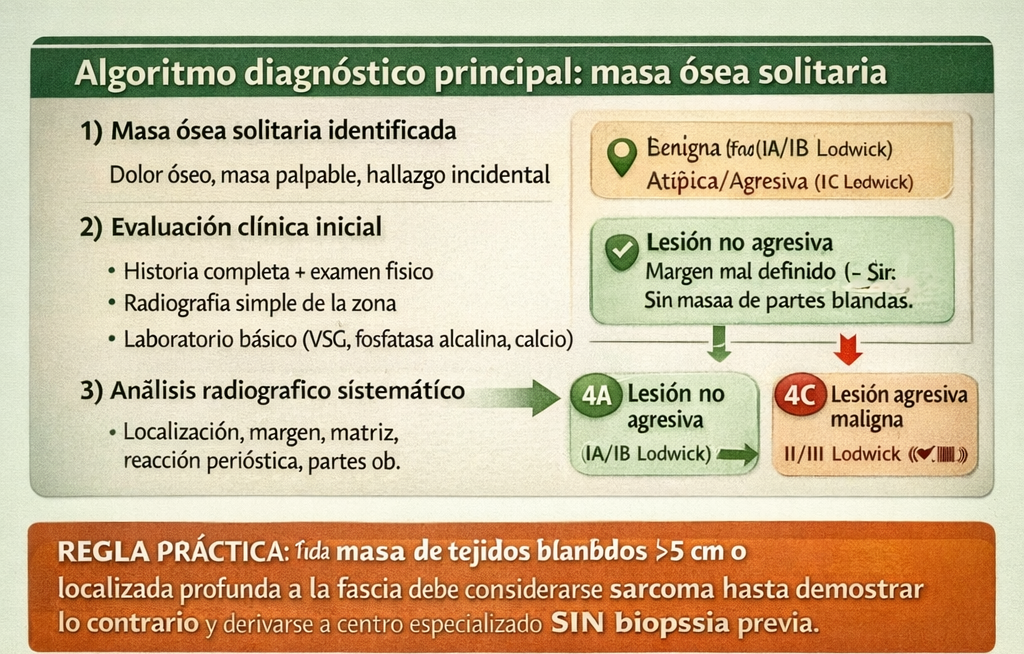
Ver algoritmo en texto (fallback)
Dolor óseo, masa palpable, hallazgo incidental
• Historia completa + examen físico
• Radiografía simple de la zona
• Laboratorio básico (VSG, fosfatasa alcalina, calcio)
Localización, margen, matriz, reacción perióstica, partes blandas
• Margen geográfico bien definido
• Sin destrucción cortical
• Sin masa de partes blandas
• Sin síntomas agresivos
• Según diagnóstico específico
• RX control 3-6 meses inicialmente
• Tratar solo si síntomas o riesgo fractura
• Margen mal definido (IC)
• Expansión ósea
• Posible masa partes blandas
• Dolor progresivo
• RM local (extensión intra/extraósea)
• TC si duda sobre matriz/mineralización
• Derivar a centro especializado
• Margen permeativo/apolillado
• Destrucción cortical
• Masa partes blandas evidente
• Reacción perióstica agresiva
• A centro oncológico especializado
• NO realizar biopsia local
• Completar estudios de extensión en centro receptor
Algoritmo: paciente >40 años con lesión lítica solitaria

Ver algoritmo en texto (fallback)
Sospecha alta de metástasis o mieloma
• Gammagrafía ósea total corporal
• TC tórax/abdomen/pelvis
• Laboratorio: PSA (♂), proteinograma, calcio
• Examen físico dirigido (mama, próstata, tiroides, piel)
• Manejo según tumor primario
• Biopsia de lesión ósea solo si diagnóstico incierto
• Tratamiento oncológico sistémico ± local
• Biopsia de lesión accesible
• Inmunohistoquímica según patología
• PET/TC si disponible
• Tratamiento empírico según perfil más probable
5) Modalidades de imagen avanzadas
Selección de modalidades de imagen según contexto clínico
| Modalidad | Indicaciones principales | Ventajas | Limitaciones |
|---|---|---|---|
| Radiografía simple | PRIMERA LÍNEA en toda sospecha de tumor óseo | Bajo costo, disponible, excelente para diagnóstico inicial, evalúa matriz | Limitada para extensión de partes blandas, pobre sensibilidad temprana |
| Ecografía | Masas de tejidos blandos, guía de biopsia, caracterización quística vs sólida | Sin radiación, dinámica, evalúa vascularización, guía procedimientos | Operador-dependiente, limitada penetración, pobre para hueso |
| Tomografía Computarizada (TC) | Evaluación de matriz mineralizada, cortical, planificación quirúrgica, tórax (metástasis) | Excelente para hueso cortical, detección de calcificación, rápida | Radiación ionizante, contraste limitado en tejidos blandos |
| Resonancia Magnética (RM) | Evaluación de extensión intra/extraósea, relación neurovascular, respuesta a QT | Mejor contraste de tejidos blandos, multiplanar, sin radiación | Costo, tiempo, artefactos por metal, contraindicaciones (marcapasos) |
| Gammagrafía ósea (Tc-99m) | Detección de metástasis óseas, lesiones múltiples, evaluación de actividad | Alta sensibilidad para metástasis, estudio corporal total | Baja especificidad, pobre resolución anatómica, falsos positivos |
| PET/TC (FDG) | Estadiaje de sarcomas de alto grado, respuesta a tratamiento, recidiva | Información metabólica + anatómica, alta sensibilidad para enfermedad sistémica | Costo elevado, disponibilidad limitada, falsos positivos (inflamación) |
RM vs TC: indicaciones específicas
| Situación clínica | Modalidad preferida | Razón |
|---|---|---|
| Evaluación extensión medular tumoral | RM | Superior para definir extensión intraósea, skip metastases |
| Evaluación de matriz mineralizada | TC | Mejor para detectar calcificación/ossificación, evaluación cortical |
| Relación con estructuras neurovasculares | RM | Mejor contraste para nervios/vasos, múltiples planos |
| Planificación quirúrgica de prótesis | TC (y RM) | TC para medidas óseas precisas; RM para extensión partes blandas |
| Respuesta a quimioterapia neoadyuvante | RM (con contraste) | Evalúa necrosis tumoral, cambios en vascularización |
| Sospecha de fractura patológica inminente | TC | Mejor para integridad cortical, evaluación biomecánica |
Secuencia recomendada de estudios de imagen:
- 1 Siempre comenzar con radiografía simple (dos proyecciones).
- 2 Si lesión parece agresiva o diagnóstico incierto → RM local (con contraste).
- 3 Si se necesita evaluar matriz mineralizada o planificación quirúrgica precisa → añadir TC.
- 4 Si sospecha de malignidad → TC tórax para estadificación pulmonar.
- 5 Si paciente >40 años o sospecha de metástasis/mieloma → gammagrafía ósea o PET/TC.
- 6 NUNCA realizar biopsia sin RM/TC local previa para planificar trayecto.
Tres escenarios concentran la mayoría de las decisiones iniciales: lesión ósea sospechosa, masa de tejidos blandos y lesión agresiva en el adulto con posible origen metastásico. En esta página se resumen como orientación estratégica inicial; el desarrollo detallado de cada grupo corresponde a sus páginas específicas.
Rutas de profundización
Desde esta página troncal puedes pasar al desarrollo específico de cada escenario.
Desarrollo del estudio de tumores primarios, estadiaje prebiopsia y correlación clínico-radiológica.
Ver tumores primariosAccede al desarrollo específico de masas de partes blandas, RM y criterios de sospecha.
Ver partes blandasDesarrollo del estudio de metástasis óseas, búsqueda de primario y secuencia diagnóstica.
Ver metástasis6) Lesión ósea sospechosa: orientación inicial
La estrategia ante una lesión ósea sospechosa no consiste en “adivinar el tumor” en la primera visita, sino en orientar correctamente el caso a partir de la edad, la localización, el patrón radiológico de agresividad, la matriz tumoral y la eventual masa de partes blandas.
Cómo orientar una lesión ósea sospechosa
| Clave de orientación | Qué debo mirar | Implicación práctica |
|---|---|---|
| Edad | Niño/adolescente, adulto joven o >40 años | En jóvenes predominan primarios; en >40 años obligan a descartar metástasis o mieloma antes de asumir primario óseo |
| Localización | Epífisis, metáfisis, diáfisis, pelvis, columna o superficie ósea | La localización estrecha mucho el diagnóstico diferencial y cambia el umbral de sospecha |
| Agresividad radiológica | Zona de transición, destrucción cortical, patrón permeativo, reacción perióstica | Cuanto peor definido y más destructivo sea el patrón, mayor necesidad de RM, derivación y planificación oncológica |
| Matriz | Osteoide, condroide, lítica pura o mixta | La matriz ayuda a clasificar el tipo de lesión y a elegir mejor la correlación con TC o RM |
| Partes blandas | Masa extraósea, edema desproporcionado o extensión fuera del hueso | Eleva la sospecha de agresividad y obliga a completar estudio local antes de plantear biopsia |
Preguntas prácticas que deben resolverse
- • ¿La radiografía muestra una lesión no agresiva típica? Si sí, puede bastar seguimiento o confirmación dirigida.
- • ¿Hay signos de agresividad local? Entonces se requiere RM local y valoración especializada.
- • ¿La edad o el contexto obligan a pensar primero en metástasis/mieloma? Especialmente en adultos >40 años.
- • ¿La lesión necesita biopsia? Solo tras completar imagen local y estadificación según el caso.
- • ¿Hay riesgo de fractura o compromiso estructural? Esto puede condicionar la urgencia de derivación y la secuencia terapéutica.
Idea clave: en una lesión ósea sospechosa, la radiografía manda y la biopsia nunca debe adelantarse a la caracterización por imagen y a la planificación del trayecto.
Siguiente paso: si el caso encaja con una lesión ósea primaria sospechosa, continúa en estrategias en los tumores primarios.
7) Masa de tejidos blandos: aproximación
REGLA PRÁCTICA: toda masa de tejidos blandos ≥5 cm o profunda a la fascia debe considerarse sarcoma hasta demostrar lo contrario y derivarse a centro especializado sin biopsia previa no planificada.
Algoritmo para evaluación de masa de tejidos blandos

Ver algoritmo en texto (fallback)
Palpable, visible o incidental en estudios de imagen
• Tamaño
• Profundidad
• Crecimiento
• Consistencia, movilidad, dolor
• Ecografía inicial
• Si rasgos claramente benignos → control o excisión simple
• Si dudas → RM para caracterización
• Derivación especializada
• RM local con contraste
• Biopsia planificada por el equipo definitivo
Qué debe responder la evaluación inicial
| Pregunta | Qué debo determinar | Consecuencia |
|---|---|---|
| ¿Es superficial o profunda? | Relación real con la fascia | La profundidad aumenta el nivel de sospecha y suele exigir RM |
| ¿Cuánto mide de verdad? | Diámetro máximo clínico y por imagen | El tamaño ≥5 cm obliga a pensar en sarcoma y derivar |
| ¿Crece o cambia? | Evolución temporal, rapidez de crecimiento, dolor asociado | El crecimiento progresivo reduce la probabilidad de lesión banal |
| ¿La ecografía basta? | Diferenciar quístico vs sólido y valorar rasgos claramente benignos | Si persisten dudas, la prueba clave es la RM |
| ¿Necesito biopsia o derivación? | Determinar si el caso requiere circuito oncológico | La biopsia solo debe hacerse cuando ya existe planificación del trayecto |
Qué debe responder la RM en una masa de tejidos blandos
- • Tamaño real y extensión completa de la lesión.
- • Profundidad respecto a la fascia y compartimento afectado.
- • Relación con paquetes neurovasculares, tendones, hueso y articulación.
- • Composición predominante: grasa, componente sólido, necrosis, hemorragia, septos.
- • Homogeneidad o heterogeneidad y patrón de realce.
- • Mejor zona para biopsia, evitando áreas necróticas o poco representativas.
Idea clave: en partes blandas, la pregunta inicial no es “qué subtipo exacto es”, sino si la masa parece claramente banal, indeterminada o sospechosa de sarcoma, porque eso define el circuito diagnóstico correcto.
Siguiente paso: si el caso encaja con una lesión ósea primaria sospechosa, continúa en estrategias en los tumores primarios.
8) Metástasis óseas de origen desconocido
PRINCIPIO FUNDAMENTAL: en un paciente >40 años con lesión ósea agresiva o lítica solitaria, el planteamiento inicial debe ser metástasis o mieloma hasta demostrar lo contrario.
Secuencia práctica de estudio inicial
| Paso | Qué debo hacer | Objetivo |
|---|---|---|
| 1. Confirmar agresividad | Radiografía de la lesión + correlación clínica | Diferenciar hallazgo banal de lesión que exige estudio sistémico |
| 2. Buscar enfermedad sistémica | TC tórax/abdomen/pelvis con contraste y estudio óseo global según contexto | Identificar primario y otras lesiones |
| 3. Dirigir laboratorio | Hemograma, función renal, calcio, fosfatasa alcalina, proteinograma, PSA u otros según sospecha | Detectar mieloma, metástasis y pistas de origen |
| 4. Decidir biopsia | Biopsiar solo cuando el primario no está claro o cuando el resultado cambia la conducta | Evitar procedimientos innecesarios o mal secuenciados |
Algoritmo práctico: lesión agresiva en el adulto
Especialmente si es lítica, destructiva o dolorosa
• Historia y exploración completas
• Radiografía de la lesión
• Laboratorio básico orientado
• TC tórax/abdomen/pelvis
• Estudio de extensión ósea si procede
• Manejo según tumor primario
• Confirmación histológica solo si es necesaria
• Valorar tratamiento sistémico, local y estabilización
• Biopsia de la localización más accesible y rentable
• Anatomía patológica + inmunohistoquímica según hallazgos
• Revisión multidisciplinaria antes de cerrar estrategia
Preguntas que deben resolverse antes de biopsiar
- • ¿La edad y el contexto hacen improbable un primario óseo?
- • ¿Ya se ha completado la búsqueda de primario con TC y laboratorio dirigido?
- • ¿Existe otra localización más accesible o segura para biopsia?
- • ¿El resultado de la biopsia cambiará realmente la conducta inmediata?
- • ¿Se ha valorado el riesgo estructural o de fractura patológica?
Idea clave: en este escenario, el error frecuente no es olvidar una entidad rara, sino pensar demasiado pronto en sarcoma primario y no completar primero el estudio sistémico.
Siguiente paso: si el escenario orienta a metástasis ósea o primario desconocido, continúa en estrategias en las metástasis.
9) Estrategia de biopsia y muestreo
LA BIOPSIA MAL PLANIFICADA ES LA PRINCIPAL CAUSA DE COMPLICACIONES Y RESULTADOS SUBÓPTIMOS en el tratamiento de tumores musculoesqueléticos. Debe ser realizada por o en estrecha consulta con el equipo que realizará el tratamiento definitivo.
Principios fundamentales de la biopsia oncológica
- 1 Último paso diagnóstico: Solo después de completar evaluación clínica y estudios de imagen.
- 2 Planificada por el cirujano definitivo: Trayecto resecable en cirugía definitiva.
- 3 Guíada por imagen: Preferiblemente bajo TC o ecografía para muestras representativas.
- 4 Trayecto longitudinal: En extremidades, paralelo al eje largo del miembro.
- 5 Mínima disrupción: No disecar planos, no usar torniquete neumático (o desinflar antes de cerrar).
- 6 Hematoma contenido: Cierre hermético por planos para contener células tumorales.
- 7 Muestra adecuada: Para histología convencional, inmunohistoquímica, estudios moleculares.
Tipos de biopsia y sus indicaciones
| Tipo | Indicaciones | Ventajas | Limitaciones |
|---|---|---|---|
| Biopsia con aguja gruesa (Tru-Cut) | • PRIMERA ELECCIÓN para la mayoría de tumores • Partes blandas y hueso (si destructivo) • Guiada por TC/ecografía |
Mínima morbilidad, muestra para arquitectura, menor contaminación, puede ser ambulatoria | Requiere experiencia, muestra limitada, riesgo de muestra no representativa |
| Biopsia abierta (incisional) | • Biopsias con aguja no diagnósticas • Tumores muy fibrosos/necrosados • Necesidad de muestra grande para estudios |
Muestra amplia, visualización directa, menor tasa de no diagnóstico | Mayor morbilidad, mayor riesgo de complicaciones, requiere hospitalización |
| Biopsia escisional | • Tumores pequeños (<3 cm) superficiales • Alta probabilidad de benignidad • Margen de tejido normal incluido |
Diagnóstico y tratamiento en un tiempo | Si es maligno, puede comprometer cirugía definitiva. Solo en casos seleccionados |
| Biopsia por trefina ósea | • Lesiones óseas escleróticas/densas • Necesidad de evaluar médula ósea • Mieloma, metástasis |
Obtiene cilindro óseo, buena para evaluación arquitectural | Dolorosa, riesgo de fractura, requiere anestesia |
Reglas de oro para la biopsia
- • NUNCA realizar biopsia transcompartimental: No cruzar planos fasciales no resecables.
- • Evitar contaminación neurovascular: Mantener distancia de paquetes neurovasculares.
- • Planificar trayecto resecable: El trayecto de biopsia debe poder extirparse en bloque con el tumor.
- • Muestrear zona viable: Evitar áreas necróticas centrales o hemorrágicas.
- • Obtener muestra para patología y biología molecular: Fresca en suero salino (no formalina) para estudios genéticos.
- • Cultivo siempre: Incluso si baja sospecha de infección.
- • Documentar exactamente: Localización, profundidad, relaciones anatómicas.
SITUACIONES ESPECIALES QUE REQUIEREN CONSIDERACIONES ADICIONALES:
- Tumores pélvicos/axiales: Mayor riesgo de complicaciones. Considerar abordaje anterior vs posterior cuidadosamente.
- Tumores parosteales: Biopsia debe incluir base de implantación para evaluar invasión cortical.
- Tumores muy vasculares (riñón, tiroides): Considerar embolización pre-biopsia o biopsia con aguja fina.
- Pacientes pediátricos: Generalmente bajo anestesia general. Considerar impacto psicológico.
- Lesiones vertebrales: Abordaje específico según nivel. Alto riesgo de inestabilidad/compresión neurológica.
10) Integración multidisciplinaria
El diagnóstico definitivo en oncología musculoesquelética es un proceso multidisciplinario que requiere integración de datos clínicos, hallazgos radiológicos y patología. La discordancia entre cualquiera de estos tres pilares debe investigarse exhaustivamente antes de iniciar tratamiento.
Comité de Tumores Musculoesqueléticos: composición y funciones
| Especialista | Contribución específica | Momentos clave de participación |
|---|---|---|
| Cirujano ortopédico oncológico | Evaluación quirúrgica, planificación de biopsia/resección, reconstrucción | Desde primera consulta, planificación biopsia, decisión quirúrgica, seguimiento |
| Radiólogo musculoesquelético | Interpretación de estudios de imagen, guía de biopsia, evaluación respuesta | Interpretación inicial, planificación biopsia, reevaluación post-tratamiento |
| Patólogo oncológico | Diagnóstico histológico, gradación, estudios moleculares, márgenes quirúrgicos | Post-biopsia, intraoperatorio (congelado), evaluación de pieza quirúrgica |
| Oncólogo médico | Tratamiento sistémico (QT, terapia dirigida, inmunoterapia), manejo de efectos adversos | Estadificación, decisión de QT neoadyuvante/adyuvante, tratamiento paliativo |
| Radiooncólogo | Radioterapia neoadyuvante/adyuvante/paliativa, radioterapia intraoperatoria | Evaluación de indicación de RT, planificación, seguimiento de complicaciones |
| Médico rehabilitador | Recuperación funcional, manejo del dolor, adaptaciones, calidad de vida | Preoperatorio, postoperatorio inmediato, seguimiento a largo plazo |
| Psicólogo oncológico | Apoyo emocional, adaptación al diagnóstico, manejo de ansiedad/depresión | Tras diagnóstico, durante tratamiento, en recidiva o enfermedad avanzada |
Flujo de decisiones en comité de tumores
- 1 Presentación del caso: Datos clínicos relevantes, estudios de imagen, resultados de biopsia si disponibles.
- 2 Revisión de imágenes: Presentación sistemática de radiografías, RM, TC, PET/TC por radiólogo.
- 3 Revisión patológica: Presentación de hallazgos histológicos, gradación, estudios especiales.
- 4 Correlación tridimensional: ¿Concuerdan clínica, imagen y patología? Si no, ¿qué falta?
- 5 Estadificación: Asignación de estadio según AJCC y/o MSTS.
- 6 Opciones terapéuticas: Discusión de todas las opciones razonables con sus riesgos/beneficios.
- 7 Recomendación consensuada: Plan de tratamiento específico, secuencia, alternativas.
- 8 Comunicación al paciente: Plan para comunicar recomendaciones y obtener consentimiento informado.
- 9 Seguimiento: Plan de seguimiento específico según diagnóstico y tratamiento.
Documentación esencial en la historia clínica oncológica
- • Informe de imagen completo: Con descripción sistemática y conclusiones.
- • Informe de patología detallado: Incluyendo diagnóstico, grado, márgenes, estudios especiales.
- • Acta de comité de tumores: Con recomendaciones específicas y justificación.
- • Consentimiento informado: Documentando opciones discutidas y decisión del paciente.
- • Plan de tratamiento: Secuencia clara de intervenciones, cronograma, objetivos.
- • Plan de seguimiento: Frecuencia de controles, estudios a realizar, signos de alarma.
CRITERIOS DE CALIDAD EN EL DIAGNÓSTICO ONCOLÓGICO MUSCULOESQUELÉTICO:
- • Tiempo diagnóstico: <4 semanas desde sospecha inicial hasta diagnóstico completo.
- • Correlación completa: 100% de casos con concordancia clínico-radiológico-patológica documentada.
- • Biopsia planificada: 100% de biopsias realizadas por o en consulta con cirujano definitivo.
- • Revisión multidisciplinaria: 100% de casos malignos discutidos en comité antes de tratamiento.
- • Documentación completa: 100% de historias con todos los elementos esenciales.
Resumen para la práctica clínica
Indicaciones
- ✓ Lesión ósea sospechosa (dolor persistente, hallazgo agresivo en RX, masa de partes blandas asociada).
- ✓ Masa de tejidos blandos ≥5 cm o profunda a la fascia (derivación a centro especializado).
- ✓ Paciente >40 años con lesión lítica solitaria (metástasis/mieloma hasta demostrar lo contrario).
- ✓ Necesidad de biopsia diagnóstica tras completar imagen local y estadificación según el caso.
Técnica
- 🔧 Primera línea: RX (hueso) y/o ecografía (tejido blando superficial) según presentación.
- 🔧 Lesión agresiva o diagnóstico incierto: RM local con contraste para extensión y planificación.
- 🔧 TC para matriz/cortical y para tórax en estadificación (metástasis pulmonares).
- 🔧 Gammagrafía ósea o PET/TC para búsqueda de multifocalidad/enfermedad sistémica cuando esté indicado.
- 🔧 Biopsia como último paso: trayecto resecable, guiada por imagen, coordinada con el equipo definitivo.
Riesgos
- ⚠️ Biopsia mal planificada: contaminación de compartimentos, complicaciones, empeoramiento del pronóstico funcional.
- ⚠️ Subestimar masas de partes blandas (≥5 cm o profundas) y retrasar derivación.
- ⚠️ Asumir primario óseo en >40 años sin descartar metástasis/mieloma.
- ⚠️ Discordancia clínico-radiológico-patológica no resuelta antes de tratar.
Resultados
- ✅ Enfoque secuencial (clínica → imagen → estadificación → biopsia planificada) mejora precisión diagnóstica.
- ✅ La derivación precoz a unidades especializadas reduce biopsias inapropiadas y optimiza resultados.
- ✅ La integración en comité (cirugía, radiología, anatomía patológica, oncología) es clave en sospecha de malignidad.
Bibliografía actualizada
Soft Tissue and Bone Tumours. 5th ed. IARC; 2020.
Imaging of Soft Tissue Tumors. (ediciones actuales).
Bone and Joint Imaging. (ediciones actuales).
Bone and Soft Tissue Tumors. 2nd ed. Springer; 1999.
Cancer Staging Manual. (edición vigente).
Sarcomas, bone metastases, CUP.
Estrategias diagnósticas integradas
El objetivo de esta página no es sustituir las fichas específicas, sino ofrecer una secuencia diagnóstica segura: reconocer la puerta de entrada correcta, estimar agresividad, completar la imagen en el orden adecuado y planificar la biopsia sin comprometer el tratamiento definitivo.
