... Tratamiento Quirúrgico ...
Técnica quirúrgica desde el punto de vista oncológico
Criterios básicos de la técnica quirúrgica
Elección del tratamiento quirúrgico
Salvamento de extremidad y técnicas de reconstrucción
Indicaciones terapéuticas relativas a la clasificación por estadios
El tratamiento de los tumores del sistema músculo esquelético debe ser multidisciplinar, colaborando con el radiólogo, oncólogo, quimioterapeuta e histopatólogo. La programación se debe basar en un diagnóstico preciso tanto radiográfico como histológico, conocimiento de los aspectos anatomopatológicos macroscópicos preoperatorios, conocimiento de las características biológicas del tumor y de las posibilidades pronosticas así como de una eventual quimioterapia y radioterapia. Si se prevé radioterapia no se deberán implantar injertos óseos por el riesgo de infección y falta de arraigamiento de los injertos. En ocasiones el cirujano ortopédico debe recurrir a otros cirujanos especializados (cirujanos vasculares, torácicos, neurocirujano, etc.). La cirugía de los tumores es compleja porque debe ser adoptada y, a veces, "inventada" caso por caso y porque a veces son intervenciones extenuantes tanto para el paciente como para el cirujano. Una terapéutica correcta de los tumores del aparato locomotor sólo puede
ser llevada a cabo válidamente en centros especializados. Implica una
educación y una política sanitaria nacional dirigidas a procurar que el
paciente, ante la primera sospecha diagnóstica, pueda ser enviado a uno de
estos centros. Si los primeros controles diagnósticos y las primeras
elecciones terapéuticas no son correctos, el resultado del tratamiento y la
herida del paciente pueden encontrarse comprometidos. Tipos de cirugía
Objetivos
Técnica quirúrgica desde el punto de vista oncológico (Enneking, 1983)
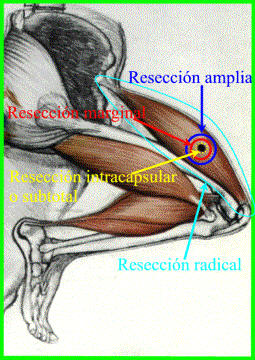
1) Cirugía intralesional o intracapsular (curetaje)El plano de disección de la resección entra en el propio tumor (por ejemplo curetaje). El tumor se extrae en fragmentos del interior de la cápsula y pseudocápsula y quedan parte de la lesión de una zona reactiva que contiene satélites y segmentos no extirpados de la lesión en el tejido vecino. Sólo está indicado en tumores histológicamente benignos en la valoración a priori. Siempre se mantiene la enfermedad microscópica residual. 2) Cirugía marginal (extracapsular o subtotal)El plano de disección es extracapsular. Se extirpa el tumor entero e intacto en bloque a través del plano de clivaje entre la cápsula o pseudocápsula del tumor y la zona reactiva o dentro de la misma. Quedan las porciones residuales de zona reactiva que contiene satélites, y tejidos blandos no atacados. Se usa en tumores benignos de partes blandas y en tumores benignos localmente agresivos de hueso. Se usa en sarcomas de partes blandas con buen plano de delimitación de la zona reactiva periférica tumoral. En los casos de tumores malignos, aunque sea de bajo grado, existe la posibilidad de implantes marginales de los bordes de la resección y “skip” metástasis. 3) Cirugía de resección amplia (Borde ancho)El plano de disección queda fuera de la zona reactiva, dentro del tejido normal. Consiste en una resección en bloque del tumor con un margen de tejidos sanos sin tocar, en ningún caso, la pseudocápsula tumoral, aunque el plano de disección transcurra por el mismo compartimento anatómico que afecta el tumor. Se trata de una técnica INTRACOMPARTIMENTAL. No existen barreras naturales entre la lesión y el borde. La planificación anatómica debe ser cuidadosa para asegurar márgenes de tejidos indemnes. Se utiliza en tumores de hueso localmente agresivos y sarcomas de baja gradación. Existe la posibilidad de dejar metástasis por escape (skip metástasis),
aunque es poco frecuente y casi exclusivamente en los tumores de grado de
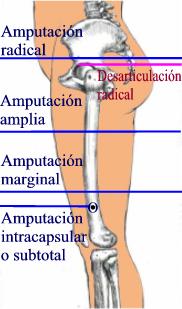
malignidad elevado. 4) Cirugía radicalCuando el plano de disección pasa por fuera del compartimento afecto. Se extirpa en bloque todo el compartimento junto con el tumor. Es una cirugía EXTRACOMPARTIMENTAL. y no es sinónimo de amputación o desarticulación. Con esta cirugía hay ausencia de enfermedad residual. Los tipos de cirugía 1 y 2 no son aceptables en ningún tumor óseo maligno. Sólo 3 y 4 son posibles en este tipo de tumores. Como se puede observar, la definición no depende del grosor de de la funda de tejido sano extraído: una intervención puede ser "radical" y tener un grosor de dos centímetros, y otra (por ejemplo, la exéresis de un tumor en el fémur) puede ser "amplia" y tener un grosor mayor. La "calidad" de la funda es más importante que su grosor: una aponeurosis de envoltura muscular o una cápsula articular, cuyo grosor es de 1 o 2 mm, tienen probablemente un valor superior que 4 o 5 mm de tejido adiposo en el canal medular o en los espacios extracompartimentales o, incluso, de tejido reactivo. Además, la definición tampoco depende del hecho que la intervención sea conservadora o mutilante: una amputación puede ser marginal o incluso intralesional si el bisturí pasa a ras del tumor o lo incide, una escapulectomía o la resección de todo el fémur pueden ser radicales (Tabla I). Si durante la intervención sucede que se pone al descubierto, se rasga o se lesiona el tejido tumoral, se contamina el campo operatorio y se expone a todos los tejidos vecinos al riesgo de una recidiva local. Si estos tejidos no son retirados, se considera que la intervención es intralesional y si se retiran, la intervención es amplía o radical pero contaminada. Para definir la intervención quirúrgica, es preciso realizar un examen macroscópico y microscópicos de la pieza resecada. Este examen debe ejecutarse simultáneamente por el cirujano y el patólogo. En efecto, solamente el cirujano conoce los puntos anatómicos por donde ha cortando a ras del tumor. Estos puntos sospechosos deberán ser marcados con tinta china y, a continuación, seccionados perpendicularmente a sus superficie para la histología. A partir de los cortes histológicos, la resección se denomina amplía si existe una capa de tejido normal entre el humor y la tinta china. Es marginal sólo está la pseudocápsula entre el tumor y la zona marcada con tinta china; es intralesional si no hay nada. Esta definición de la calidad oncológica de las exéresis es esencial y al que sin ella no se pueden evaluar los resultados del tratamiento, no se pueden comparar series diferentes y, en definitiva no se puede aprender nada para progresar en esta cirugía. |
Tabla I: Márgenes quirúrgicos. |
||
| Definición | Intervención conservadora | Amputación |
| Intralesional | Curetaje o exéresis"por fragmentos" | Amputación con sección a través del tumor |
| Marginal | Resección marginal | Amputación con sección rozando el tumor |
| Amplia | Resección amplia | Amputación amplia a través del hueso |
| Radical | Resección local radical | Desarticulación o amputación radical |
| Reproducido de Enneking WF: Musculoskeletal Tumor Surgery. New York, NY, Churchill Livingstone, 1983, p 91. | ||
Criterios básicos de la técnica quirúrgicaNo se usa isquemia a menos que sea imprescindible por la posibilidad de provocar émbolos tumorales y con ello metástasis. Controlar sistemáticamente el paquete vasculonervioso principal de la extremidad próximo al tumor a desecar. Los márgenes de resección para un tumor óseo maligno de alto grado son de 5 cm por encima y por debajo del último nivel medular detectado por TAC o RM, a excepción de las articulaciones y el cartílago articular que suponen una barrera anatómica. La tumoración de partes blandas se reseca a distancia, extirpando el máximo margen de seguridad posible. Estadios quirúrgicosVea Estadios quirúrgicos de los tumores del sistema ME Clasificación basada en:
Mediante los estudios citados previamente se determina:
Es básico la valoración de los tegumentos. Valorar la respuesta de un volumen tumoral y afectación de la circulación complementaria posterior al tratamiento quimioterápico. Elección del tratamiento quirúrgicoUna vez realizado el diagnóstico de extensión del tumor podemos definirlo como resecable o no resecable.
1) propios de las características locales del tumor.
2) según a la localización anatómica del tumor.
3) según la edad.
4) recidivas sobre cirugía previa.
5) fractura patológica.
6) indicaciones derivadas de complicaciones de la evolución local de un tumor en tratamiento.
7) imposibilidad de reconstrucción.Cirugía de preservación de la extremidadDiscusiónEn este campo ha habido un gran avance debido a la quimioterapia preoperatoria y los mejores métodos de diagnóstico que permite mayor número de intervenciones quirúrgicas de salvamento. El interés despertado por esta técnica es debido a que diversos estudios han demostrado que no existen grandes diferencias en la supervivencia y la tasa de recurrencia local de los enfermos tratados con cirugía de preservación y amputación. Los tumores pélvicos malignos continua siendo un reto importante. Los mejores resultados se obtienen cuando se puede garantizar un margen amplio y mantener o reconstruir la continuidad sacrofemoral. En general los pacientes prefieren un procedimiento de salvamento del miembro a una amputación. En un estudio se
demostró que los pacientes que habían tenido una artrodesis realizaron
trabajos más exigentes, pero tenían dificultad para sentarse y su estado
emocional, aun siendo bueno, no era tanto como los que habían tenido la
artroplastia, pero mejor que lo que habían sufrido una amputación. Criterios básicos.La resección del tumor debe ser cuidadosa sin comprometer significativamente el planteamiento oncológico, para conseguir una tasa de recidiva y supervivencia comparable a la cirugía ablativa. La funcionalidad tras la reconstrucción de la extremidad debe ser mejor que con la amputación. Indicaciones.La mayoría de tumores en estadio IA y IIA, y algunos IB.
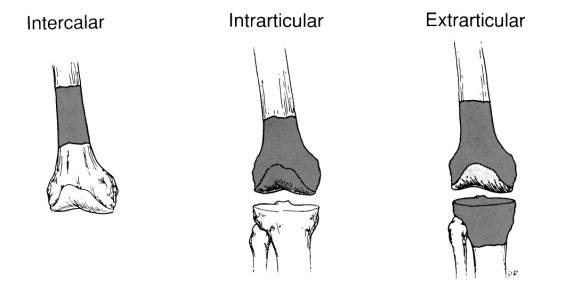
Técnica y alternativas de reconstrucción.Generalmente supone la resección en bloque del tumor óseo con un manguito de tejido normal a su alrededor. En la mayoría de los casos se realiza una biopsia incisional entes de la resección. Esta incisión también debe ser resecada en este acto quirúrgico. Las incisiones cutáneas se planean de manera que permitan el acceso a estructuras neurovasculares principales y que incluyan el trayecto de la biopsia. Después de crear los colgajos cutáneos, se disecan y aíslan cuidadosamente las estructuras neurovasculares lejos de la zona de resección, realizando la disección final por tejido normal y a distancia de la zona reactiva del tumor. El tamaño óptimo del manguito de partes blandas a resecar y su distancia al tumor es un tema controvertido, pero debe aumentarse en las áreas en que haya afectación extraósea. Después de la disección de partes blandas debe seleccionarse el nivel de resección ósea proximal y distal al tumor, basados en cálculos obtenidos de la TAC y la RM, y por medio de referencias conocidas como una articulación. Hay tres tipos de resección para los sarcomas óseos (Figura 2)
Si el tumor afecta a la
diáfisis se realiza una resección intercalar. Cuando el tumor afecta a la
metáfisis y ocasionalmente invade al articulación, se realiza una
osteotomía de la diáfisis y posteriormente una resección intraarticular o
extraarticular, desconociendo el margen aceptable de tejido óseo a resecar.
se considera adecuado un margen de 4 cm. de tejido óseo incluido en la
pieza. Si el tumor invade la articulación se realiza una resección
extraarticular. En todos los casos la pieza es disecada con un manguito de
tejidos blandos y posteriormente se completará la resección que proceda.
Aun no esta claro cual es la mejor técnica, el mejor material, y el mejor método de fijación. En la elección influyen la localización las preferencias del paciente y la experiencia del cirujano. Las resecciones intercalares son las más sencillas. Cuando se afecta la articulación la técnica más duradera es la artrodesis. Los aloinjertos tienen la ventaja de ausencia de morbilidad en la zona dadora, la posibilidad de obtener un injerto de forma y tamaño adecuado al defecto creado y la posibilidad de reinsertar tendones y ligamentos. Sin embargo presentan como desventajas la disponibilidad limitada, periodo prolongado de consolidación, potencial contagio de enfermedades, la posibilidad de rechazo, el desarrollo de fracturas por fatiga y una tasa de infección situada entre el 10-15%. La reconstrucción ósea debe seguirse con una reconstrucción de partes blandas, tales como la reinserción de los músculos y tendones o las transferencias tendinosas. En estos casos es obvio que los aloinjertos segmentarios ofrecen ventajas a los dispositivos metálicos. Otro punto a tener en cuenta es la cobertura cutánea de la reconstrucción esquelética, debiendo usarse, si hay dudas de la viabilidad, colgajos musculares de transposición con o sin injertos cutáneos. Problemas en el salvamento de las extremidades.
Complicaciones precoces. Pueden llegar a ser del 30%. Estas complicaciones se pueden paliar con la mejora de la técnica quirúrgica, el empleo más agresivo de los colgajos musculares, libres y de rotación en el momento de la resección y al cuidado postoperatorio de la necrosis de la herida.
Complicaciones tardías. Están relacionadas con la duración de la reconstrucción y a recidivas locales. Aunque la tasa de recidiva podría disminuir con una mejor gradación y una mayor experiencia con las técnicas, las complicaciones tardías de estas reconstrucciones probablemente se incrementaran al aumentar la supervivencia de estos pacientes.
Amputación-desarticulación
Indicaciones terapéuticas relativas a la clasificación por estadios
Para cada estadio tumoral, cada una de las diferentes intervenciones quirúrgicas comporta un riesgo de recidivas local que va del 0 al 100%. La indicación de tener en cuenta, en primer lugar, este riesgo de recidivas local sin olvidar que, en los tumores, grado elevado de malignidad la recidivas local aumentar en gran medida el riesgo de metástasis. Además, la indicación de tener en cuenta la edad, la función subsiguiente después de la intervención, el trabajo y las costumbres habituales del paciente. Finalmente, la y indicación quirúrgica depende también de las terapias coadyuvantes locales y generales. El método de Enneking consiste en evaluar las indicaciones quirúrgicas según el estadio del tumor y al riesgo de recidiva.
Figura 2: Tipos básicos de resecciones óseas para los sarcomas de hueso |