Inmunoterapia y medicina de precisión en tumores musculoesqueléticos
En tumores óseos y de partes blandas, la cirugía y la radioterapia siguen siendo pilares del control local, y el tratamiento sistémico se selecciona por subtipo y riesgo. La inmunoterapia y la medicina de precisión no son “universales” en sarcomas, pero son críticas en escenarios seleccionados: biomarcadores accionables, tumores con alteraciones diana, enfermedad avanzada/refractaria y ensayos clínicos.
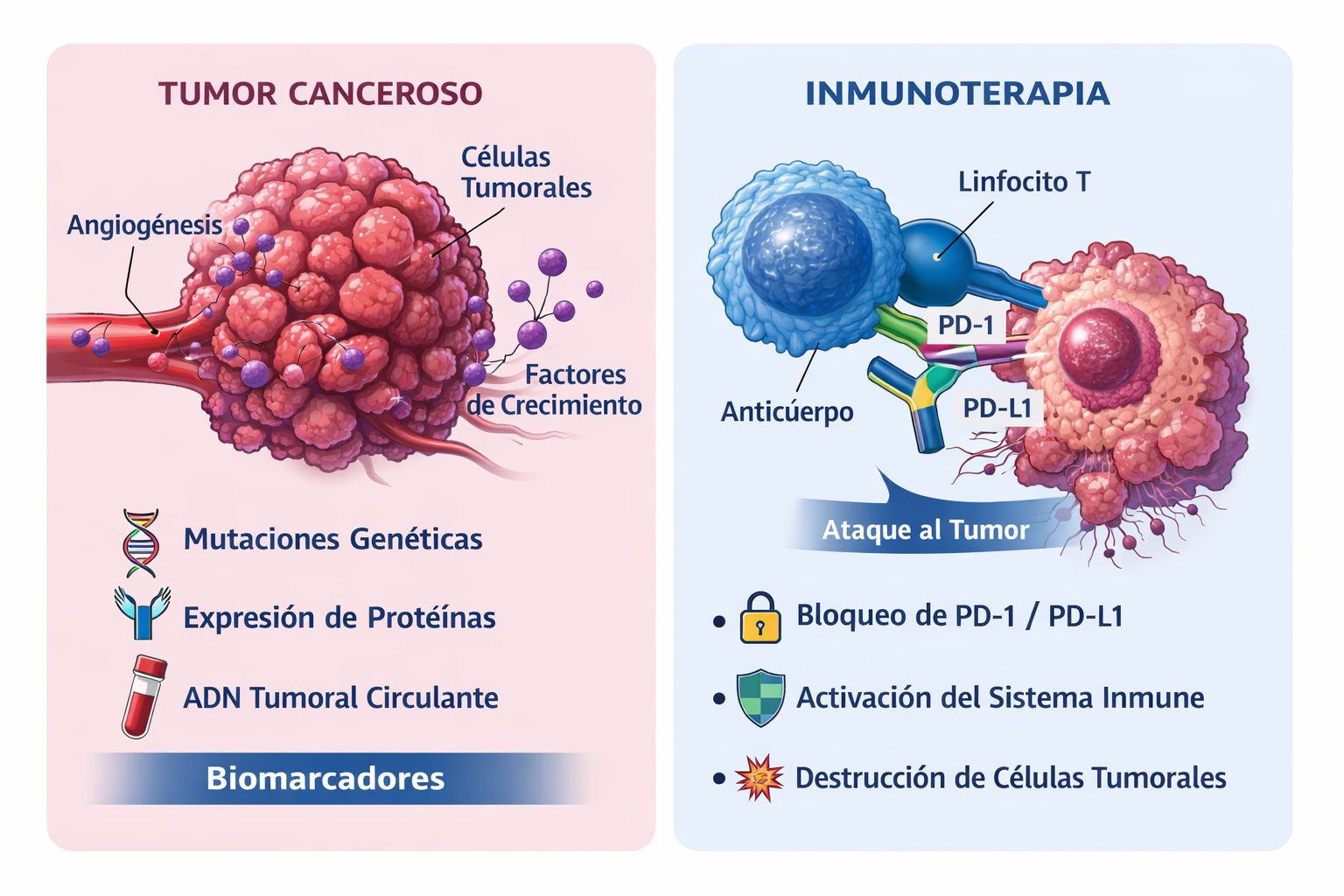
Idea clave: en “precisión” manda la selección: pedir lo adecuado, en el momento adecuado, con muestra adecuada, y traducirlo a decisiones (tratamiento/ensayo) en comité.
Cuándo pedir biomarcadores y/o NGS
No se trata de “hacer NGS a todo” por defecto, sino de optimizar rendimiento clínico (tratamiento/ensayo/clarificación diagnóstica). Un esquema pragmático:
Indicaciones frecuentes (prácticas)
- ✓ Enfermedad avanzada, metastásica o refractaria (cuando se agotan líneas estándar o el beneficio marginal es bajo).
- ✓ Subtipo raro o con alta probabilidad de alteración diana (tumores “fusion-driven”, entidades poco frecuentes, fenotipo atípico).
- ✓ Diagnóstico complejo (duda entre entidades, necesidad de confirmación molecular).
- ✓ Derivación a centro de referencia / comité molecular (para matching a ensayos).
Cuándo priorizarlo (timing)
- ⚡ Si la decisión terapéutica depende del biomarcador (acceso a fármacos diana o ensayo).
- ⚡ Si vas a necesitar muestra adicional (anticipar para evitar rebiopsias “a destiempo”).
- ⚠️ Si hay riesgo de “muestra pobre” (necrosis, poco tumor): planificar con Anatomía Patológica y Radiología/Trauma.
Regla práctica: si el resultado no va a cambiar manejo (tratamiento o ensayo) y hay limitación de tejido/coste, no lo priorices.
Muestra: lo que hace que el informe “sirva” o “no sirva”
Requisitos habituales (conceptual)
- ✓ Contenido tumoral suficiente y fijación/procesado adecuados.
- ✓ Evitar necrosis y priorizar áreas viables (coordinación con Radiología/Patología).
- ⚡ Si el objetivo es “fusiones”, asegurar que la plataforma lo cubre (NGS DNA/RNA según caso).
- ⚡ Custodia de bloque/laminillas y trazabilidad (para segundas opiniones y ensayos).
Errores típicos
- ⚠️ Pedir panel amplio sobre muestra mínima → informe “no concluyente” / “no evaluable”.
- ⚠️ No planificar rebiopsia cuando cambia la biología (progresión, post-tratamiento).
- ⚠️ No alinear la pregunta clínica con la prueba (p. ej., buscar fusiones con test que no las detecta).
Biomarcadores “clave” (mapa mental)
En precisión conviven biomarcadores “tumor-agnostic” (válidos en múltiples tumores) y biomarcadores “subtipo-específicos”. Este cuadro es deliberadamente práctico:
| Biomarcador | Qué aporta | Salida clínica típica |
|---|---|---|
| Alteración diana (mutación/amplificación) | Predice sensibilidad a fármacos dirigidos en escenarios concretos | Selección de TKI/targeted o acceso a ensayo |
| Fusiones (genes de fusión) | Puede definir entidad y/o abrir opción terapéutica | Confirmación diagnóstica + “matching” a terapia/ensayo |
| MSI-H / dMMR | Marcador “tumor-agnostic” asociado a respuesta en inmunoterapia en varios tumores | Candidato a inmunoterapia según contexto y elegibilidad |
| TMB alto (según plataforma) | Biomarcador imperfecto; puede orientar en escenarios concretos | Consideración de inmunoterapia/ensayo, no automático |
| PD-L1 | Valor predictivo variable por tumor/subtipo | Apoyo contextual (no “llave maestra” en sarcomas) |
| Firma molecular / clasificación | Refuerza o redefine diagnóstico (cuando histología es ambigua) | Cambio de estrategia terapéutica por entidad correcta |
Importante: un biomarcador sin “acción” (fármaco/ensayo disponible) puede ser útil para diagnóstico, pero su valor terapéutico inmediato puede ser limitado.
Inmunoterapia: cómo pensarla en sarcomas (sin humo)
Qué sí
- ✓ Considerarla en escenarios seleccionados, especialmente si hay biomarcadores relevantes o contexto de ensayo.
- ✓ Integrarla con el plan global (control local, síntomas, líneas previas, comorbilidades).
- ✓ Control estricto de toxicidades inmunomediadas (ver bloque de toxicidad).
Qué no
- ⚠️ No asumir que “sarcoma = responde” o que PD-L1/TMB por sí solos garantizan beneficio.
- ⚠️ No usarla como sustituto de cirugía/RT cuando hay opción curativa local.
- ⚠️ No obviar contraindicaciones relativas o riesgo alto de eventos inmunes graves sin plan de vigilancia.
Rol típico: enfermedad avanzada/refractaria + biomarcadores/ensayo + decisión en comité multidisciplinar (idealmente con soporte de comité molecular).
Terapia de precisión: objetivos “accionables” y estrategia
La terapia de precisión se apoya en detectar alteraciones “accionables” y decidir si existe fármaco con evidencia suficiente o ensayo apropiado. En musculoesquelético esto suele implicar: fusiones, vías diana, y subtipos con tratamientos dirigidos conocidos.
Qué priorizar en el informe
- ✓ Alteración + nivel de evidencia (si la plataforma lo reporta).
- ✓ Cobertura de fusiones (DNA/RNA) y limitaciones técnicas.
- ⚡ Recomendación de “matching” a ensayos si no hay opción estándar robusta.
Cómo aterrizarlo
- 🧑⚕️ Discusión en comité (idealmente con Patología + Oncología + Radiología + Cirugía).
- 🧪 Identificar centros/ensayos activos y criterios de inclusión (biomarcador + situación clínica).
- ⚠️ Evitar sobreinterpretación de variantes de significado incierto.
Ensayos clínicos: dónde realmente “pasa” la innovación
En sarcomas, una parte significativa de acceso a innovación (inmunoterapia combinada, nuevas dianas, ADC, terapias celulares, etc.) ocurre en ensayos. La medicina de precisión suele ser el “puente” para entrar.
- ✓ Matching: biomarcador + subtipo + líneas previas + estado funcional.
- ✓ Logística: disponibilidad de muestra, tiempos, documentación, consentimiento, y derivación.
- ⚡ Rebiopsia si el ensayo la exige o si la biología ha cambiado.
Consejo práctico: documenta siempre “qué se ha pedido” (plataforma) y “qué cubre/no cubre”, para evitar repetir pruebas inútiles.
Toxicidad: lo que hay que vigilar (visión de seguridad)
Inmunoterapia (eventos inmunomediados)
- ⚠️ Piel, GI, hígado, endocrino, pulmón, riñón, neuro (variable por fármaco/combinación).
- 🧪 Necesidad de protocolos de detección precoz y manejo escalonado.
- 🚨 Banderas rojas: disnea nueva, diarrea intensa, ictericia, cefalea severa, debilidad progresiva.
Terapias dirigidas
- ⚡ TKI: HTA, diarrea, mano-pie, hepatotoxicidad, fatiga.
- 🧪 Monitorización analítica y educación del paciente (adherencia y señales de alarma).
- ⚠️ Interacciones farmacológicas: revisar siempre medicación concomitante.
Principio de seguridad: cuanto más “innovador” el tratamiento, más importante es el circuito de seguimiento y la coordinación asistencial.
Algoritmo práctico (resumen operativo)
| Paso | Pregunta | Acción |
|---|---|---|
| 1 | ¿Hay intención curativa local? | Prioriza control local (cirugía/RT) y planifica biomarcadores si condicionan adyuvancia/ensayo |
| 2 | ¿Avanzado / refractario / raro / duda diagnóstica? | Plantea NGS/biomarcadores + comité (idealmente molecular) |
| 3 | ¿Muestra adecuada? | Coordina con Patología; si no, planifica rebiopsia (evita “no evaluable”) |
| 4 | ¿Alteración accionable o biomarcador relevante? | Valora terapia dirigida / inmunoterapia en contexto apropiado o ensayo |
| 5 | ¿Hay ensayo disponible y el paciente es elegible? | Derivación y matching con documentación completa (muestra, informes, staging) |
Accesos directos
Resumen práctico
Indicaciones
- Orientar el uso razonable de biomarcadores/NGS en tumores óseos y sarcomas de partes blandas.
- Estructurar la toma de decisiones sobre inmunoterapia/terapias de precisión en escenarios seleccionados.
- Mejorar la derivación y el matching a ensayos clínicos (comité molecular cuando exista).
Técnica
- Definir pregunta clínica: diagnóstico, opción terapéutica, o ensayo.
- Asegurar muestra adecuada (contenido tumoral y plataforma apropiada: DNA/RNA según objetivo).
- Interpretar resultados con nivel de evidencia y limitaciones técnicas; decidir en comité.
- Vigilar seguridad: protocolos de toxicidad inmunomediada y de terapias dirigidas.
Riesgos y complicaciones
- Informes no evaluables por mala muestra o por elegir la prueba inadecuada para la pregunta clínica.
- Sobreinterpretación de hallazgos de baja evidencia (variantes inciertas) y decisiones erróneas.
- Toxicidades relevantes sin circuito de vigilancia y actuación precoz (especialmente inmunoterapia).
- Pérdida de oportunidad de ensayo por retraso en biomarcadores o falta de documentación.
Qué esperar del resultado
- Mejor selección de pacientes para tratamientos dirigidos o inmunoterapia cuando procede.
- Optimización del acceso a ensayos clínicos y a innovación terapéutica.
- Plan coherente y seguro integrado en la estrategia multimodal.
Resumen para la práctica clínica
📌 Indicaciones
- ✓ Orientar el uso razonable de biomarcadores/NGS en tumores óseos y sarcomas de partes blandas.
- ✓ Estructurar la toma de decisiones sobre inmunoterapia/terapias de precisión en escenarios seleccionados.
- ✓ Mejorar la derivación y el matching a ensayos clínicos (comité molecular cuando exista).
🔧 Técnica
- 🔧 Definir pregunta clínica: diagnóstico, opción terapéutica, o ensayo.
- 🔧 Asegurar muestra adecuada (contenido tumoral y plataforma apropiada: DNA/RNA según objetivo).
- 🔧 Interpretar resultados con nivel de evidencia y limitaciones técnicas; decidir en comité.
- 🔧 Vigilar seguridad: protocolos de toxicidad inmunomediada y de terapias dirigidas.
⚠️ Riesgos
- ⚠️ Informes no evaluables por mala muestra o por elegir la prueba inadecuada para la pregunta clínica.
- ⚠️ Sobreinterpretación de hallazgos de baja evidencia (variantes inciertas) y decisiones erróneas.
- ⚠️ Toxicidades relevantes sin circuito de vigilancia y actuación precoz (especialmente inmunoterapia).
- ⚠️ Pérdida de oportunidad de ensayo por retraso en biomarcadores o falta de documentación.
✅ Resultados esperados
- ✅ Mejor selección de pacientes para tratamientos dirigidos o inmunoterapia cuando procede.
- ✅ Optimización del acceso a ensayos clínicos y a innovación terapéutica.
- ✅ Plan coherente y seguro integrado en la estrategia multimodal.
Bibliografía y fuentes recomendadas (para mantener actualizado)
Esta página es un marco práctico. Para decisiones concretas, apóyate en guías por subtipo y en circuitos de comité (incluyendo comité molecular si existe). Añade aquí la versión exacta de las guías que uses en tu servicio.
Guías clínicas (anotar versión exacta)
- NCCN Soft Tissue Sarcoma (Version X.YYYY)
- NCCN Bone Cancer (Version X.YYYY)
- ESMO Soft tissue and visceral sarcomas (actualización según año)
- ESMO Bone sarcomas (actualización según año)
Patología molecular y precisión
- Revisiones de patología molecular aplicada a sarcomas (fusiones, clasificación, pruebas).
- Artículos de “matching” a ensayos y medicina de precisión en tumores raros.
- Consensos locales de comité molecular (si los tienes).
Inmunoterapia y toxicidad
- Guías de manejo de toxicidad inmunomediada (protocolos oncológicos/servicio).
- Revisiones sobre inmunoterapia en sarcomas (por subtipos, combinaciones, biomarcadores).
Para búsqueda continua
- PubMed: “sarcoma” + “checkpoint inhibitor”, “NGS”, “fusion”, “precision oncology”.
- Revistas: Ann Oncol, Lancet Oncol, JCO, JNCCN.
- Congresos: CTOS, ASCO, ESMO, ESTRO.
Nota: donde pongas “NCCN/ESMO”, cita siempre versión/año exactos en tu web (esto evita que el contenido quede “desfasado” por defecto).
Precisión = selección + comité + seguridad
Biomarcadores · NGS · Matching · Ensayos · Toxicidad · Integración multimodal
