Radioterapia en tumores del sistema musculoesquelético — Actualización 2026: principios, indicaciones, técnicas modernas y manejo de toxicidad
La radioterapia (RT) constituye una herramienta fundamental en el tratamiento multidisciplinar de los tumores del sistema musculoesquelético. Su papel ha evolucionado desde la RT convencional bidimensional hasta técnicas de alta precisión: RT conformada 3D (3D-CRT), IMRT, VMAT, IGRT, SBRT/SABR, radioterapia adaptativa (incl. MR-guided RT) y terapia con partículas (protones; iones en centros específicos). La indicación de RT depende de la histología y radiosensibilidad tumoral, la resecabilidad quirúrgica, el estado de los márgenes, la presencia de enfermedad metastásica, el volumen tumoral, la proximidad a órganos críticos y el estado funcional del paciente. En sarcomas óseos y de partes blandas, la RT se emplea como tratamiento adyuvante (postoperatorio) para mejorar control local en márgenes comprometidos o tumores de alto riesgo, como neoadyuvante (preoperatorio) para facilitar la resección, y como tratamiento definitivo en tumores irresecables o radiosensibles. En metástasis óseas, la RT es clave para paliación del dolor, prevención de fracturas y control de compresión medular.
1) En 1 minuto
- ✅ Definición: uso médico de radiaciones ionizantes (fotones, electrones, protones, iones) con daño de ADN (directo e indirecto) y muerte celular (apoptosis, necrosis, catástrofe mitótica).
- ✅ Técnicas modernas (2026):
- 🔹 IMRT/VMAT: máxima conformación de dosis y ahorro de órganos sanos.
- 🔹 IGRT: verificación con imagen antes de cada sesión (CBCT/TC, RX, US) para precisión.
- 🔹 SBRT/SABR: altas dosis por fracción en pocas fracciones, sobre todo en metástasis/recidivas bien delimitadas.
- 🔹 RT adaptativa (incl. MR-guided): ajuste del plan a cambios anatómicos (pérdida de volumen, variaciones viscerales).
- 🔹 Protones (y iones en centros específicos): ventaja física (pico de Bragg) para ahorrar tejidos sanos en localizaciones críticas.
- ✅ Volúmenes (ICRU): GTV (macroscópico), CTV (microscópico), PTV (márgenes por incertidumbre), OAR (órganos a riesgo).
- ✅ Fraccionamiento típico:
- 🔹 Convencional: 1,8–2 Gy/día, 5 días/semana, hasta 50–70 Gy.
- 🔹 Hipofraccionado / SBRT: 5–20 Gy por fracción, 1–5 fracciones (según localización y OAR).
- ✅ Papel por histología:
- 🔹 Ewing: radiosensible. RT adyuvante o definitiva según control quirúrgico y localización.
- 🔹 Linfoma óseo / Plasmocitoma: muy radiosensibles. Papel central (local).
- 🔹 Condrosarcoma: radiorresistente (salvo mesenquimal). RT en irresecables o márgenes +; protones/alta precisión en base de cráneo.
- 🔹 Osteosarcoma: radiorresistente. RT en márgenes + no corregibles o paliación.
- 🔹 Tumor de células gigantes: RT no rutinaria; considerar en irresecables/recidivas múltiples.
- 🔹 Metástasis óseas: paliación del dolor, prevención de fractura, compresión medular; SBRT en oligometástasis seleccionadas.
- ✅ Toxicidad: aguda (radiodermitis, edema, fatiga) y tardía (fibrosis, fracturas/insuficiencia ósea, neuropatía, segundos tumores).
Pitfall: no integrar la RT en el momento adecuado del plan multidisciplinar. La RT postoperatoria suele iniciarse tras cicatrización (≈3–5 semanas) y, salvo causas justificadas, conviene evitar demoras prolongadas. La RT preoperatoria requiere coordinación con la vía de biopsia y la resección para minimizar morbilidad de herida y asegurar la inclusión de trayectos de biopsia en el campo.
2) Conceptos
1) Bases físicas y biológicas
Los efectos biológicos se producen por daño directo e indirecto al ADN (radicales libres), con muerte celular por apoptosis, necrosis o catástrofe mitótica. La radiosensibilidad varía por tipo tumoral.
- 🔹 Alta radiosensibilidad: linfomas, plasmocitoma, sarcoma de Ewing (células redondas pequeñas).
- 🔹 Intermedia: sarcomas de partes blandas (dependiente de grado y subtipo).
- 🔹 Baja: osteosarcoma y condrosarcoma convencional (salvo variantes).
2) Objetivos de la RT en tumores musculoesqueléticos
- 🔹 Curativo: definitivo (radiosensibles/irresecables), adyuvante (márgenes comprometidos), neoadyuvante (facilitar resección).
- 🔹 Paliativo: dolor, prevención de fractura, compresión medular, sangrado, control sintomático.
3) Modalidades técnicas (2026)
1) Teleterapia con fotones
- 🔹 3D-CRT: planificación tridimensional con haces conformados. En retroceso frente a IMRT/VMAT.
- 🔹 IMRT: modulación de intensidad para conformación alta y ahorro de OAR; útil en pelvis, columna, base de cráneo.
- 🔹 VMAT: IMRT en arcos; reduce tiempo y puede mejorar eficiencia con planificación equivalente.
2) IGRT
Verificación con imagen inmediatamente antes de cada fracción (p. ej., CBCT) para corregir desplazamientos. Es esencial en IMRT/VMAT y obligada en SBRT.
3) SBRT / SABR
- 🔹 Altas dosis por fracción (habitual 6–20 Gy) en 1–5 fracciones con precisión alta.
- 🔹 Indicada en oligometástasis óseas (incluida columna), recidivas locales y casos seleccionados de primarios irresecables.
- 🔹 Requiere inmovilización estricta, IGRT y respeto estricto de restricciones de médula/plexos/viscerales.
4) Partículas: protones (y iones en centros específicos)
- 🔹 Ventaja física: pico de Bragg (menos dosis de salida), útil para ahorrar OAR en anatomía compleja.
- 🔹 Indicaciones típicas: cordoma/condrosarcoma de base de cráneo, columna, pelvis seleccionada, pediatría (reducción de dosis integral).
- 🔹 Disponibilidad en España: centros privados (p. ej., Madrid) y despliegue progresivo en red pública según proyectos en marcha.
5) RT adaptativa y MR-guided RT
La RT adaptativa permite modificar el plan ante cambios anatómicos (tumor, edema, variabilidad visceral). La RT guiada por RM aporta mejor contraste de tejidos blandos y puede facilitar márgenes más ajustados en escenarios seleccionados.
4) Planificación
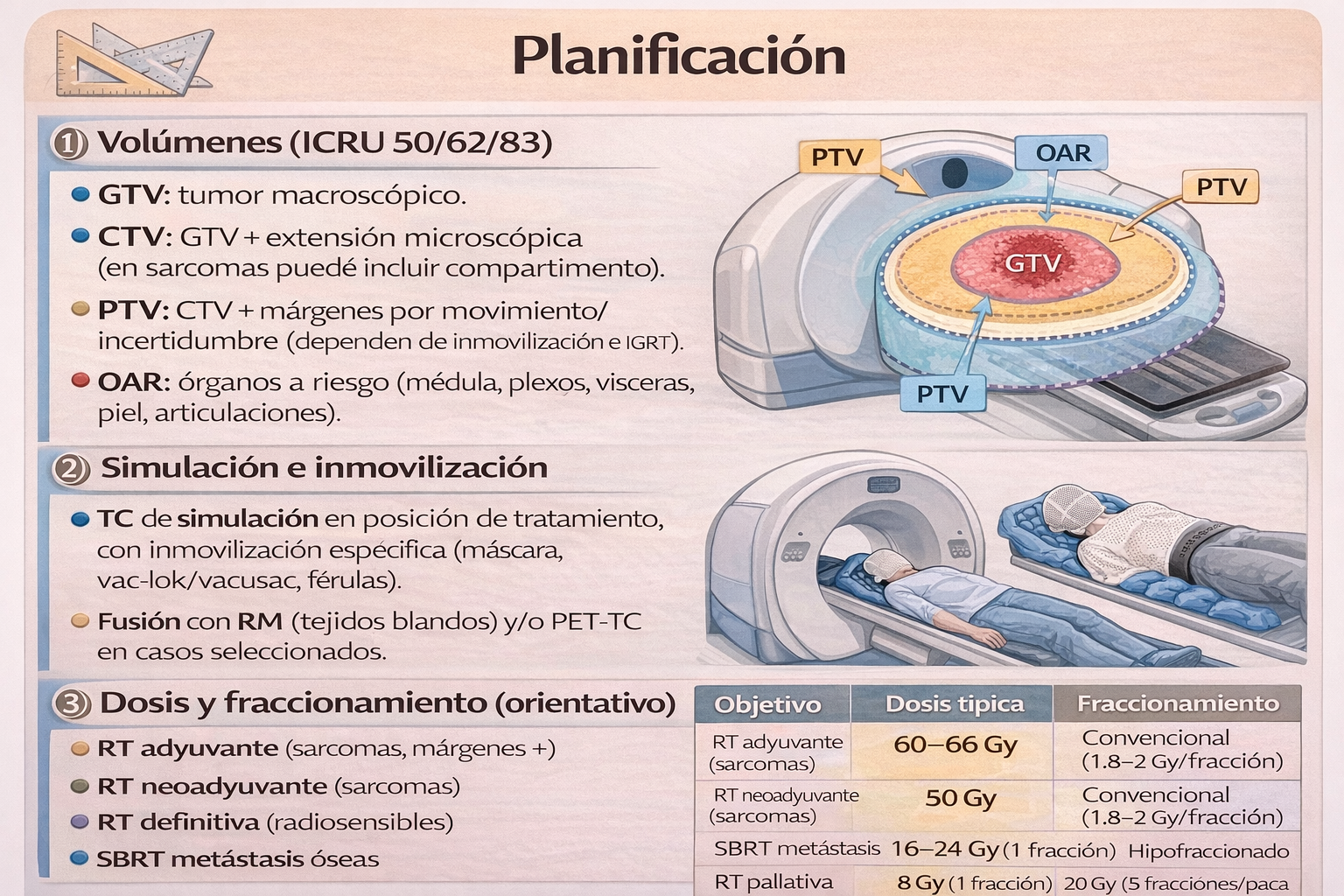
1) Volúmenes (ICRU 50/62/83)
- 🔹 GTV: tumor macroscópico.
- 🔹 CTV: GTV + extensión microscópica (en sarcomas puede incluir compartimento).
- 🔹 PTV: CTV + márgenes por movimiento/incertidumbre (dependen de inmovilización e IGRT).
- 🔹 OAR: órganos a riesgo (médula, plexos, vísceras, piel, articulaciones).
2) Simulación e inmovilización
- 🔹 TC de simulación en posición de tratamiento, con inmovilización específica (máscara, vac-lok/vacusac, férulas).
- 🔹 Fusión con RM (tejidos blandos) y/o PET-TC en casos seleccionados.
3) Dosis y fraccionamiento (orientativo)
| Objetivo | Dosis típica | Fraccionamiento |
|---|---|---|
| RT adyuvante (sarcomas, márgenes +) | 60–66 Gy | Convencional (1,8–2 Gy/fracción) |
| RT neoadyuvante (sarcomas) | 50 Gy | Convencional (1,8–2 Gy/fracción) |
| RT definitiva (radiosensibles) | 40–60 Gy | Convencional |
| SBRT metástasis óseas | 16–24 Gy (1 fracción) 24–35 Gy (3–5 fracciones) |
Hipofraccionado |
| RT paliativa (metástasis) | 8 Gy (1 fracción) 20 Gy (5 fracciones) 30 Gy (10 fracciones) |
Única o hipofraccionado |
4) Órganos de riesgo (ejemplos)
Las restricciones dependen del esquema y del órgano. A modo de ejemplo:
- 🔹 Médula espinal: en fraccionamiento convencional, Dmax típicamente ≤45–50 Gy. En SBRT, restricciones por fracción muy estrictas.
- 🔹 Plexo braquial: Dmax habitualmente ≤60–66 Gy (convencional).
- 🔹 Intestino delgado: limitar V45 y Dmax según volumen y contexto.
- 🔹 Riñones: limitar dosis media (especialmente en campos extensos).
- 🔹 Piel: controlar Dmax para reducir radiodermitis severa.
Planificavion de la radioterapia
5) Indicaciones por tipo tumoral
1) Sarcoma de Ewing
- 🔹 Radiosensibilidad: alta.
- 🔹 RT adyuvante: márgenes comprometidos o alto riesgo (p. ej., gran tamaño, mala respuesta).
- 🔹 RT definitiva: irresecables (pelvis/columna/base de cráneo) o no candidatos quirúrgicos.
- 🔹 Dosis orientativa: 45–55 Gy (boost hasta ~60 Gy si residual macroscópico según caso).
2) Linfoma óseo y plasmocitoma
- 🔹 Radiosensibilidad: muy alta.
- 🔹 RT: papel central como control local, sola o con tratamiento sistémico.
- 🔹 Dosis orientativa: 30–40 Gy (linfoma), 40–50 Gy (plasmocitoma solitario).
3) Condrosarcoma
- 🔹 Radiosensibilidad: baja (salvo mesenquimal).
- 🔹 Cirugía: tratamiento principal cuando resecable.
- 🔹 RT: irresecables o márgenes positivos; en base de cráneo se favorecen técnicas de alta precisión/partículas.
- 🔹 Dosis orientativa: 60–70 Gy (según objetivo, técnica y OAR).
4) Osteosarcoma
- 🔹 Radiosensibilidad: baja.
- 🔹 Estándar: cirugía + quimioterapia (neo/adyuvante).
- 🔹 RT: márgenes positivos no corregibles en localizaciones complejas; paliación en dolor/irresecable.
- 🔹 Dosis orientativa: 60–66 Gy (adyuvante); paliativa según síntomas.
5) Tumor de células gigantes
- 🔹 RT: excepcional (irresecable, sacro/columna, o recidivas múltiples no controlables quirúrgicamente).
- 🔹 Dosis orientativa: 45–50 Gy (convencional).
6) Metástasis óseas
- 🔹 Indicaciones: dolor, riesgo de fractura (p. ej., Mirels en huesos largos), compresión medular (urgencia), sangrado.
- 🔹 Esquemas habituales: 8 Gy x1, 20 Gy x5, 30 Gy x10 (según complejidad y objetivo). En casos seleccionados, SBRT (control local más agresivo).
- 🔹 Columna: valorar estabilidad mecánica (SINS) y compresión epidural; la combinación de cirugía de descompresión/estabilización + RT (incl. SBRT) es frecuente en escenarios seleccionados.
6) Radioterapia adyuvante (postoperatoria)
- 🔹 Indicaciones: R1/R2, márgenes cercanos, alto grado, rotura/siembra tumoral, localizaciones donde no es posible margen amplio (pelvis, columna, base de cráneo).
- 🔹 Inicio: tras cicatrización adecuada (habitual 3–5 semanas; individualizar).
- 🔹 Dosis: orientativamente 60–66 Gy sobre lecho (ajustar según riesgo y OAR).
7) Radioterapia neoadyuvante (preoperatoria)
- 🔹 Indicaciones: sarcomas de partes blandas profundos, alto grado y >5 cm; casos borderline resecables.
- 🔹 Ventajas: menor dosis total (≈50 Gy) y menor volumen irradiado; potencial reducción de toxicidad tardía.
- 🔹 Inconvenientes: mayor tasa de complicaciones de herida; coordinar cierre/colgajos si procede.
- 🔹 Cirugía: suele programarse 4–6 semanas tras finalizar RT, según evolución clínica.
8) Radioterapia definitiva
- 🔹 Indicaciones: tumores radiosensibles (linfoma/plasmocitoma), irresecables por localización o no candidatos quirúrgicos.
- 🔹 Requisitos: diagnóstico histológico, estadificación completa, técnica de alta precisión (IMRT/VMAT ± partículas).
- 🔹 Dosis: 60–70 Gy según histología y tolerancias (en radiosensibles puede ser menor).
9) Radioterapia paliativa
- 🔹 Objetivo: control sintomático y calidad de vida.
- 🔹 Esquemas: 8 Gy x1 (metástasis no complicadas), 20 Gy x5 o 30 Gy x10 (lesiones complejas o con afectación neurológica), SBRT en oligometástasis seleccionadas.
- 🔹 Respuesta: el alivio del dolor suele iniciar en días, con máximo a 2–4 semanas.
10) Complicaciones
1) Agudas
- 🔹 Radiodermitis: eritema, sequedad, descamación húmeda. Manejo: hidratación, corticoide tópico si indicado, apósitos.
- 🔹 Edema y dolor transitorio (inflamatorio).
- 🔹 Fatiga frecuente.
- 🔹 Síntomas digestivos si pelvis/abdomen; mucositis/disfagia en campos de cabeza/cuello.
2) Tardías
- 🔹 Fibrosis y rigidez con limitación funcional.
- 🔹 Compromiso óseo: insuficiencia/fragilidad, fracturas postirradiación (riesgo ↑ con dosis altas, campos amplios y factores óseos previos).
- 🔹 Neuropatía por plexopatía o lesión de nervios periféricos.
- 🔹 Linfedema (especialmente extremidades con ingle/axila).
- 🔹 Segundos tumores: riesgo bajo pero real, especialmente en jóvenes y grandes dosis/volúmenes.
- 🔹 Niños: alteraciones del crecimiento si se irradian fisis.
3) Manejo
- 🔹 Prevención: IMRT/VMAT + IGRT, márgenes adecuados, restricciones OAR.
- 🔹 Fibrosis/rigidez: fisioterapia y tratamiento sintomático.
- 🔹 Fracturas: evaluación ortopédica; estabilización cuando indicado.
- 🔹 Seguimiento prolongado en pacientes jóvenes (riesgos tardíos).
11) Algoritmo de decisión (comité multidisciplinar)
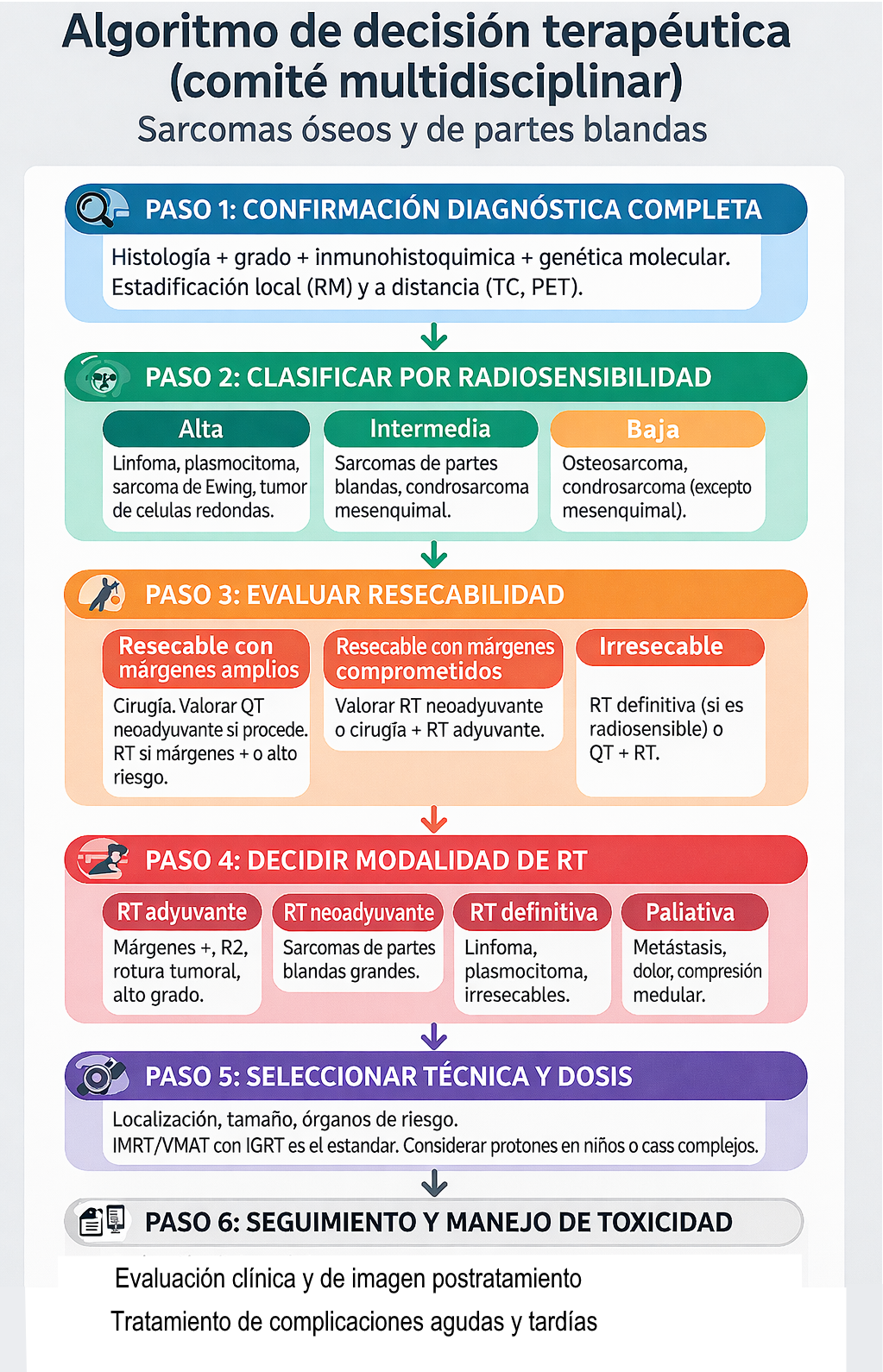
Resumen práctico
Indicaciones
- RT adyuvante (postoperatoria) en tumores de alto riesgo, márgenes positivos o recidiva local.
- RT neoadyuvante (preoperatoria) en sarcomas de partes blandas grandes/profundos para facilitar resección y reducir toxicidad tardía (a costa de mayor riesgo de herida).
- RT definitiva en tumores radiosensibles o irresecables cuando no es posible cirugía.
- RT paliativa en metástasis óseas sintomáticas (dolor, compresión medular, sangrado) y en riesgo de fractura (integrado con ortopedia).
- SBRT en oligometástasis óseas seleccionadas para control local agresivo.
Técnica
- Simulación: TC de planificación con inmovilización específica; fusión con RM/PET cuando aporta valor.
- Volúmenes: GTV/CTV/PTV y OAR según ICRU; márgenes acordes a técnica e IGRT.
- Planificación: IMRT/VMAT con IGRT como estándar; SBRT cuando procede; protones/partículas en indicaciones seleccionadas.
- Dosis: neoadyuvante típica 50 Gy; adyuvante 60–66 Gy; paliativa 8 Gy x1 o fraccionados; SBRT según localización y restricciones.
Riesgos y complicaciones
- No coordinar RT con la estrategia quirúrgica (trayecto de biopsia, cierre, colgajos) y aumentar morbilidad.
- Iniciar RT adyuvante sin cicatrización adecuada o retrasarla de forma excesiva sin motivo.
- No respetar restricciones de órganos de riesgo (médula/plexos/viscerales), especialmente en SBRT.
- Falta de IGRT en tratamientos conformados (IMRT/VMAT/SBRT).
- Seguimiento insuficiente de toxicidad tardía (fibrosis, fracturas, neuropatía, segundos tumores).
Qué esperar del resultado
- En sarcomas de extremidad, cirugía conservadora + RT consigue tasas altas de control local en la mayoría de series modernas.
- En metástasis óseas, RT logra mejoría del dolor en un porcentaje relevante de pacientes y puede reducir necesidad de analgésicos.
- En tumores radiosensibles (linfoma/plasmocitoma), la RT aporta control local elevado en enfermedad localizada.
12) Bibliografía (selección)
Guías clínicas y consensos
- 📄 Gronchi A, Miah AB, Dei Tos AP, et al. Soft tissue and visceral sarcomas: ESMO–EURACAN–GENTURIS Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021;32(11):1348–1365. doi:10.1016/j.annonc.2021.07.006
- 📄 Strauss SJ, Frezza AM, Abecassis N, et al. Bone sarcomas: ESMO–EURACAN–GENTURIS Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021;32(12):1520–1536. doi:10.1016/j.annonc.2021.08.1995
- 📄 Alcorn SR, Lutz ST, Hartsell WF, et al. External Beam Radiation Therapy for Symptomatic Bone Metastases: An ASTRO Clinical Practice Guideline. Pract Radiat Oncol. 2024;14(5):377–397. PMID:38788923
- 📄 Serrano C, Hindi N, Cruz J, et al. SEOM-GEIS clinical guideline for management of soft-tissue sarcomas (2024). Clin Transl Oncol. 2025;27(4):1460–1471. doi:10.1007/s12094-024-03842-5
- 📄 National Comprehensive Cancer Network (NCCN). NCCN Guidelines®: Soft Tissue Sarcoma. Version 1.2026. (Acceso bajo registro en NCCN).
Radioterapia perioperatoria en sarcomas de partes blandas
- 📄 O'Sullivan B, Davis AM, Turcotte R, et al. Preoperative versus postoperative radiotherapy in soft-tissue sarcoma of the limbs: a randomised trial. Lancet. 2002;359(9325):2235–2241. doi:10.1016/S0140-6736(02)09292-9
Columna, oligometástasis y SBRT
- 📄 Laufer I, Rubin DG, Lis E, et al. The NOMS framework: approach to the treatment of spinal metastatic tumors. Oncologist. 2013;18(6):744–751. doi:10.1634/theoncologist.2012-0293
- 📄 Fisher CG, DiPaola CP, Ryken TC, et al. A novel classification system for spinal instability in neoplastic disease: the Spinal Instability Neoplastic Score (SINS). Spine. 2010;35(22):E1221–E1229. doi:10.1097/BRS.0b013e3181e16ae2
- 📄 Palma DA, Olson R, Harrow S, et al. Stereotactic Ablative Radiotherapy for the Comprehensive Treatment of Oligometastatic Cancers: Long-Term Results of the SABR-COMET Phase II Randomized Trial. J Clin Oncol. 2020;38(25):2830–2838. doi:10.1200/JCO.20.00818
Partículas (protones) y tumores de base de cráneo/columna
- 📄 Combs SE, et al. ESTRO ACROP guideline: target volume definition for particle therapy in skull base chordoma and chondrosarcoma. Radiother Oncol. 2021;156:80–94. PMID:33857965
- 📄 DeLaney TF, Haas RL. Innovative radiotherapy of sarcoma: proton beam radiation. Eur J Cancer. 2016;62:112–123. PMID:27258968
- 📄 Gillies CSM, Lim P, Dunlea C, et al. Proton beam therapy in paediatric radiation oncology: defining the limitations, uncertainties and optimisation of treatment plans. EJC Paediatric Oncology. 2025;5:100242. doi:10.1016/j.ejcped.2025.100242
Complicaciones óseas tras RT
- 📄 Mascard E, Vaz G, Martin V. Prevention and treatment of post-irradiation fractures and other complications. Orthop Traumatol Surg Res. 2025;112(1 Suppl):104441. PMID:41005531
- 📄 Kao Y, Tsai C, Shen Y, et al. Osteoradionecrosis of the hip, a troublesome complication of radiation therapy: case series and systematic review. Front Med (Lausanne). 2022;9:858929. doi:10.3389/fmed.2022.858929
Clásicos de referencia (dosis paliativa)
- 📄 Chow E, Harris K, Fan G, Tsao M, Sze WM. Palliative radiotherapy trials for bone metastases: a systematic review. J Clin Oncol. 2007;25(11):1423–1436. doi:10.1200/JCO.2006.09.5281
- 📄 Hartsell WF, Scott CB, Bruner DW, et al. Randomized trial of short- versus long-course radiotherapy for palliation of painful bone metastases (RTOG 9714). J Natl Cancer Inst. 2005;97(11):798–804. doi:10.1093/jnci/dji139
Resumen para la práctica clínica
📌 Indicaciones
- ✅ RT adyuvante (postoperatoria) en tumores de alto riesgo, márgenes positivos o recidiva local.
- ✅ RT neoadyuvante (preoperatoria) en sarcomas de partes blandas grandes/profundos para facilitar resección y reducir toxicidad tardía (a costa de mayor riesgo de herida).
- ✅ RT definitiva en tumores radiosensibles o irresecables cuando no es posible cirugía.
- ✅ RT paliativa en metástasis óseas sintomáticas (dolor, compresión medular, sangrado) y en riesgo de fractura (integrado con ortopedia).
- ✅ SBRT en oligometástasis óseas seleccionadas para control local agresivo.
🔧 Técnica
- 🔧 Simulación: TC de planificación con inmovilización específica; fusión con RM/PET cuando aporta valor.
- 🔧 Volúmenes: GTV/CTV/PTV y OAR según ICRU; márgenes acordes a técnica e IGRT.
- 🔧 Planificación: IMRT/VMAT con IGRT como estándar; SBRT cuando procede; protones/partículas en indicaciones seleccionadas.
- 🔧 Dosis: neoadyuvante típica 50 Gy; adyuvante 60–66 Gy; paliativa 8 Gy x1 o fraccionados; SBRT según localización y restricciones.
⚠️ Riesgos
- ⚠️ No coordinar RT con la estrategia quirúrgica (trayecto de biopsia, cierre, colgajos) y aumentar morbilidad.
- ⚠️ Iniciar RT adyuvante sin cicatrización adecuada o retrasarla de forma excesiva sin motivo.
- ⚠️ No respetar restricciones de órganos de riesgo (médula/plexos/viscerales), especialmente en SBRT.
- ⚠️ Falta de IGRT en tratamientos conformados (IMRT/VMAT/SBRT).
- ⚠️ Seguimiento insuficiente de toxicidad tardía (fibrosis, fracturas, neuropatía, segundos tumores).
✅ Resultados
- ✅ En sarcomas de extremidad, cirugía conservadora + RT consigue tasas altas de control local en la mayoría de series modernas.
- ✅ En metástasis óseas, RT logra mejoría del dolor en un porcentaje relevante de pacientes y puede reducir necesidad de analgésicos.
- ✅ En tumores radiosensibles (linfoma/plasmocitoma), la RT aporta control local elevado en enfermedad localizada.
