... Osteosarcomas Primarios ...
Discusión
Los osteosarcomas comprenden una familia de tumores del tejido conjuntivo con diferentes grados de potencial maligno. Se caracterizan por producir osteoide óseo o tejido óseo por las células neoplásicas. Se han identificado varios subtipos de osteosarcomas.
Constituyen cerca del 20% de las neoplasias malignas primarias del hueso. Representa el 0.2% de las neoplasias malignas (alrededor de 100 nuevos casos por año en España). Se considera que suponen el 5% de los tumores de la niñez, y en estas edades, el 50 % se localizan en los huesos de la rodilla.
Afecta a los hombres en un 60% y a las mujeres en un 40%. El 58% se dan en la segunda década de la vida; y presentan una distribución bimodal con respecto a la edad, con un pico a los 17 años, y otro en la sexta década (secundario a lesiones óseas como Paget, osteocondroma, displasia fibrosa o áreas previamente irradiadas).
La mayoría de los osteosarcomas son de etiología desconocida por lo que son considerados idiopáticos o primarios. En un pequeño número se conocen factores predisponentes, como la enfermedad de Paget, los infartos óseos, displasia fibrosa, radiaciones ionizantes e ingestión de substancias radioactivas. Estas lesiones se clasifican como osteosarcomas secundarios.
Todos los tipos de osteosarcomas pueden ser subclasificados en función de el sitio anatómico, como axial o apendicular. También se pueden clasificar de acuerdo a su localización en el hueso como central (medular), intracortical, o yuxtacortical. Otro subgrupo comprende los osteosarcomas localizados en los tejidos blandos (osteosarcomas extraesqueléticos o de los tejidos blandos).
Presentación
clínica
La presentación clínica puede ser muy variada y depende del tipo de osteosarcoma, del sitio anatómico, y de la edad del paciente.
Lo más frecuente es que se presente como una masa de tejidos blandos, dolorosa. Ocasionalmente su primera manifestación es una fractura patológica. El dolor puede ser suave e intermitente al principio, pero evoluciona a constante y severo. En los tumores yuxtacorticales, la presencia de una masa dura, dolorosa, que crece lentamente, es la forma más común de presentación. Las metástasis pulmonares es la complicación más común, pero es raro en los sarcomas de la mandíbula y es una complicación tardía de los osteosarcomas multicéntricos.
Estudios
de
imagen
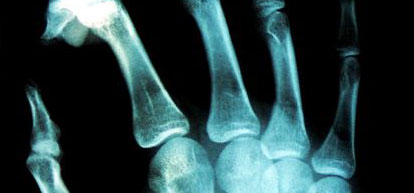
Las radiografías simples proporcionan una información adecuada para el diagnóstico. Con ellas se puede apreciar destrucción ósea y focos escleróticos de formación ósea, una reacción perióstica reactiva agresiva (sol naciente, laminar, triángulo de Codman) y una masa de tejidos blandos. La tomografía convencional puede ayudar a delimitar la matriz y la destrucción cortical y en la detección de fracturas patológicas ocultas. La arteriografía es útil para mapear el tumor, su vascularización y para la identificación del área más adecuada para la biopsia. La gammagrafía ósea puede ayudar a la localización de metástasis intraóseas y skip metástasis. La TAC y la RM son básicas para determinar la extensión intraósea y extraósea del tumor.
Histopatología
Uno de los desafíos más difíciles que se enfrenta el patólogo ocurre cuando hay insuficiente información clínica y radiográfica que puede producir ningún diagnóstico, diagnóstico falso, o un retraso en el diagnóstico hasta que el patólogo consigue los datos pertinente. La importancia de la buena comunicación entre radiólogo, cirujano, y patólogo en el diagnóstico de tumores del hueso fue resaltada por Jaffe,y permanece hoy permanece vigente.
La toma de muestras es otro problema importante enfrentado por patólogos del sistema musculoesquelético. Una zona reactiva rodea los sarcomas, y un error común cometido por cirujanos es enviar sólo material reactivo. Se están dando a los patólogos las biopsias más pequeñas y haciéndoles las preguntas más detalladas. La heterogeneidad del tumor es común, y los subtipos pueden ser difíciles, sobre todo en un espécimen pequeño. Las biopsias con aguja pueden ser muy exactas e informativas cuando se realizan por un equipo experimentado, pero no es fidedigno cuando se ejecutan por un equipo inexperto.
La medición de la respuesta. Puede haber dificultades en la medida de la respuesta al tratamiento quimioterápico. Pueden existir santuarios del tumor, dando lugar a pequeñas áreas de tumor viable. Existen datos que correlacionan esa viabilidad con los resultados de la RM dinámica, pero permanece sin ser demostrado que la RM dinámica tenga importancia para el pronostico. ¿Es difícil afrontar las áreas circunscritas de tumor viable con áreas necróticas; cómo informarlo es importante?
Los hallazgos histopatológicos varían de acuerdo al subtipo particular. Las características comunes de todos los subtipos es la presencia de osteoide o hueso neoformado por las células malignas.
Los osteosarcomas pueden ser graduados en base a su celularidad, atipia celular (pleomorfismo celular), y actividad mitótica. En general el grado numérico (1 al 4) del sistema de Broder, indica el grado de malignidad (El grado 1 indica el menos indiferenciado y el 4 el más indiferenciado) (Tabla 1). Por ejemplo, el osteosarcoma central bien diferenciado y el osteosarcoma parosteal son estimados como grado 1 y raramente como grado 2; el osteosarcoma periosteal y el osteosarcoma maxilar como grado 2, y raramente como grado 3; y el osteosarcoma convencional como grado 3 o 4. El osteosarcoma telangiectásico, los osteosarcomas desarrollados en hueso pagético, los osteosarcomas postirradiación y los osteosarcomas multifocales son generalmente tumores grado 4. Esta gradación es de importancia clínica, terapéutica y pronóstica.
TABLA 1. Grado histológico del osteosarcoma |
|
Grado |
Características histológicas |
1 |
Celularidad: ligeramente incrementada Atipia celular: mínima o ligera Actividad mitótica: baja Matriz osteoide: regular |
2 |
Celularidad: moderada Atipia celular: media o moderada Actividad mitótica: baja o moderada Matriz osteoide: regular |
3 |
Celularidad: aumentada Atipia celular: moderada a pronunciada Actividad mitótica: moderada a alta Matriz osteoide: irregular |
4 |
Celularidad: marcadamente incrementada Atipia celular: marcado pleomorfismo celular Actividad mitótica: alta Matriz osteoide: irregular, abundante |
Unni KK, Dahli DC. Grading of bone tumors. Semin Diagn Pathol 1984;1:165-172 |
|
Factores
pronósticos
Los pacientes con enfermedad localizada tienen mejor pronóstico que con la enfermedad metastásica. |
|
La localización primaria del tumor es un factor pronóstico importante. |
|
En el esqueleto axial tienen mayor riesgo de progresión y de muerte. |
|
Resecabilidad del tumor. Es el factor pronóstico más importante, ya que este tumor es muy resistente a la radioterapia. |
|
Los osteosarcomas de localización craneofacial y otros huesos planos tienen una buena supervivencia tras la cirugía del hueso afecto, y más si se asocian a la quimioterapia. |
|
Los osteosarcomas secundarios tienen el mismo pronóstico que los primarios si se tratan agresivamente con cirugía y poliquimioterapia. |
|
Otros factores pronósticos que se han nombrado son: la edad, el tamaño del tumor, las skip metástasis, los niveles de lactodeshidrogenasa, los niveles de fosfatasas alcalinas. |
|
Otros factores pronósticos potenciales, que no han sido probados con gran número de pacientes incluyen: la expresión HER2/Erb-2 (un factor humano de crecimiento epidérmico), la poliploidía de las células tumorales, la pérdida de heterozigosidad del gen RB, la pérdida de heterozigosidad del locus p53, incremento de la expresión de la p-glicoproteína, hiperexpresión de C-erb2. Ninguno de estos factores predice el resultado. |
|
El único factor que predice el resultado de forma consistente es la respuesta histopatológica del tumor a la quimioterapia preoperatoria. Los pacientes con una necrosis mayor del 95% después de la quimioterapia preoperatoria tienen un pronóstico mejor que los que obtienen menor proporción de necrosis. |
Un 20% de los pacientes tendrán metástasis perceptibles en el momento del diagnóstico, principalmente en el pulmón. El pronóstico para los pacientes con enfermedad metastásica parece estar determinado por el sitio o sitios y el número de metástasis, y por la resecabilidad quirúrgica de estas. Los pacientes que tienen una resección completa del tumor primario y de las metástasis (cuando son pulmonares), si son seguidos con quimioterapia pueden lograr supervivencias a largo plazo, aunque en conjunto el índice de supervivencia libre de enfermedad es del 20% en los pacientes con enfermedad metastásica en el momento del diagnostico. El pronóstico para la supervivencia es mejor en las metástasis unilaterales que en las bilaterales y en los pacientes con menos nódulos comparados con los que tienen muchos nódulos.
Dos ensayos se diseñaron en los años ochenta par ver la historia natural del osteosarcoma resecable de las extremidades. El resultado fue similar a otros estudios realizados en 1970; la mitad de estos pacientes desarrolló metástasis dentro de los 6 meses desde el diagnóstico, y el 80% desarrollaron recidivas dentro de los 2 años del diagnóstico. La historia natural del osteosarcoma no cambia con el tiempo y menos del 20% de los pacientes con enfermedad localizada resecable, tratada solo con cirugía, sobrevivirán libres de recaída.
Opciones
de
tratamiento
Los ensayos clínicos aleatorizados han establecido que la quimioterapia neoadyuvante y adyuvante son eficaces en la prevención de la recaída en los pacientes sin tumores metastáticos ocultos . Es indispensable que los pacientes con un osteosarcoma probado o con sospecha sean evaluados inicialmente por un oncólogo ortopédico familiarizado con el manejo quirúrgica de esta enfermedad. Esta evaluación debe ser hecha antes de a la biopsia inicial, ya que una biopsia impropiamente realizada puede arriesgar al procedimiento miembro-económico.
Osteosarcoma localizado
Los
tumores
localizados
están
limitados
al
hueso
de
origen,
aunque
las
skip
metástasis
locales
pueden
estar
presentes
dentro
del
hueso,
indicando
un
peor
pronóstico.
Aproximadamente
la
mitad
de
los
tumores
se
localizan
en
el
fémur,
con
80%
de
los
casos,
levantándose
adyacente
a
la
articulación
de
la
rodilla
en
los
pacientes
jóvenes.
Otros
sitios
primarios
en
orden
descendente
de
frecuencia
son
la
tibia,
húmero,
la
pelvis,
la
mandíbula,
el
peroné,
y
las
costillas.
Los
ensayos
clínicos
aleatorizados
han
establecido
que
la
quimioterapia
del
adyuvante
es
eficaz
en
la
prevención
de
la
recaída
o
repetición
en
los
pacientes
con
tumores
primarios
localizados
resecables.
Un
ensayo
randomizado
sugiere
que
no
hay
diferencia
en
la
supervivencia
libre
de
enfermedad
entre
cirugía
inmediata
seguida
por
quimioterapia
adyuvante
y
quimioterapia
preoperatoria.
Varios
ensayos
evaluaron
el
papel
de
la
quimioterapia
administrada
preopoeratoriamente
y
postoperatoriamente.
Algunos
de
estos
ensayos
evaluaron
la
necrosis
del
tumor
primario
después
de
la
quimioterapia
y
usaron
esta
información
para
determinar
la
terapia
subsecuente.
Los
protocolos
de
la
quimioterapia
actualmente
incluya
combinaciones
de
los
agentes
siguientes:
metotrexato
a
altas
dosis,
doxorrubicina,
ciclofosfamida,
cisplatino,
ifosfamida,
etopósido,
y
el
carboplatino.
Los
rangos
de
supervivencia
globales,
libres
de
recaída
se
sitúan
entre
50%
a
80%
en
estos
ensayos.
Uno
ensayo
randomizado
no
encontró
ninguna
diferencia
en
la
supervivencia
entre
2
drogas
dadas
para
una
duración
más
corta
y
regímenes
multiagente,
aunque
la
supervivencia
libre
de
enfermedad
en
ambos
casos
era
menor
de
50%.
El
tipo
de
cirugía
requerido
para
la
ablación
completa
del
tumor
primario
depende
de
varios
factores
que
deben
evaluarse
en
términos
individuales.
Si
se
contempla
la
cirugía
de
salvamento
(extirpación
del
tumor
maligno
del
hueso
sin
amputación
y
reemplazo
de
huesos
o
articulaciones
con
aloinjertos
o
dispositivos
protésicos),
la
biopsia
debe
realizarse
por
el
cirujano
que
hará
el
tratamiento
definitivo,
ya
que
la
situación
de
la
incisión
es
crucial,
y
se
prefiere
una
biopsia
con
aguja
a
un
biopsia
incisional
abierta.
La
rotacionplastia
y
los
procedimientos
miembro-económicos
han
sido
evaluados
para
los
resultados
funcionales
y
para
la
supervivencia.
No
hay
diferencias
en
la
supervivencia
global
entre
pacientes
tratados
por
amputación
y
los
tratados
con
un
procedimiento
miembro-económico.
Los
procedimientos
miembro-económicos
deben
ser
planeados
sólo
cuando
el
estadio
preoperatorio
indica
que
es
posible
lograr
márgenes
quirúrgicos
adecuados.
Si
el
examen
patológico
del
espécimen
quirúrgico
muestra
márgenes
inadecuados,
debe
ser
considerada
una
amputación
inmediata,
sobre
todo
si
la
respuesta
histológica
a
la
quimioterapia
preoperatoria
ha
sido
pobre.
La
quimioterapia
preoperatoria
aumenta
el
número
de
pacientes
que
pueden
recibir
un
procedimiento
miembro-económico
en
lugar
de
la
amputación.
Para
pacientes
que
reciben
quimioterapia
previa
a
la
cirugía,
el
grado
de
necrosis
tumoral
observada
postoperatoriamente
es
favorablemente
predictiva
de
la
supervivencia
libre
de
enfermedad
y
la
supervivencia
global.
En
general,
70%
a
90%
de
osteosarcomas
de
la
extremidad
puede
tratarse
por
un
procedimiento
miembro-económico
y
no
requieren
la
amputación.
La
quimioterapia
preoperatoria
(administrada
intravenosamente
o
intraarterialmente)
es
un
intento
aumentar
la
posibilidad
de
hacer
un
procedimiento
miembro-económico.
Opciones
de
tratamiento:
Las opciones de tratamiento para los osteosarcoma sin metástasis, completamente resecables de grado alto incluyen lo siguiente:
La inmensa mayoría de pacientes recibe quimioterapia preoperatoria (neoadyuvante) seguida por cirugía extirpativa (amputación, salvamento del miembro, o rotacionplastia) y quimioterapia adyuvante postoperatoria. En algunos ensayos el tipo de quimioterapia postoperatoria adyuvante es determinada por el grado de necrosis observado en el tumor primario.
-
La quimioterapia preoperatoria (sistémica o intraarterialmente) seguida por cirugía extirpativa (amputación, salvamento del miembro, o rotacionplastia). Después de la cirugía el tumor se evalúa patológicamente para ver el grado de respuesta a la quimioterapia inicial. Si el tumor ha respondido, determinado patológicamente por el grado de necrosis, se continua con el régimen de quimioterapia preoperatoria; si el tumor no ha respondido, se usa un régimen alternativo. Este abordaje no se ha evaluado en un estudio randomizado.
Para
lesiones
que
no
pueden
extirparse,
los
estudios
clínicos
se
están
dirigiendo
ahora
a
la
combinación
de
quimioterapia
intensiva
y
la
radiación
a
altas
dosis
muy
bien
localizadas.
Osteosarcoma metastásico
Osteosarcoma metastático/irresecable al diagnóstico:
La
evidencia
radiológica
de
depósitos
de
tumor
metastático
en
el
pulmón,
otros
huesos,
u
otros
sitios
distantes
se
encuentra
en
10%
a
20%
de
pacientes
al
diagnóstico;
85%
a
90%
de
la
enfermedad
metastática
está
en
los
pulmones.
El
segundo
sitio
más
común
de
metástasis
es
otro
hueso.
Las
presentaciones
con
metástasis
óseas
múltiples
conllevan
un
pronóstico
mucho
más
pobre.
En el pasado, el índice de supervivencia libre de progresión en los pacientes con osteosarcoma irresecable o metástasis era menor del 20%. Los estudios posteriores observaron un índice de supervivencia mayor del 40% en los pacientes con sólo enfermedad metastática pulmonar . El pronóstico para estos pacientes parece ser más favorable con metástasis pulmonares unilaterales que bilaterales, y para pacientes con menos nódulos y lóbulos involucrados. Los pacientes con metástasis óseas tienen un pronóstico pobre. Es necesario el tratamiento agresivo, incluyendo extirpación quirúrgica del tumor primario, y/o metástasis en el momento del diagnóstico o después de regímenes intensivos multiagentes. Todos los pacientes deben recibir quimioterapia intensiva multiagente tanto si el tumor primario o las metástasis son quirúrgicamente resecables o no.
Opciones
d
Las opciones de tratamiento que se aceptan incluyen:
Quimioterapia preoperatoria seguida por la ablación quirúrgica del tumor primario y la resección de las metástasis. Esto se sigue por poliquimioterapia postoperatoria. Los regímenes quimioterapéuticos utilizados incluyen metotrexato a altas dosis, doxorrubicina, ciclofosfamida, cisplatino, ifosfamida, etopósido, y carboplatino.
-
La ablación quirúrgica del tumor primario y metástasis dónde sea posible, seguido por poliquimioterapia. Los regímenes quimioterapéuticos utilizados en el tratamiento del osteosarcoma metastático incluye altas dosis de metotrexato, doxorrubicina, el ciclofosfamida, el cisplatino, ifosfamida, etopósido, y carboplatino.
Osteosarcoma
recurrente
La recidiva del osteosarcoma es muy común en el pulmón. Los pacientes con osteosarcoma recurrente confinados a los pulmones deben evaluarse para la resección quirúrgica, ya que a veces pueden curarse con la resección quirúrgica agresiva con o sin quimioterapia. La capacidad de lograr una resección completa de la enfermedad recurrente es el factor pronostico más importantes en la primera recaída, con una tasa de supervivencia del 20% a 40% de 3 a 5 años después de la resección completa de los tumores metastáticos pulmonares. La tasa de supervivencia a 5 años después de la resección de las metástasis pulmonares es del 23% a 31%. Los factores que sugieren un resultado bueno incluyen 4 o menos nódulos pulmonares, los metástasis pulmonares unilaterales, o intervalos largos entre la resección del tumor primario y las metástasis. El pronóstico es pobre para los pacientes con metástasis óseas que tengan osteosarcoma metastático recurrente o progresivo irresecable. El resultado de la post-recaída de pacientes que tienen una repetición local es peor que en los pacientes que recaen con metástasis solo. En un estudio de 540 pacientes con enfermedad localizada en el momento de diagnóstico, sólo 1 de 31 pacientes quién tenía enfermedad localmente recurrente estaba, a los 15 meses, libre de enfermedad después del último tratamiento, considerando que la supervivencia libre de enfermedad era del 25% para aquellos que sólo tenían metástasis. La selección del tratamiento depende de muchos factores, incluyendo el sitio de repetición, el tratamiento primario previo del paciente, y las consideraciones individuales del pacientes. La Ifosfamida con uroprotección, exclusivamente, o en combinación con etopósido, ha mostrado actividad en a uno tercio de los pacientes con osteosarcoma recurrente que no ha recibido previamente esta droga.
Efectos tardíos del Tratamiento de Tumores del Hueso
Nefrotoxicidad. El tratamiento continuado con cisplatino a altas dosis provoca que el 60% de pacientes tienen la tasas de filtración glomerular anormal pero el fracaso renal agudo y crónico es raro. El tratamiento continuo con ifosfamida, hay normalmente daño tubular en lugar del daño glomerular. La hipofostatemia ocurre en 21% de pacientes, y puede unirse a la dosis acumulativa. Los pacientes tienen riesgo de sufrir hipofostatemia durante 3 años después del tratamiento.
Ototoxicidad. Está asociado con el uso de cisplatino, e implica pérdida auditiva de alta frecuencia, que es parcialmente reversible. Está relacionada con la proporción de dosis en lugar de con la dosis cumulativa, y la toxicidad más probablemente, ocurre con los problemas de oído pre-existentes y con la exposición profesional del ruido.
Cardiotoxicidad de la Adriamicina. 20 a 50% de pacientes pueden tener anormalidades subclínicas cardíacas que pueden empeorar con el tiempo. El riesgo aumentado está asociado con las dosis más grandes, dosis cumulativa, y el sexo hembra.
Segundas neoplasias. Hay una incidencia aumentada de leucemia que puede relacionarse por el uso de agentes alquilantes. Sin embargo, permanece incierto acerca de si la leucemia es el resultado de una predisposición a la neoplasia o el resultado de la quimioterapia.
La calidad de vida. La mayoría de los estudios ha sido muy pequeños, estudios de instituciones simples. Sin embargo, la calidad de vida puede ser afectada por las terapias locales, como el fracaso mecánico de la endoprótesis. Algunos estudios han indicado que el funcionando físico es mejor para los pacientes de salvamento de miembro que para los pacientes con amputación, mientras otros no han mostrado ninguna diferencia.
En resumen hay muchas anormalidades tardías subclínicas relacionadas con la quimioterapia, pero no está cómo interactuarán con el proceso de envejecimiento normal. Se necesita más información, así como los efectos locales a largo plazo.
Problemas a largo plazo después de la cirugía
Dr. Por-Ulf Tunn de la División de Cirugía y Oncología Quirúrgico, la Universidad de Berlín, Alemania, presentó una sesión en los problemas a largo plazo después de la cirugía para el osteosarcoma.
Informó los resultados de un estudio de 78 niños tratados para el sarcoma osteogénico en una institución simple, con un abordaje multidisciplinario, desde 1970 y un seguimiento de un mínimo de 3 años. 56% sufrieron amputación y 44% salvamento del miembro; 25 pacientes tenían reconstrucción endoprotésica y 5 pacientes tenían rotacionplastia. Hubo una proporción del 7% de recidiva local en el grupo de la amputación y una proporción del 9% de recidiva local en el grupo de salvamento de miembro. Hubo una proporción del 80% de complicación en el grupo del endoprótesis, relacionado con fracturar de hueso o implante, la infección, o aflojamiento. La sordera ocurrió en 2 pacientes, las hepatitis B relacionadas con la transfusión en 1, y una segunda malignidad (cáncer de mama) en 1. Todos completaron la escuela y empezaron el entrenamiento profesional.
Referencias
National Cancer Institute