... Osteosarcomas ...
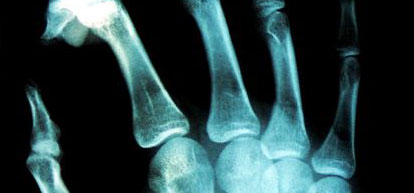
Osteosarcoma central de bajo grado (bien diferenciado)
Osteosarcoma multicéntrico (multifocal)
Osteosarcoma central
Discusión:
También conocido como osteosarcoma clásico, común, convencional.
Es el tipo más frecuente de osteosarcoma, constituyendo el 80 - 85% de todas las formas, si bien solo representa el 0,2% de todas las neoplasias malignas del hombre.
Es el tumor maligno de hueso en el que la neoformación de osteoide o hueso se produce por células tumorales y constituye un criterio de diagnóstico.
Lo más común es que el tumor maligno primario del hueso derive del mesénquima.
Su incidencia más alta se da en la segunda década de la vida, y es ligeramente mas frecuente en hombres.
Es interesante destacar que, aparentemente hay una incidencia superior de osteosarcomas en los individuos de mayor estatura.
Las complicaciones más frecuentes del osteosarcoma clásico son la fractura patológica y las metástasis pulmonares.
Sitios
afectados:
Ocurre
en
la
región
de
rodilla
(fémur
distal
o
tibia
proximal)
en
el
50%
de
pacientes.
Otros sitios incluyen húmero proximal, fémur proximal, y la pelvis. Infrecuentemente ocurre en la columna.
La
mayoría
de
los
osteosarcomas
ocurren
en
el
metáfisis.
La
placa
de
crecimiento
supone
un
barrera
Presentación
Clínica:
El síntoma inicial es el dolor en el sitio del tumor, que a menudo irradia a una articulación vecina. El dolor puede empezar insidiosamente, pero rápidamente se convierte en severo, constante y que no mejora con la inmovilización ni con los analgésicos ordinarios. Con posterioridad se aprecia una masa palpable y una limitación de la función articular vecina. En los casos avanzados aparecen el resto de signos del proceso inflamatorio. La duración de los síntomas previos al diagnóstico es variable.
Puede haber fractura patológica, pero es rara y asociada a lesiones predominantemente líticas.
Las fosfatasas alcalinas suelen estar de modera a severamente aumentadas, revelando la actividad osteoblástica del tumor, aunque no siempre hay correlación entre esta actividad y sus valores en el suero. Las fosfatasas alcalinas séricas tienen más importancia como significado pronóstico, ya que descienden después de la cirugía y vuelven a aumentar cuando aparece una recidiva local o se produce una metástasis.
Los ganglios linfáticos regionales no es frecuente su afectación, y las metástasis pulmonares pueden estar presentes en el momento dl diagnóstico.
Estudios de imagen
El osteosarcoma clásico nace en el centro (intramedularmente), penetra y destruye la cortical, levanta y traspasa el periostio e invade los tejidos vecinos.
Radiografías simples
El aspecto radiográfico varia según la edad, la localización, la rapidez de su crecimiento, la fase de crecimiento y su producción de material óseo neoplásico.
En la radiografía simple, el osteosarcoma convencional, puede mostrar destrucción medular y cortical, así como una reacción perióstica agresiva, la presencia de una masa de tejidos blandos y hueso dentro de la lesión destructiva o en la periferia, incluso dentro de la masa de tejidos blandos.
El grado de readioopacidad en el tumor refleja la combinación de la cantidad de producción ósea tumoral, la calcificación de la matriz y la sustancia osteoide, pudiendo aparecer como lesiones esclerosas puras, osteolíticas puras, y más frecuentemente una combinación de ambas. Los bordes generalmente son borrosos, con una amplia zona de transición. El tipo de destrucción ósea puede ser moteado o permeativo, y raramente geográfico. La reacción perióstica puede adoptar la forma de "sol naciente", "púas de peine" y triángulo de Codman. Menos frecuentemente adopta el tipo laminar en forma de "hojas de cebolla". También es frecuente la presencia de una masa de tejidos blandos con focos de esclerosis.
En ocasiones el osteosarcoma se extiende por el canal medular de la diáfisis, sobre todo en el húmero proximal. En otras ocasiones se ven nódulos aislados a lo largo de la diáfisis constituyendo las llamadas "skip metástasis", que en ocasiones "salta" a la articulación.
TAC
Es importante para determinar la extensión en la médula ósea.
RM
Es igual o más efectiva para la determinación de la extensión intraósea y extraósea del tumor. La RM puede demostrar el edema peritumoral, así como identificar varios componentes intratumorales, tales como áreas celulares y zonas de necrosis y licuefacción. Los componentes cartilaginosos son fácilmente distinguibles con gadolinio.
Gammagrafía
Muestra un incremento en la captación del radiotrazador y puede mostrar focos metastásicos intraóseos o lesiones multicéntricas.
Arteriografía
Raramente se usa. Es útil para mapear el tumor y para ver el abastecimiento vascular del tumor e identificar las áreas más adecuadas para la toma de la biopsia.
Histopatología
Macroscópicamente el tumor tiene aspecto parenquimatoso o encefaloide en sus zonas no osteógenas. Las zonas osteógenas son más duras y menos vascularizadas.
En el aspecto histológico el osteosarcoma se puede dividir en osteoblástico, condroblástico y fibroblástico. La apariencia del tumor refleja estos grados histológicos. El examen microscópico revela un gran pleomorfismo celular, con células grandes, fusiformes o poliédricas, polimorfismo de los nucleolos, atipias, hipercromía, y mitosis frecuentes y atípicas. Estas células pueden ser tan indiferenciadas que el estudio citológico no puede determinar si son de origen epitelial o mesenquimal, y en algunas ocasiones una variante de osteosarcoma convencional se le llama osteosarcoma epiteloide. Esta apariencia puede llevar a un incorrecto diagnóstico de metástasis de carcinoma. El material intercelular puede ser tejido osteoide, óseo, fibroso o cartilaginoso con una distribución muy anárquica. También pueden estar presentes áreas de necrosis y hemorragias.
En algunas ocasiones el osteosarcoma convencional presenta un gran número de células gigantes que producen un estroma que puede oscurecer el subyacente estroma sarcomatoso. Esta variante se conoce como osteosarcoma rico en células gigantes.
Evolución
y
Pronóstico:
En general la evolución es rápida, excepto en los tumores de tipo densificante. Puede producir metástasis por vía hematógena en los pulmones, esqueleto y otros lugares. Las metástasis linfáticas son raras.
En
el
momento
del
diagnóstico,
la
mayoría
de
los
osteosarcomas
están
en
el
estadio
IIb
que
han
infiltrado
el
tejido
blando.
En
50%
de
pacientes
adolescentes,
el
tumor
penetra
por
el
platillo
de
crecimiento
en
la
epífisis
Metástasis:
El
osteosarcoma
tiende
a
tener
metástasis hematógenas
tempranas.
Las
metástasis
pulmonares
o
linfáticas
se
detectan
en
el
momento
de
la
presentación
en
aproximadamente
10%
de
pacientes.
Después
de
la
resección
quirúrgica,
se
encuentran metástasis
salteadas
en
25%
de
pacientes.
Sitio de las metástasis. Con respecto al sitio, pacientes que tienen metástasis viscerales tienen las proporciones de supervivencia pobres. Con metástasis óseas solo, el manejo no operatorio, la supervivencia es 0%. Sin embargo en los pacientes con el metástasis del hueso operable, hay un índice de supervivencia superior al 10%. Con respecto a los metástasis pulmonares, si la enfermedad es operable hay una 30% de supervivencia global.
Tiempo de metástasis. Las metástasis pueden ocurrir sincrónicamente (al diagnóstico) o metasincrónicamente. Para aquellos con metástasis sincrónicas, 20% a 40% desarrollan metástasis. Para aquellos con metástasis metasincronicas tempranas, la supervivencia es menos de 10%. Para aquellos con metástasis metasincronicas tardías, la supervivencia global es 30% a 50%.
La identificación de metástasis. Un problema es la identificación correcta de las metástasis. De 51 casos considerados en la institución del Dr. Picci del Laboratorio de Investigación Oncológica al Instituto Ortopedico Rizzoli en el Bolonia, Italia, para aquellos que tenían metástasis de pulmón al diagnóstico y quién sufría el toracotomía, sólo 57% demostraron el tumor en la intervención; 22 casos eran negativos, con otros diagnósticos documentados, como subatelectasia, infiltración linfoide, o fibrosis intersticial. Cómo paciente probable de tener metástasis histológicas era la asociación con un número de nódulos pulmonares anormales: con 1 nódulo, sólo 31% eran realmente metástasis, pero con más de 7 nódulos 100% eran metástasis. Con 29 casos operables, se dieron 45% quirúrgicamente enfermedad-libre.
La experiencia con las metástasis del metasincronicas ha mostrado que el más largo intervalo enfermedad-libre antes de que la metástasis apareciera, y el más bajo grado del tumor, probablemente podría lograrse la supervivencia más prolongada. Treinta por ciento de pacientes operables eran sobrevivientes a largo plazo. La cirugía debe ser muy agresiva para ser eficaz.
Éxitos recientes con la dirección de pacientes con osteosarcoma de alto riesgo. Se han informado sobrevivientes de metástasis del hueso. En un estudio que usa un "protocolo del prognosis pobre" actualizado, con ifosfamida a dosis alta y G-CSF de apoyo, se trataron 61 pacientes con osteosarcoma metastático. Ellos incluyeron las metástasis a los pulmones, hueso y recidivas locales, con 41% de pacientes informados como libres de la enfermedad.
Supervivencia:
En
el
pasado
la
tasa
de
supervivencia
estaba
alrededor
de
15%,
pero
con
la
terapia
complementaria
la
supervivencia
es
mayor
del
50%.
La
enfermedad metastática
evidente
a
la
presentación
también
indica
la
presencia
de
enfermedad
más
agresiva
y
peor
pronóstico.
Tratamiento
Cirugía
Algunas de las preguntas de los cirujanos oncológicos son si la cirugía puede provocar la curación y cual es la mejor cirugía desde el pufo de vista oncológico y funcional. La intervención ideal es, desde luego, aquella en que el paciente se cura y no tiene ninguna morbosidad y ninguna complicación. Hay normalmente y por desgracia, un trueque entre la función y complicaciones.
La cirugía sola como tratamiento proporciona un índice de supervivencia del 20%.
Salvamento
del
miembro
contra
la
amputación.
Cuando
se
considera
el
osteosarcoma
de
la
extremidad,
las
opciones
incluyen
amputación
o
salvamento
del
miembro.
La
amputación
está
asociada
con
una
más
baja
proporción
de
recidiva
local
pero
no
con
un
beneficio
de
supervivencia.
En
algunos
informes,
no
hay
ninguna
diferencia
funcional
y
ninguna
diferencia
en
la
calidad
de
vida.
Extrapolado
sobre
tiempo
de
vida
paciente,
la
amputación
es
más
cara
debido
a
la
necesidad
de
nuevas
prótesis.
Opciones quirúrgicas para el osteosarcoma femoral distal. Hay varios opciones para el tratamiento del osteosarcoma femoral distal , incluso la amputación, reconstrucción endoprotésica, compuesto del aloinjerto/prótesis, autoinjerto, osteogénesis de distracción, artrodesis, rotaciónplastia, y autoinjerto radiado.
La reconstrucción endoprotésica tiene la ventaja de carga de peso inmediata y una proporción de complicaciones tempranas baja, pero los fracasos tardíos pueden ocurrir. Los aloinjertos llevan el riesgo de no-unión y fractura y un riesgo aumentado de infección, y se asocia con muchos problemas precoces; sus resultados tardíos son buenos si sobreviven el periodo postoperatorio temprano. La reconstrucción Aloinjerto/endoprótesis para el fémur distal no juega un papel importante. La osteogénesis de distracción con la instrumentación de Ilizarov tarda muchos meses para lograr el crecimiento nuevo. La artrodesis presenta un problema funcional: los pacientes no pueden sentarse cómodamente. La rotacionplastia es funcionalmente superior a la amputación pero es cosméticamente problemática. El papel del autoinjerto en el reemplazo femoral distal es mínimo; de vez en cuando pueden usarse autoinjertos de tibia o iliacos para el salvamento de no-uniones del aloinjerto.
Con respecto a la reconstrucción endoprotésica, las complicaciones quirúrgicas tempranas incluyen muerte, embolia pulmonar, infecciones, y la recidiva local. Las complicaciones tardías incluyen el fracaso del implante, y el aflojamiento es inevitable. La infección tardía diseminada por vía hematógena también es posible. Los resultados de el Hospital Ortopédico Real en el Reino Unido, muestra 100% supervivencia del implante humeral proximal pero altas tasas de fracaso en las extremidades inferiores. Hubo una 60% proporción de fracaso del fémur proximal a los 20 años, o aproximadamente una proporción del 2% de fracaso anual. Para la tibia proximal y fémur distal, la proporción de fracaso era más alta, 3% por año.
Debido a los nuevos miembros artificiales requeridos, hay más gasto incurrido para la amputación que para la reconstrucción endoprotésica para los sobrevivientes a largo plazo. Los estudios anteriores han mostrado que la proporción de supervivencia es el mismo sin tener en cuenta si los pacientes tienen salvamento del miembro o amputación.
Más recidiva local ocurre con las resecciones marginales y menos de 90% de necrosis en el espécimen quirúrgico siguiendo a la quimioterapia.
Quimioterapia:
Con
la
quimioterapia
adyuvante,
el
índice
de
supervivencia
a
los
5
años
está
en
más
de un
50%.
Algunos cirujanos insisten en la quimioterapia preoperatoria en el manejo del osteosarcoma.
El
papel
de
Altas
dosis
Metotrexato
Dr. Kirsten Sundby Hall de la Sección de Hospital de Radio noruega de Oncología en Oslo, Noruega, presentó una sesión en el uso de metotrexato de la alto-dosis en el tratamiento de osteosarcoma.
Historia del uso del metotrexato en el osteosarcoma. El Metotrexato es un antagonista del ácido fólico y es el único citostático en uso que tiene un antídoto (leucovorin). Su primer uso informado fue en 1948, y Jaffe usó el metotrexato para sarcoma metastático en 1972, logrando una 30% proporción de respuesta. En 1977, Rosen dio el metotrexato a altas dosis como terapia de neoadyuvante para la enfermedad primaria, e informo una proporción del 50% de respuesta.
El uso Neoadyuvante de metotrexato. Las ventajas de la terapia neoadyuvante (preoperatoria) incluye la oportunidad para examinar la proporción de respuesta histológica y permitir los protocolos del salvamento en la respuesta pobre. Puede haber un efecto primario en el tumor, permitiendo hacer los procedimientos de salvamento de miembro más seguros. La administración puntual de la quimioterapia previa a la cirugía puede permitir el tratamiento temprano de micrometástasis. En el estudio, [del Grupo de Sarcoma escandinavo] el uso de metotrexato de alta-dosis para el osteosarcoma era asociado con una supervivencia más larga en la respuesta buena contra las respuestas pobres. También, la respuesta histológica pobre se puso en correlación con el nivel sérico más bajo de metotrexato en la sangre a 24 y 48 horas cuando se comparó con las respuestas buenos. Los pacientes con los niveles en sangre más altas de metotrexato también tenían mejor supervivencia e índice de recaída-libre, aunque ésta era una tendencia y no estadísticamente significante.
Problemas corrientes en el uso de metotrexato de alta-dosis. Incluso con las dosis normales, existe gran variabilidad en el metotrexato del suero paciente. Una opción para lograr los niveles terapéuticos es medir el nivel del suero y entonces dosificar la subida en los pacientes seleccionados.
La tendencia ha sido agregar otros agentes a los regímenes de quimioterapia con metotrexato para el osteosarcoma; estas drogas incluyen adriamicina y cisplatino.
Un estudio no mostró una mejoría en la supervivencia con metotrexato de alta-dosis agregado a un régimen multiagente para el osteosarcoma. Las posibles razones para la falta de efecto serían la dosis demasiado bajas, la sobrehidratación, el prematuro rescate con leucovorin, la intensidad de dosis inadecuada, y la duración del tratamiento corta.
En conclusión, el metotrexato a altas dosis mejora la supervivencia en el osteosarcoma, el efecto se relaciona a la concentración en suero, puede usarse la subida de dosis para aumentar el efecto, y otros regímenes de citostáticos agregados a altas dosis de metotrexato podría mejorar los resultados.
Salvamento
del
miembro:
Resección
quirúrgica
de
las
metástasis
pulmonares
del
osteosarcoma.
La
resección
quirúrgica
agresiva
mejorará
el
índice
de
supervivencia
a
los
5
años;
La
resección
de
metástasis
pulmonares,
junto
con
la
poliquimioterapia
se
asocia
con
una
supervivencia
a
largo
plazo
en
aproximadamente
20
por
ciento
de
tales
pacientes.
La resección del tumor pulmonar requiere un buen control de la enfermedad local y ninguna metástasis extra-pulmonar.
Osteosarcoma de celulas pequeñas
Discusión
Hutter (1966) lo llamó "osteosarcoma primitivo multipotencial primario del hueso", "polihistioma" por Jacobson (1977), Sim y col. (1979) "osteosarcoma de células pequeñas". Algunos autores lo clasifican como condrosarcoma mesenquimal, por su producción de matriz cartilaginosa, y Schajowicz (1983), desde un punto de vista histogénico como un tumor de células redondas productor de osteoide tumoral o hueso y le da el nombre de osteosarcoma mesenquimal.
Supone el 1% de todos los osteosarcomas.
Las localizaciones preferidas son el fémur distal, el húmero proximal, y la tibia proximal.
La edad de presentación suele ser la segunda década.
Radiografías
Se presenta, generalmente como una lesión radiolucente con bordes permeativos, asociada con una gran masa de tejidos blandos. Esa presentación hace recordar a los tumores de células redondas, como el sarcoma de Ewing. En algunos casos se presenta como una lesión esclerosa similar a la del osteosarcoma clásico. En la mayoría de los casos hay una importante reacción perióstica.
Histología
El estudio histológico de estas lesiones muestran acúmulos de células redondas pequeñas, bandas separadas de colágeno y una fina matriz eosinófila que recuerda el sarcoma de Ewing. Además esta lesión también puede mostrar una tinción positiva del glucógeno, como en el sarcoma de Ewing. Sin embargo, la presencia de núcleos ovales y las células fusiformes en algunas áreas, y la producción de osteoide o hueso y en algunos casos puede haber algo de cartílago maligno, ayudan a diferenciar el sarcoma de Ewing de esta entidad.
La diferenciación de osteosarcoma de células pequeñas puede ser difícil; estos tumores tienen áreas que se parecen al sarcoma de Ewing pero también tienen algún osteoide. Hay informes de 11/22 translocaciones en el osteosarcomas de células pequeñas, mientras se plantea la pregunta acerca de si deben tratarse como el sarcoma osteogénico o como el sarcoma de Ewing.
Osteossarcoma fibrohistiocitico
Esta variante recuerda al fibrohistiocitoma maligno, y en algún caso pueden confundirse debido a que ambos tumores tienden a aparecer en una edad superior que la del osteosarcoma clásico, generalmente después de la tercera década. Ambos afectan a la porción articular de los huesos largos, y la reacción perióstica es menor que en la del osteosarcoma convencional.
Radiográficamente ambas lesiones suelen ser radiolucentes y generalmente el osteosarcoma fibrohistiocítco presenta áreas de formación ósea que asemejan a bolas de algodón o acúmulos de nubes, mientras que el fibrohistiocitoma maligno no tiene esta apariencia.
Histológicamente, el osteosarcoma fibrohistiocítico se caracteriza por la presencia de células fusiformes pleomórficas y células gigantes, muchas de las cuales poseen núcleos extravagantes. Es lesión recuerda al osteosarcoma rico en células gigantes. No es normal un fondo inflamatorio, y la configuración nebulosa estoriforme o espiral, característica del fibrohistiocitoma, a pesar de que algunas veces es un hallazgo dominante, puede ser menos prominente o puede ser sustituido por grandes áreas de células pleomórficas organizadas en un manto difuso. Como en todos los otros subtipos de osteosarcoma, la distinción de otros sarcomas depende de la demostración de formación de osteoide o hueso por las células malignas en le típico patrón que se ve en el osteosarcoma.
Osteossarcoma telangiectasico
El osteosarcoma telangiectásico o hemorrágico es muy raro (5% de los osteosarcomas) y muy agresivo. Es el doble frecuente en mujeres que en hombres, y predomina en la segunda y la tercera década. Suele aparecer en el fémur o la tibia. Es un tumor hipervasularizado con zonas necróticas y hemorrágicas, que presenta grandes sinusoides, cavidades hemáticas y células gigantes multinucleadas reaccionales a la hemorragia.
Radiográficamente se presenta como una lesión lítica y destructiva exclusivamente. Puede haber masa de tejidos blandos. La reacción perióstica es agresiva (laminar, en sol naciente, triangulo de Codman). En algunas ocasiones recuerda al quiste óseo aneurismático. La RM muestra áreas de alta señal en T1 debidas a la presencia de hemoglobina. En ocasiones pueden verse niveles líquido-líquido, indicando la presencia de hemorragias, que también pueden aparecer en el quiste óseo aneurismático.
Las fracturas patológicas no son raras en casos de lesiones grandes.
Macroscópicamente el tumor es muy blando, semejando a una esponja con grandes cavidades llenas de sangre y coágulos. Generalmente se ve gran destrucción de la cortical y masa de partes blandas.
Histológicamente se pueden ver dos patrones. Hay grandes cavidades entremezcladas con tabiques y zonas cuyo tejido revela origen sarcomatoso, y que en poco aumento recuerda a un quiste óseo aneurismático. A mayor aumento se ven elementos de origen mesenquimatoso con gran pleomorfismo, muchas mitosis y células gigantes benignas y malignas, así como una producción focal de osteoide mucho mayor que la que se ve en el quiste óseo aneurismático. En algunas ocasiones la producción de osteoide es mínima.
La evolución es rápida y agresiva. Y aunque responde bien a la quimioterapia, su agresividad no da tiempo ni a acabar los ciclos de quimioterapia preoperatoria, teniendo que recurrir directamente a la amputación.
Osteosarcoma rico en celulas gigantes
Es una variedad rara de osteosarcoma, con una apariencia de sarcoma indiferenciado con hiperabundancia de osteoclastos (células gigantes) y escasez de osteoide o hueso tumoral.
Supone aproximadamente el 3% de todos los osteosarcomas.
Histológicamente está relacionado con el osteosarcoma telangiectásico y con el fibrohistiocítico.
Radiográficamente se caracteriza por la ausencia de muchos de los signos clásicos del osteosarcoma, y la diferenciación de algunas lesiones malignas es difícil. En muchos casos la lesión lítica muestra unos bordes pobremente definidos. La localización típica es la metáfisis o diáfisis de los huesos largos, generalmente la tibia y el fémur. La reacción perióstica está ausente o es escasa, y generalmente no hay masa de tejidos blandos
Histológicamente tiene un estrecho parecido al tumor de células gigantes. La producción de osteoide es escasa y difícil de identificar.
Osteosarcoma central de bajo grado
Es una variedad muy rara. Supone menos del 2% de todos los osteosarcomas, y generalmente afecta a pacientes mayores que los del osteosarcoma clásico (28 años).
Sus sitios predilectos son la tibia y el fémur.
El osteosarcoma central de bajo grado (bien diferenciado) es un tumor central, osteolítico, condensante o mixto, que presenta un patrón radiológico poco agresivo.
Clínicamente, los pacientes con este tipo de tumor presentan una larga historia de dolor, disconfort o tumefacción inespecífica.
Estudios radiográficos. En muchos casos se etiqueta de displasia fibrosa en base a la radiografía y a la histología. No obstante en otros casos es indistinguible radiográficamente del osteosarcoma central clásico, pero más a menudo la lesión aparenta benignidad, con un anillo escleroso bien definido. La expansión es frecuente, y la cortical es a menudo adelgazada. Es rara la reacción perióstica, así como la extensión a los tejidos blandos.
Las radiografías, en muchos casos recuerdan a la displasia fibrosa, tumor de células gigantes, fibroma desmoplástico y ocasionalmente a la miositis osificante.
El diagnóstico histológico es muy difícil, y puede parecerse a la displasia fibrosa, fibroma no osificante, osteoblastoma, fibroma condromixoide, o reacciones inespecíficas. En el examen microscópico se observan campos fibroblásticos con trabéculas óseas y osteoides. Las células intercaladas entre las trabéculas son fusiformes, organizadas en manojos, sin apariencia de malignidad. El núcleo puede mostrar alguna atipia, pero no hay pleomorfismo y las mitosis son raras. puede haber alguna producción de colágeno y hueso, y las células estromales pueden invadir la cavidad medular y las trabéculas del huso esponjoso y cortical. La lesión puede parecerse al fibroma desmoplástico en unos caso y a la displasia fibrosa en el otro extremo. No obstante se diferencian porque las espículas formadas en esta última lesión son generalmente voluminosas y poco delicadas, de forma curvilínea. También pueden verse focos de cartílago, aunque es raro. Como consecuencia el diagnóstico solo es posible con la ayuda de la correlación radiográfica.
La evolución es lenta o muy lenta y el pronóstico es bueno, aunque se han descrito casos con metástasis.
El tratamiento de elección es la resección quirúrgica amplia, sin necesidad de quimioterapia
Osteosarcoma intracortical
Es la forma más rara de osteosarcoma. Solo se han comunicado 8 casos.
El rango de edad oscila entre los 10 a los 40 años (media 24), siendo el sexo femenino el predominante.
Clínicamente se presenta con dolor, frecuentemente asociado con la actividad. En algunos pacientes hay una historia de traumatismo previo.
El tumor afecta la cortical y no se extiende a la medular ni al tejido blando.
Radiográficamente se presenta como una lesión radiolucente rodeada de una reacción esclerosa. El tamaño de la lesión varia de 1 a 4.2 cm. En algunos casos la lesión puede evocar a un osteoma osteoide o un osteoblastoma intracortical.
Histológicamente muestran las células tumorales redondas o fusiformes, pleomórficas, con núcleo vesicular y prominentes nucleolos. También se observan figuras mitóticas. La matriz producida por las células malignas tiene un patrón acordonado con osteoide tumoral.
Osteosarcoma maxilar
Se da en pacientes de más edad que el osteosarcoma convencional (35 años de media).
Generalmente es un tumor bien diferenciado, con un índice bajo de mitosis, un gran componente condroblástico, y un pobre potencial de malignidad.
Su pronóstico es mejor que otras formas de osteosarcoma, aunque su localización impide la cirugía amplia.
Osteosarcoma multicentrico (multifocal)
También llamado osteosarcomatosis esclerosante. Se trata de focos múltiples de osteosarcomas esclerosantes que aparecen, al mismo tiempo o en un intervalo corto, en diferentes lugares del esqueleto; son las variantes sincrónica y metacrónica.
Es un tipo muy raro de osteosarcoma (1.5% de todos los osteosarcomas), y se suele presentar a una edad inferior a los 18 años con ligero predominio por las mujeres, sobre todo en edades superiores.
Su distribución es muy difusa. Los focos pueden ser muy numerosos, y algunos muy pequeños. Los sitios preferidos en orden de frecuencia son: el tercio distal del fémur, proximal de la tibia, proximal del fémur, pelvis, y húmero proximal, aunque se puede presentar en cualquier hueso del esqueleto.
No está claro si este tipo de osteosarcoma es una entidad separada o se trata de múltiples metástasis de un osteosarcoma convencional. Cuando hay múltiples huesos afectados en ausencia de metástasis pulmonares, lo más probables es que se trate de un osteosarcoma multicéntrico.
Amstutz clasificó los osteosarcomas multicéntricos en tres patrones: Tipo I, lesiones sincrónicas que se da en pacientes jóvenes, En la mayoría de los casos sin metástasis pulmonares. Radiográficamente las lesiones se localizan preferentemente en la metáfisis de los huesos largos, y son densas y esclerosas. Histológicamente la lesión es una densa osificación osteoblástica tipo osteosarcoma. Tipo II, son lesiones de bajo grado, sincrónicas, limitadas al esqueleto axial, y se da en adultos. Tipo III, son los casos de lesiones metacrónicas, y se caracteriza porque las lesiones esqueléticas son asimétricas y de tamaño variable, y no necesariamente son esclerosas. La edad es variable, pero suelen ser adolescentes o adultos jóvenes. En algún caso de este este último grupo se cree que se trata de metástasis de un osteosarcoma primario.
Las radiografías y la anatomía patológica de los focos de osteosarcoma tienen la peculiaridad de ser uniformemente condensantes o ebúrneos y de no atravesar la cortical.
El pronóstico del osteosarcoma multifocal sincrónico es pobre y la mayoría de los pacientes sobreviven unos pocos meses después del diagnóstico. En el caso de las lesiones metacrónicas, son potencialmente curables con tratamiento quirúrgico.