... Condroblastoma ...
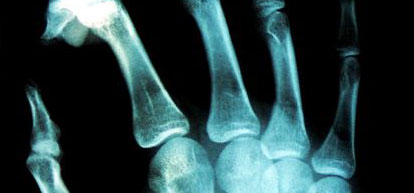
Discusión:
Definición de la OMS: "Tumor benigno relativamente raro, que se caracteriza por un tejido muy celular y relativamente indiferenciado constituido por células redondeadas o poligonales semejantes a los condroblastos y de bordes netos por células gigantes multinucleadas de tipo osteoclástico aisladas o en grupos. En general se encuentra poco material intercelular, pero es típica la presencia de pequeñas cantidades de matriz cartilaginosa intercelular con zonas de calcificación focal."
Es
el
más
común
de
los
tumores
óseos
epifisarios
en
los
adolescentes
y
niños,
aunque no
infrecuentemente,
el
tumor
también
se
da
en
los
adultos.
En
el
informe
de
AJ.
Ramappa et al, el 62% de los 47 pacientes eran de 20 años de edad o más jóvenes
(en contraste, 38% de pacientes tenían más allá de la madurez de esqueleto)
Predomina en el sexo masculino, es el doble de frecuente que en le femenino. Su frecuencia es del 1% de los tumores primarios del hueso y el 9% de los tumores benignos del hueso.
El
equivalente
en
los
adultos
del
condroblastoma
es
el
tumor
de células
gigantes,
por
eso
Ewing
lo
llamó
tumor
de
células
gigantes
calcificado.
Presentación
clínica:
Dolor moderado de meses de evolución, cerca de una articulación. Limitación del movimiento articular. En ocasiones puede haber tumefacción y derrame articular.
La mayoría son lesiones en estadio activo 2 /3 de Enneking
Localización:
Las
lesiones
están
ampliamente
distribuidas
en
el
esqueleto,
pero
la
mayoría
están
en
las
epífisis
o
apófisis.
Nota, el condroblastoma es el tumor más común que afecta la rótula, seguido por el tumor de células gigantes.
Las lesiones metastáticas son raras pero ocurren. Los nódulos pulmonares tienen la misma apariencia histológica que la lesión primaria.
Radiografías:
La
lesión es radiolucente,
de
la
epífisis
con
calcificaciones
punteadas
finas. Se
observa
una osteolisis oval
localizada
excéntricamente
en
la
epífisis.
En
el
estadio
3
del
condroblastoma
pueden
extenderse
por
el
platillo
de
crecimiento
en
la
metáfisis
o
a
través
del
cartílago
articular
en
la
articulación.
Es una lesión con patrón geográfico de destrucción, con bordes lisos en el 63% de los casos, festoneados en el 27% y lobulados en el 10%. En algún caso puede observarse trabeculación interna.
Hay ligera expansión del hueso con ensanchamiento o abombamiento de la cortical. En más del 50% de los casos hay reacción perióstica sólida o en capa, generalmente localizada a distancia del tumor. Este fenómeno es atribuido a una respuesta inflamatoria
El
tumor
normalmente
se
rodea
por
un
margen
bien
definido
de
hueso
reactivo
(a
diferencia
del
tumor
de
células
gigantes).
TAC:
Es útil en la demostración de la densidad del tejido, las calcificaciones sutiles, la magnitud de la afectación de la epífisis, y a menudo y mas importante la situación de la lesión respecto al cartílago articular y epifisario.
RNM
Muestra una gran área de afectación que incluye edema de los tejidos blandos y de la médula ósea. Esta apariencia tan agresiva puede hacer pensar en un tumor maligno. Probablemente la combinación de matriz condroide altamente celular y calcificación es la responsable del descenso de relajación en la imágenes ponderadas en T2. En T" se observa una señal heterogénea de baja a intermedia, arquitectura lobular interna y márgenes lobulares finos. Los lóbulos focales de baja, intermedia, y alta intensidad de señal están superpuestos y lo mas probable es que correspondan a calcificación, matriz condroide y líquido de la lesión. Además la RNM puede demostrar una extensión, por otro lado rara, del tumor a los tejidos blandos, y puede revelar el derrame articular.
Histología:
El condroblastoma está compuesto por nódulos de matriz cartilaginosa bastante madura rodeados por tejido celular abundante, relativamente indiferenciado, compuesto por células redondas y poligonales pseudocondroblásticas. En los bordes de las áreas diferenciadas, hay usualmente células tipo osteoclástico o condroclástico. Las células de pequeño tamaño son globulosas y poliédricas, de contornos citoplasmáticos nítidos. Los nucleolos son redondos, bien coloreados, a menudo con nucleolo evidente. Entre las células, las fibrillas colágenas son escasas y la sustancia fundamental aún más. Se ven diseminados algunos núcleos pequeños de calcificación. Las sales calcáreas se incrustan en la sustancia intercelular y en las mismas células, formando una delicada red hexagonal pericelular que provoca la degeneración y la muerte de las células. A pesar de que la matriz condroide es relativamente escasa en el condroblastoma, las células muestran una reacción inmunohistológica al proteína S-100, idéntica a la de otros tumores cartilaginosos.
Las
metástasis
pulmonares
no
muestran
histológicamente
evidencia
de
malignidad,
no
obstante
se
ha
aportado
algún
caso
de
transformación
maligna.
Diagnóstico diferencial
Hay sólo tres tumores que pueden invadir la fisis: el condroblastoma, tumor de células gigantes, y el condrosarcoma de células claras.
Radiográfico
En la localización típica hay pocas lesiones para incluir en el diagnóstico diferencial. Los hallazgos pueden ser inespecíficos si no hay calcificaciones o si se extiende a la metáfisis cuando se ha cerrado el cartílago epifisario.
Condrosarcoma de células claras: El condrosarcoma de células claras (vea el condrosarcoma) es raro, de crecimiento lento, tumor localmente recurrente, confundido fácilmente con el condroblastoma pero maligno. No existe ninguna diferencia, ya que exhiben el mismo patrón de benignidad, excepto una mayor expansión y una tendencia a evolucionar.
Absceso óseo: Pueden tener zonas de opacidad a los rayos X debido a pequeños secuestros. El absceso es fundamentalmente metafisario, y está rodeado de un ribete intenso y ancho de osteoesclerosis. No hay calcificaciones en la lesión, y en raros casos hay reacción perióstica.
Osteonecrosis de la cabeza humeral y femoral: ocasionalmente recuerda al condroblastoma. Generalmente hallazgos radiográficos clásicos tales como un signo de la media luna, y una densidad más homogénea adyacente a ella. La resonancia magnética de la osteonecrosis también es típica y son variado en dependencia del estadio de la osteonecrosis.
Ganglión intraóseo: Es una lesión rara cerca de la superficie articular, invariablemente de localización excéntrica, y preferentemente en la rodilla, tobillo, y hombro. Es infrecuente verlo antes de la maduración esquelética.
Tumor de células gigantes: el tumor de células gigantes normalmente aparece en la 3-4 década (mientras el condroblastoma aparece en la segunda), y los que se ven en el esqueleto inmaduro se localizan en la metáfisis. El tumor de células gigantes tiene contornos más nítidos y a veces (muy pocas) contiene pequeñas calcificaciones y puede expandirse a epífisis y diáfisis.
Osteoblastoma de la epífisis: es extraordinariamente raro. Su localización usual es la metáfisis o la diáfisis.
Encondroma: es raro en la epífisis, pero en alguna ocasión se puede parecer al condroblastoma.
Granuloma de Langerhans: como el osteoblastoma y encondroma es raro en la epífisis, nunca presenta calcificaciones centrales.
Ocasionalmente, una radiolucencia normal en el humero proximal (que representa aumento de tejido esponjoso en el trocánter mayor) puede provocar confusión y diagnosticarse de condroblastoma.
Patológico
Histológicamente el condroblastoma debe diferenciarse del condrosarcoma y del tumor de células gigantes. Como ocasionalmente presenta grandes núcleos de tamaño y forma variable, junto con la presencia de figuras amitóticas, pueden indicar malignidad.
Como las células gigantes pseudoosteoclásticas forman parte del patrón histológico del condroblastoma, estando presentes particularmente en los bordes de las áreas condroides de este tumor, esto puede confundir con el tumor de células gigantes. Las células gigantes del condroblastoma, se pueden distinguir de las mismas células del tumor de células gigantes por la apariencia redonda de las primeras, en contraste con la apariencia fusiforme de las células del estroma del tumor de células gigantes. La presencia de áreas condroides indica la naturaleza cierta del tumor. Si a pesar de eso existen dudas, la tinción de la matriz con fucsina-aldehído en un pH de 1.0 es útil, especialmente cuando se combina con la proteína S-100. La matriz condroide del condroblastoma se tiñe de púrpura con aldehído-fucsina. La tinción con proteína S-100 está presente en el citoplasma del condroblastoma pero está ausente en las células mononucleares del tumor de células gigantes.
Tratamiento:
Es importante una biopsia previa para documentar la histología.
El
tratamiento
de
elección
es
la
escisión
amplia,
si
técnicamente
es
posible.
Consiste
en
curetaje
intralesional
combinado
con
tratamiento
adyuvante
local
como
congelación
con
nitrógeno
líquido
o
fenol
y
colocación
de
chips
óseos
de
aloinjerto
o
autoinjerto o
polimetilmetacrilato. Debido
a
que
los
condroblastomas
pueden
extenderse
al
hueso
subcondral,
es
difícil
de
realizar
la
escisión
marginal
o
curetaje
completo.
En los adolescentes mayores, el curetaje de los platillos de crecimiento puede promover el cierre epifisario (evita las deformidades angulares).
La mayoría de condroblastomas están en estadio 2 activo, y son dóciles al tratamiento con curetaje, con riesgo moderado de recurrencia.
Es importante evitar la penetración en la articulación porque las células del condroblastoma crecerán en el líquido articular.
Puede agregarse al curetaje el metilmetacrilato para el defecto para prevenir la recurrencia.
El condroblastoma en estadio 3 (más común en la pelvis) no es dócil al curetaje debido a que el 50% recidivan. En la fase 3 requerirá la escisión en bloque. En esta fase pueden metastatizar a los pulmones.
En general, el pronóstico es bueno para la mayoría de los pacientes; sin embargo la proporción de recidiva local es del 14%. Este tumor, relativamente raro, requiere un tratamiento quirúrgico cuidadoso con el objetivo de evitar la repetición local y la pérdida subsiguiente de función de la articulación. El estudio cuidadoso de las imágenes preoperatorias mejorarán los resultados quirúrgicos. Si hay nódulos pulmonares, deben quitarse siempre que sea posible.
Los pacientes con lesiones alrededor de la cadera (fémur proximal, trocánter mayor, y pelvis) más probablemente desarrollarán recidivas así como lesiones metastáticas; (J Bone Joint Surg [AM] 82-A: 1140-5, 2000)