Última revisión:
Cirugía oncológica ortopédica: principios, márgenes (Enneking/R) y reconstrucción
Tratamiento quirúrgico de los tumores musculoesqueléticos — Actualización 2026: control local con márgenes oncológicos adecuados y preservación funcional cuando sea seguro
La cirugía sigue siendo el pilar del control local en los tumores musculoesqueléticos y debe planificarse en un comité multidisciplinar. En 2026, además de la clasificación clásica de márgenes de Enneking, se integra de forma rutinaria el lenguaje de márgenes R (Rx/R0/R1/R2), con orientación y marcaje sistemático de la pieza para una valoración anatomopatológica fiable. La estrategia quirúrgica se define por: histología y grado, extensión anatómica (RM/TC), respuesta a tratamiento neoadyuvante cuando aplique, posibilidad real de R0 y función esperable tras la reconstrucción.
Planificación quirúrgica
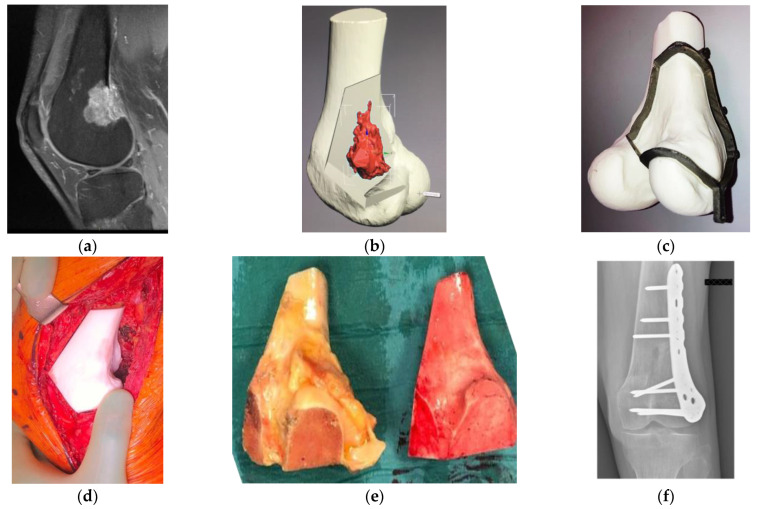
0) En 1 minuto
- ✅ Objetivo: resección en bloque con margen negativo siempre que sea factible (ideal: R0), sin “contaminar” planos.
- ✅ Márgenes (2 lenguajes que conviven):
- 🔹 Enneking: intralesional / marginal / amplia / radical.
- 🔹 Clasificación R:
- 🔹 Rx: margen no valorable.
- 🔹 R0: márgenes microscópicamente negativos.
- 🔹 R1: margen microscópicamente positivo.
- 🔹 R2: tumor macroscópico residual.
- ✅ Regla práctica en sarcomas de partes blandas: intentar R0; como orientación, ≥1 cm o una barrera anatómica intacta (fascia, periostio, epineurio, adventicia) suele considerarse adecuado, según localización/histología/RT.
- ✅ Biopsia: debe estar planificada y su trayecto siempre se reseca con la pieza definitiva.
- ✅ Preservación vs. amputación: preservación si se puede lograr margen oncológico seguro y la función final será razonable; amputación si no se puede garantizar R0 (o equivalente “amplio/radical”) o si el resultado funcional será peor que una buena prótesis.
Pitfall crítico: “Resección no planificada” o intralesional/marginal en un tumor maligno por falta de estadificación/planificación (incluida biopsia mal situada) → alta recidiva local, necesidad de reintervenciones y peor pronóstico. Igual de importante: orientar y marcar la pieza para que el patólogo pueda definir el margen real.
1) Conceptos generales
1.1 Principios 2026
- ✅ Centro especializado + MDT: radiología músculo-esquelética, patología de sarcoma, oncología médica, RT, cirugía plástica/vascular.
- ✅ Planificación por imagen: RM con protocolo de sarcoma (incluye compartimentos, relación con fascia/paquetes), TC para cortical/planificación ósea, angioTC si dudas vasculares.
- ✅ Planificación de la biopsia: el trayecto debe quedar en el campo de resección definitiva (evitar múltiples trayectos/drenajes innecesarios).
- ✅ Reconstrucción “desde el inicio”: decidir antes de operar cobertura de partes blandas, necesidad de colgajos, y compatibilidad con RT/QT.
- ✅ Si se prevé RT: priorizar cobertura fiable de partes blandas (colgajos cuando proceda) y valorar el riesgo de complicaciones de injertos biológicos.
2) Tipos de cirugía
| Tipo | Descripción |
|---|---|
| Preventiva | Lesiones con riesgo de complicación (p. ej., fractura) o selección de casos con potencial de progresión. |
| Diagnóstica | Biopsia (ideal core/incisional planificada) y procedimientos de estadificación selectivos. |
| Terapéutica |
|
3) Márgenes quirúrgicos: Enneking (clásico) y clasificación R (actual)
3.1 Enneking (1983): relación del plano de disección con el tumor
Enneking define el margen por dónde pasa el plano de disección (tumor / pseudocápsula / zona reactiva / tejido sano / compartimento), no por “cuántos centímetros” mide el margen.
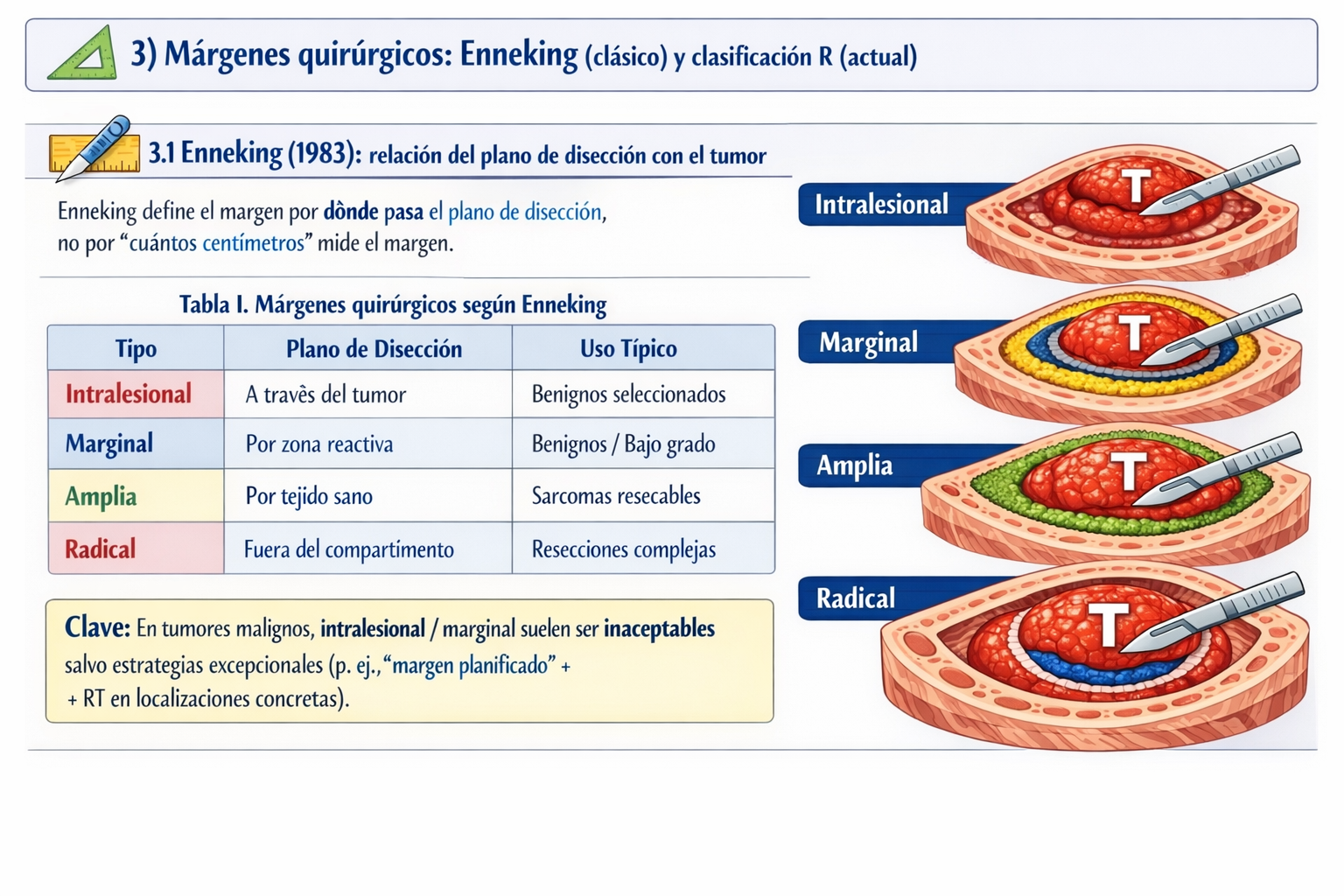
| Tipo | Plano de disección | Uso típico |
|---|---|---|
| Intralesional | A través del tumor (curetaje/exéresis por fragmentos) | Benignos seleccionados ± coadyuvantes |
| Marginal | Por la zona reactiva/peritumoral (extracapsular) | Benignos / bajo grado muy seleccionados |
| Amplia | Por tejido sano (fuera de zona reactiva) dentro del compartimento | Objetivo frecuente en sarcomas resecables |
| Radical | Fuera del compartimento (resección del compartimento completo) | Casos seleccionados (p. ej., resecciones complejas) |
Clave: en tumores malignos, intralesional/marginal suelen ser inaceptables salvo estrategias excepcionales (p. ej., “margen planificado” + RT en localizaciones concretas).
3.2 Clasificación R (Rx/R0/R1/R2): lo que finalmente informa el patólogo
| R | Significado | Implicación práctica |
|---|---|---|
| Rx | No evaluable | Problema de orientación/fragmentación; dificulta decisiones |
| R0 | Margen microscópicamente negativo | Objetivo estándar cuando es factible |
| R1 | Margen microscópicamente positivo | Valorar re-resección si morbilidad asumible; si no, adyuvancia (RT) según caso |
| R2 | Tumor macroscópico residual | Re-operación/estrategias multimodales; peor control local |
3.3 Cómo se “gana” un margen en 2026
- 🔹 Barreras anatómicas: una fascia intacta, periostio, epineurio o adventicia pueden “equivaler” a márgenes más amplios en mm.
- 🔹 Distancia en mm: se reporta la distancia al margen más cercano y el tipo de tejido en ese margen.
- 🔹 Respuesta a neoadyuvancia: en algunos tumores óseos, buena necrosis post-QT puede permitir márgenes más ajustados si son negativos.
3.4 Evaluación anatomopatológica (recomendación práctica)
- 🔹 Orientación de la pieza (suturas/clips/marcadores) + tinta en superficies críticas.
- 🔹 Comunicación cirujano–patólogo: señalar “zona de máximo riesgo” (donde se pasó más cerca).
- 🔹 Informe: estado del margen (claro/involucrado), distancia (mm), tejido del margen, necrosis/respuesta si aplica.
4) Técnica quirúrgica desde el punto de vista oncológico
4.1 Principios intraoperatorios
- ✅ “No contaminar” planos: evitar apertura tumoral; minimizar manipulación; no cambiar instrumental/campos entre tumor y reconstrucción sin protocolo.
- ✅ Control proximal: identificar y proteger paquetes vasculonerviosos; si se prevé resección vascular, planificar reconstrucción.
- ✅ Torniquete/isquemia: uso selectivo (campo seco vs. necesidad de valorar perfusión). Priorizar tiempos cortos y estrategia hemostática.
- ✅ Trayecto de biopsia: siempre incluido en la resección.
- ✅ Plan de cortes óseos: guiado por RM/TC (extensión medular/cortical) y barreras; objetivo: resección en bloque con margen negativo.
- ✅ Herramientas 2026 (cuando disponibles): guías de corte específicas, navegación, impresión 3D para planificación, plantillas de osteotomía.
4.2 Particularidades por tipo de tumor (resumen)
- 🔹 Partes blandas (STS): en general, en bloque; margen recomendado suele ser ≥1 cm o barrera intacta; RT perioperatoria en tumores de mayor riesgo.
- 🔹 Óseos (osteosarcoma/Ewing/UPS): resección con márgenes negativos si es posible; valorar respuesta a QT para decisiones “close margin”.
- 🔹 Axial/pelvis/columna: márgenes amplios pueden no ser factibles; integrar RT avanzada (protones/iones) y resecciones complejas en centros expertos.
5) Criterios de resecabilidad y amputación
5.1 Resecabilidad para preservación de extremidad (criterios prácticos)
- 🔹 R0 alcanzable (o un “margen oncológico aceptable” en contexto de RT/neoadyuvancia) sin abrir tumor.
- 🔹 Paquete vasculonervioso: si está en contacto/encasamiento, decidir si se puede despegar con margen o si requiere resección y reconstrucción factible.
- 🔹 Cobertura de partes blandas viable (posibilidad de colgajo si es necesario).
- 🔹 Función final razonable y rehabilitación realista (edad, comorbilidad, adherencia).
5.2 Indicaciones habituales de amputación / cirugía ablativa
Indicada cuando no es posible garantizar control local con margen adecuado o cuando la extremidad resultante sería no funcional.
Por características locales:
- 🔹 Contaminación por cirugía previa no planificada con diseminación de planos.
- 🔹 Invasión cutánea extensa o pérdida de cobertura no reconstructible.
- 🔹 Afectación nerviosa crítica que impide una función útil (según nivel y alternativas reconstructivas).
- 🔹 Infección/complicaciones no controlables tras reconstrucción previa.
Por localización:
- 🔹 Lesiones distales con mala tolerancia a RT/reconstrucción y alto riesgo de complicaciones.
- 🔹 Determinados tumores infiltrantes en áreas con paquetes vasculonerviosos “sin margen” (según anatomía y experiencia del centro).
Recidiva local tras preservación:
- 🔹 Requiere reevaluación completa; la amputación es frecuente si se han perdido planos o no se puede lograr margen seguro con re-resección.
Fractura patológica (óseos malignos):
- 🔹 Aumenta complejidad y riesgo de contaminación; la decisión depende de histología, extensión, respuesta a QT y viabilidad de margen.
6) Cirugía de preservación de extremidad
6.1 Ideas clave
- ✅ Cuando la selección es adecuada, la preservación puede ofrecer control local comparable a la amputación, con mejor resultado funcional en muchos casos.
- ✅ El objetivo no es “salvar por salvar”: es salvar con margen seguro y función razonable.
- ✅ La pelvis y el eje axial siguen siendo los escenarios más exigentes (resecciones complejas, RT avanzada, prótesis a medida/3D).
6.2 Tipos de resección ósea (recordatorio)
- 🔹 Intercalar: entre articulaciones (diáfisis/metáfisis sin entrar en articulación).
- 🔹 Intraarticular: resección de un lado articular.
- 🔹 Extraarticular: incluye ambos lados o sacrifica la articulación completa por extensión tumoral.
6.3 Complicaciones (visión práctica)
- 🔹 Herida/cobertura: necrosis, dehiscencia, infección (más riesgo con RT neoadyuvante, grandes colgajos o QT).
- 🔹 Reconstrucción: infección protésica, aflojamiento, fractura de injerto, pseudoartrosis/no unión.
- 🔹 Función: rigidez, debilidad, alteraciones de la marcha, dolor crónico.
7) Reconstrucción: opciones y tendencias (2026)
7.1 Opciones clásicas (según defecto)
Defectos intercalares
- 🔹 Aloinjerto intercalar (placa/enclavado) ± refuerzo biológico.
- 🔹 Endoprótesis segmentaria (modular o a medida) cuando se prioriza carga precoz.
- 🔹 Peroné vascularizado (solo o combinado) en defectos seleccionados.
- 🔹 Masquelet (membrana inducida) en escenarios seleccionados (más frecuente en reconstrucción compleja/infección, según experiencia).
Defectos articulares/metafisarios
- 🔹 Endoprótesis de resección (modular o personalizada).
- 🔹 Allograft–prosthetic composite (APC) para mejorar anclaje de partes blandas en casos seleccionados.
- 🔹 Artrodesis cuando se prioriza durabilidad o se requiere resección amplia con estabilidad.
- 🔹 Prótesis expansible en pediatría seleccionada.
- 🔹 Rotaciónplastia (Van Nes) en niños/jóvenes seleccionados (excelente eficiencia protésica).
7.2 Tendencias 2026
- 🔹 Planificación 3D y guías de corte para osteotomías precisas (especialmente pelvis/escápula).
- 🔹 Implantes personalizados / impresión 3D con superficies porosas para osteointegración.
- 🔹 Mejoras antiinfección (protocolos, recubrimientos/estrategias según disponibilidad del centro).
- 🔹 Cirugía plástica “temprana”: colgajos microvascularizados para disminuir complicaciones de herida en resecciones grandes/RT.
8) Amputación / desarticulación
- 🔹 La elección del nivel debe maximizar margen y función protésica.
- 🔹 En malignos, se busca un procedimiento equivalente a amplio/radical (Enneking) y, cuando aplique, evitar R1/R2.
- 🔹 Planificar cierre y cobertura: colgajos cuando la piel/tejidos estén comprometidos (especialmente tras RT o cirugía previa).
9) Indicaciones terapéuticas según estadios (Enneking) — enfoque práctico
| Estadio | Descripción | Tratamiento quirúrgico orientativo |
|---|---|---|
| Benigno 1 | Inactivo | Observación. Si se opera: intralesional/marginal según caso. |
| Benigno 2 | Activo | Marginal o intralesional + coadyuvantes (fresa de alta velocidad, PMMA, crioterapia, etc.) según localización. |
| Benigno 3 | Agresivo | Ideal: amplia. Alternativa: intralesional/marginal + coadyuvantes en escenarios seleccionados. |
| Maligno I | Bajo grado | Resección amplia (objetivo: R0). Reconstrucción según defecto. |
| Maligno II | Alto grado | Tratamiento multimodal (QT/RT según subtipo) + resección con margen negativo si es factible. Amputación si no hay margen seguro. |
| Maligno III | Metastásico | En casos seleccionados: control del primario + tratamiento sistémico + control de metástasis (cirugía/ablación/RT estereotáxica). |
10) Algoritmo de decisión quirúrgica

Resumen para la práctica clínica
📌 Indicaciones
- ✅ Resección en bloque con objetivo de margen negativo (R0) cuando sea factible, priorizando control oncológico.
- ✅ Cirugía intralesional + coadyuvantes en benignos agresivos seleccionados (según riesgo y localización).
- ✅ Amputación cuando no se puede garantizar un margen oncológico seguro o la extremidad resultante sería no funcional.
🔧 Técnica
- 🔧 Planificación preoperatoria con RM/TC, incluyendo plan de biopsia y reconstrucción/cobertura.
- 🔧 Cirugía “no touch”: evitar contaminación, resección en bloque, control neurovascular; guías/navegación/3D cuando aporten precisión.
- 🔧 Orientación y marcaje de la pieza (tinta) para informe fiable de márgenes (R0/R1/R2) y distancia al margen en mm.
⚠️ Riesgos
- ⚠️ Recidiva local (mayor con márgenes positivos o inciertos).
- ⚠️ Complicaciones de la herida (dehiscencia/infección), especialmente con RT/QT y grandes resecciones.
- ⚠️ Complicaciones de la reconstrucción (infección protésica, aflojamiento, fractura de injerto, no unión).
- ⚠️ Déficit funcional y dolor crónico en un subgrupo de pacientes.
✅ Resultados
- ✅ El control local depende de histología, estadio, respuesta a tratamiento sistémico y calidad del margen.
- ✅ En tumores resecables tratados en centros expertos, la preservación puede lograr control local comparable a amputación.
- ✅ Pronóstico global condicionado por estadio y biología tumoral.
11) Bibliografía (selección)
Clásicos y conceptos
- 📄 Enneking WF. Musculoskeletal Tumor Surgery. Churchill Livingstone; 1983.
- 📄 Enneking WF, Spanier SS, Goodman MA. A system for the surgical staging of musculoskeletal sarcoma. Clin Orthop Relat Res. 1980;(153):106-120.
Guías y práctica contemporánea
- 📄 British Sarcoma Group. UK guidelines for the management of bone sarcomas. Br J Cancer. 2024.
- 📄 British Sarcoma Group. UK guidelines for the management of soft tissue sarcomas. Br J Cancer. 2024.
- 📄 SEOM–GEIS. Spanish clinical guidelines for the management of soft-tissue sarcomas (2024). Clin Transl Oncol. 2024.
- 📄 Gomez-Brouchet A, et al. Assessment of resection margins in bone sarcoma treated with conservative surgery. Guías/consenso sobre márgenes y reporte.
Reconstrucción (referencias orientativas)
- 📄 Gitelis S, Piasecki P. Allograft prosthetic composite arthroplasty for aggressive bone tumors. Clin Orthop Relat Res. 1991;(270):197-201.
- 📄 Kotz R, Dominkus M, et al. Advances in bone tumour treatment in children. J Bone Joint Surg Br. 2002;84(3):401-406.
