Tomografía Computarizada (TC) en Tumores Musculoesqueléticos — Actualización 2026: técnica de elección para valorar la mineralización de la matriz, la integridad cortical y el screening pulmonar metastásico
La tomografía computarizada (TC) es una técnica de imagen transversal que, junto con la resonancia magnética, constituye la base de la estadificación local y a distancia de los tumores musculoesqueléticos. Su principal ventaja reside en la excelente resolución espacial para valorar estructuras óseas, permitiendo detectar con precisión la destrucción cortical, la reacción perióstica y, especialmente, la mineralización de la matriz tumoral (osteoide, condroide). Es insustituible para la detección de metástasis pulmonares, donde supera en sensibilidad a la radiografía simple. La Actualización 2026 enfatiza la importancia de realizar la TC con contraste intravenoso para evaluar la vascularización tumoral y su relación con los grandes vasos, la necesidad de adquirir imágenes con ventana ósea y de partes blandas, y la utilidad de la TC en la planificación quirúrgica (nivel de resección, reconstrucciones protésicas) y en la detección de recidivas. La TC debe realizarse siempre antes de la biopsia para evitar artefactos por hematoma y planificar correctamente el procedimiento.
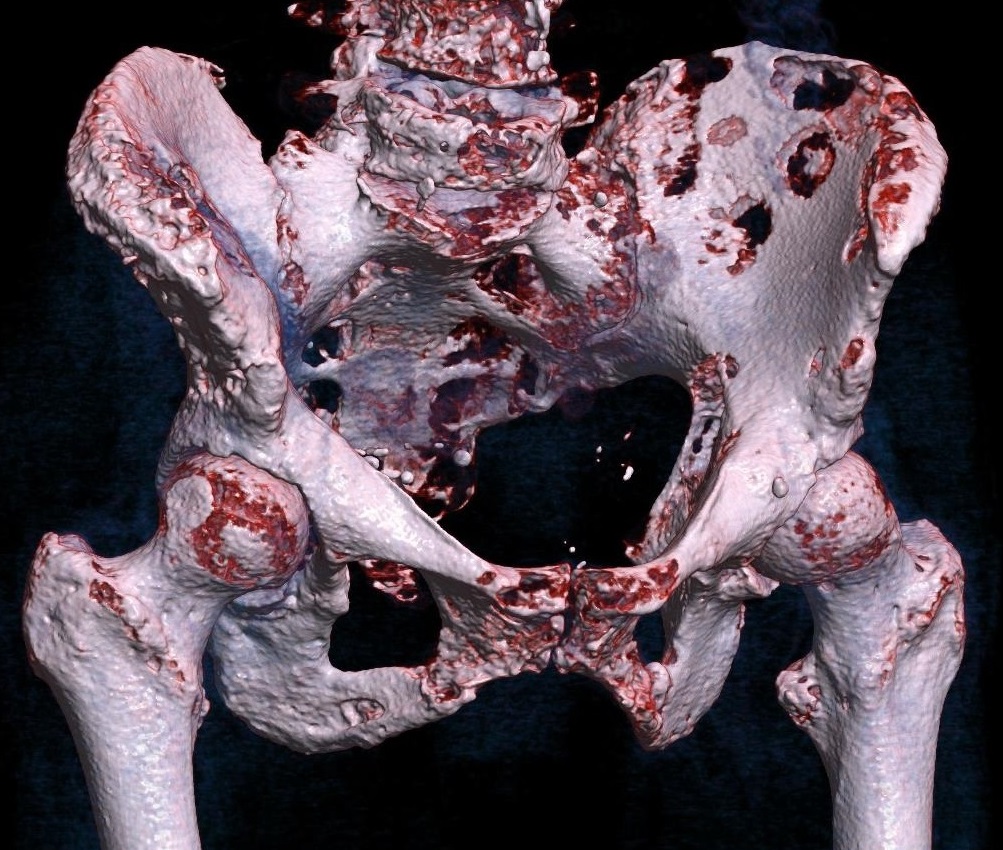
Hallazgo radiológico característico
0) En 1 minuto
- ✅ Qué es: La tomografía computarizada (TC) es una técnica de imagen que utiliza rayos X para obtener imágenes transversales de alta resolución. Es fundamental en la evaluación de tumores óseos por su capacidad para mostrar la estructura ósea con gran detalle.
- ✅ Utilidad principal:
- 🔹 Valoración de la matriz tumoral: Detecta mineralización (osteoide, condroide) que ayuda al diagnóstico diferencial.
- 🔹 Destrucción cortical: Evalúa con precisión la integridad de la cortical, la permeación y las fracturas patológicas ocultas.
- 🔹 Extensión tumoral: Define la extensión intraósea (canal medular) y a partes blandas, así como la relación con vasos y vísceras.
- 🔹 Detección de metástasis pulmonares: Es la técnica de elección, con mayor sensibilidad que la radiografía simple.
- ✅ Debe realizarse siempre antes de la biopsia para evitar artefactos por hematoma y planificar el trayecto.
- ✅ Limitaciones: Menor resolución de contraste en partes blandas que la RM, artefactos por material metálico, radiación ionizante.
Pitfall: El error más grave es no realizar la TC antes de la biopsia. El hematoma post-biopsia puede distorsionar la imagen, dificultando la evaluación de la extensión tumoral real y la planificación quirúrgica. Otro error es no utilizar ventana ósea y de partes blandas en la misma exploración, perdiendo información crucial sobre la cortical y la matriz tumoral. Finalmente, la TC no sustituye a la RM para valorar la extensión intramedular y la relación con estructuras neurovasculares; ambas son complementarias.
1) Conceptos
1.1 Principios básicos
La TC utiliza radiación ionizante para obtener imágenes en cortes axiales que posteriormente pueden reconstruirse en planos sagital, coronal o 3D. La densidad de los tejidos se mide en unidades Hounsfield (UH), lo que permite caracterizar lesiones (grasa: -50 a -100 UH, líquido: 0 UH, calcificaciones: >100 UH).
En tumores musculoesqueléticos, la TC debe realizarse siempre con contraste intravenoso para evaluar la vascularización tumoral y la relación con los grandes vasos, y con adquisiciones en ventana ósea (para valorar la cortical y la matriz) y ventana de partes blandas (para evaluar la extensión extraósea).
1.2 Importancia de la TC pre-biopsia
- ✅ La TC debe realizarse antes de cualquier procedimiento invasivo (biopsia).
- ✅ El hematoma post-biopsia puede falsear la lectura de la imagen, dificultando la evaluación de la extensión real del tumor y la planificación quirúrgica.
- ✅ Además, la TC pre-biopsia permite planificar el trayecto de la biopsia (evitando necrosis, eligiendo la zona más representativa y el abordaje más seguro).
2) Indicaciones en tumores musculoesqueléticos
2.1 Evaluación de la lesión primaria
- 🔹 Valoración de la matriz tumoral:
- 🔹 Matriz osteoide: Calcificaciones densas, amorfas, algodonosas (osteosarcoma).
- 🔹 Matriz condroide: Calcificaciones en anillos o arcos (condrosarcoma).
- 🔹 Matriz fibrosa: Generalmente sin calcificaciones (fibrosarcoma).
- 🔹 Destrucción cortical: La TC es superior a la RM para detectar erosión, permeación o rotura cortical. Permite distinguir entre lesiones intraóseas y aquellas con extensión extraósea.
- 🔹 Reacción perióstica: Visualiza patrones como el triángulo de Codman, en capas de cebolla o en rayos de sol.
- 🔹 Extensión intraósea: Aunque la RM es superior para medir la extensión longitudinal en la médula, la TC puede ser útil en localizaciones complejas (pelvis, sacro).
- 🔹 Extensión a partes blandas: La TC con contraste delimita la masa tumoral y su relación con estructuras vecinas.
- 🔹 Relaciones vasculares y viscerales: Fundamental en tumores de tronco, raíces de extremidades y retroperitoneo.
2.2 Localizaciones complejas
- 🔹 Tumores del tronco, pelvis y raíces de extremidades: La TC es a menudo indispensable para evaluar la extensión y planificar la cirugía.
- 🔹 Tumores yuxtacorticales: Ayuda a distinguir entre formas periósticas, parosteales y centrales (osteosarcoma yuxtacortical vs. convencional).
- 🔹 Niños pequeños: Menos útil que en adultos por la menor definición, pero puede ser necesaria en ciertos casos.
2.3 Estadificación a distancia
- 🔹 TC torácico: OBLIGATORIO en todos los sarcomas óseos y de partes blandas. Es la técnica de elección para detectar metástasis pulmonares, con una sensibilidad muy superior a la radiografía simple. Debe realizarse con cortes finos (≤1-2 mm) y reconstrucciones multiplanares.
- 🔹 TC abdominal: Indicada en sarcomas retroperitoneales, liposarcomas de extremidad (pueden metastatizar a retroperitoneo) y en ciertos subtipos con tendencia a metástasis hepáticas (leiomiosarcoma).
2.4 Seguimiento y detección de recidivas
- 🔹 La TC puede ser útil para controlar la aparición de recidivas locales tras resección ósea, especialmente en localizaciones donde la RM es difícil de interpretar por artefactos metálicos.
- 🔹 También permite evaluar la respuesta a la quimioterapia y radioterapia (cambios en el tamaño, necrosis, calcificaciones).
| Indicación | Utilidad principal |
|---|---|
| Matriz tumoral | Identificar mineralización osteoide (densa, amorfa) vs. condroide (anillos, arcos). |
| Destrucción cortical | Evaluar erosión, permeación, rotura y fracturas patológicas ocultas. |
| Extensión tumoral | Delimitar extensión intraósea (canal medular) y a partes blandas. Relación con vasos y vísceras. |
| Localizaciones complejas | Tronco, pelvis, raíces de extremidades, tumores yuxtacorticales. |
| Estadificación | TC torácico (metástasis pulmonares). TC abdominal (metástasis hepáticas, retroperitoneales). |
| Seguimiento | Detección de recidivas locales (especialmente con material metálico) y evaluación de respuesta a tratamiento. |
3) Técnica y adquisición
- ✅ Contraste intravenoso: Debe administrarse siempre para evaluar la vascularización tumoral, la relación con los grandes vasos y para caracterizar mejor las masas de partes blandas.
- ✅ Ventanas de adquisición:
- 🔹 Ventana ósea: Para valorar la cortical, la matriz tumoral y la reacción perióstica.
- 🔹 Ventana de partes blandas: Para evaluar la extensión extraósea y la relación con estructuras vecinas.
- ✅ Cortes finos: En la lesión primaria, se recomiendan cortes de 1-2 mm para permitir reconstrucciones multiplanares de alta calidad.
- ✅ TC torácico: Debe realizarse con cortes finos (≤1 mm) y, si es posible, con sincronización respiratoria para evitar artefactos.
- ✅ Reconstrucciones 3D: Útiles para planificación quirúrgica, especialmente en tumores pélvicos o de localización compleja.
4) Hallazgos por tipo de tumor
| Tipo de tumor | Hallazgos en TC |
|---|---|
| Osteosarcoma | Matriz osteoide densa, amorfa, algodonosa. Destrucción cortical agresiva. Reacción perióstica (triángulo de Codman, rayos de sol). Masa de partes blandas con calcificaciones. |
| Condrosarcoma | Matriz condroide con calcificaciones en anillos, arcos o floculentas. Expansión ósea. Puede haber masa de partes blandas. |
| Sarcoma de Ewing | Lesión lítica permeativa, sin matriz. Gran masa de partes blandas. Reacción perióstica laminar ("en capas de cebolla"). |
| Tumor de células gigantes | Lesión lítica excéntrica, metafisoepifisaria, sin matriz. Puede tener erosión cortical pero generalmente bien delimitada. |
| Metástasis líticas | Áreas de destrucción ósea, sin matriz. Pueden ser únicas o múltiples. |
| Metástasis blásticas | Áreas de aumento de densidad ósea (próstata, mama). |
5) Limitaciones y falsos positivos
- ⚠️ Menor resolución de contraste en partes blandas: La RM es superior para delimitar la extensión intramedular, la afectación de partes blandas y la relación con estructuras neurovasculares.
- ⚠️ Artefactos por material metálico: La presencia de prótesis, placas o tornillos degrada la imagen. No obstante, los equipos modernos disponen de algoritmos de reducción de artefactos metálicos.
- ⚠️ Radiación ionizante: Especialmente relevante en niños y adultos jóvenes. Debe optimizarse la dosis (protocolos pediátricos).
- ⚠️ Falsos positivos:
- 🔹 Extensión tumoral en canal medular: Puede ser simulada por edema o hemorragia medular postraumática o post-biopsia.
- 🔹 Metástasis pulmonares: Pueden confundirse con nódulos de atelectasia, fibrosis o granulomas.
6) Algoritmo de uso de TC en sarcomas
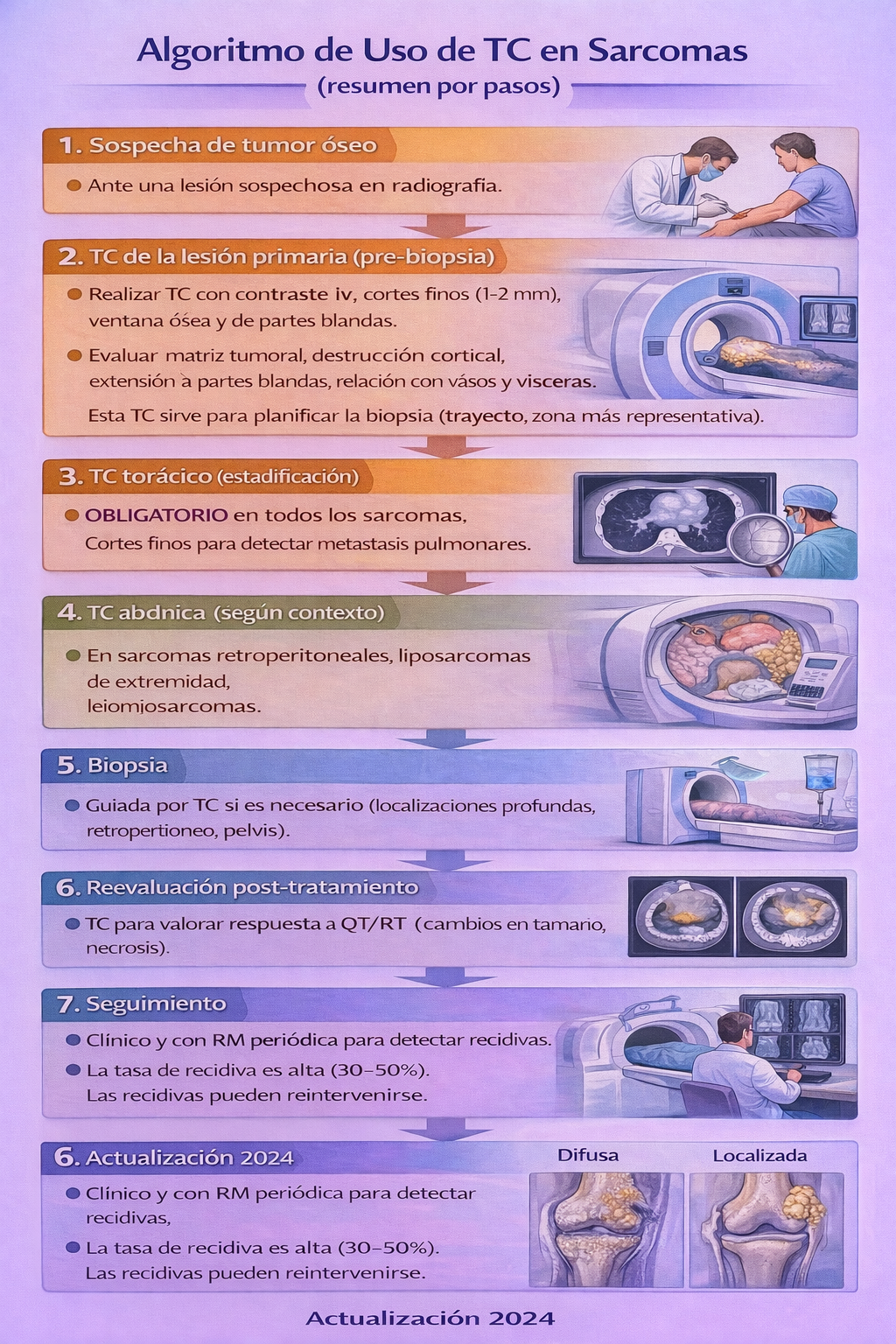
Resumen para la práctica clínica
📌 Indicaciones
- ✅ TC con contraste de la lesión primaria (pre-biopsia) para evaluar matriz tumoral, destrucción cortical y extensión a partes blandas.
- ✅ TC torácico de alta resolución para detección de metástasis pulmonares en todos los sarcomas.
- ✅ TC abdominal en sarcomas retroperitoneales, liposarcomas de extremidad y leiomiosarcomas.
🔧 Técnica
- 🔧 TC helicoidal multicorte con cortes finos (≤2 mm).
- 🔧 Administración de contraste intravenoso (excepto contraindicación).
- 🔧 Adquisición con ventana ósea y de partes blandas. Reconstrucciones multiplanares y 3D en casos seleccionados.
⚠️ Riesgos
- ⚠️ Exposición a radiación ionizante (especialmente en niños).
- ⚠️ Reacciones alérgicas al contraste yodado.
- ⚠️ Nefrotoxicidad por contraste (en pacientes con insuficiencia renal).
- ⚠️ Artefactos por material metálico (prótesis, implantes).
✅ Resultados
- ✅ Sensibilidad >95% para detectar metástasis pulmonares.
- ✅ Alta especificidad para caracterizar matriz tumoral (osteoide vs. condroide).
7) Bibliografía
Referencias clave
- 📄 Panicek DM, Gatsonis C, Rosenthal DI, et al. CT and MR imaging in the local staging of primary malignant musculoskeletal neoplasms: Report of the Radiology Diagnostic Oncology Group. Radiology. 1997;202(1):237-246.
- 📄 Meyer JS, Nadel HR, Marina N, et al. Imaging guidelines for children with Ewing sarcoma and osteosarcoma: a report from the Children's Oncology Group Bone Tumor Committee. Pediatr Blood Cancer. 2008;51(2):163-170.
- 📄 Saifuddin A, Sharif B, Gerrand C, Whelan J. The current status of MRI in the pre-operative assessment of intramedullary conventional appendicular osteosarcoma. Skeletal Radiol. 2019;48(4):503-516. (Incluye comparación con TC).
Técnica y protocolos
- 📄 Murphey MD, Kransdorf MJ, Smith SE. Imaging of musculoskeletal tumors. Radiol Clin North Am. 2011;49(6):1143-1165.
