Resonancia Magnética (RM) en Tumores Musculoesqueléticos — Actualización 2026: valoración de extensión intraósea y de partes blandas, relación con estructuras neurovasculares y planificación quirúrgica
La resonancia magnética (RM) constituye, junto con la tomografía computarizada (TC), el avance más importante en la evaluación y estadificación de los tumores musculoesqueléticos. Ofrece la caracterización anatómica más precisa de cualquier método de imagen, permitiendo una excelente diferenciación entre tejido sano y patológico. Su capacidad multiplanar y su alto contraste tisular la convierten en la técnica de elección para valorar la extensión local de sarcomas óseos y de partes blandas, incluyendo la afectación intraósea (extensión longitudinal, skip metástasis), la relación con estructuras neurovasculares y articulaciones, y la delimitación de compartimentos anatómicos. La Actualización 2026 enfatiza el uso de secuencias avanzadas (difusión, perfusión) para mejorar la caracterización tumoral y la evaluación de respuesta a la quimioterapia neoadyuvante, así como el papel de la RM en la detección precoz de recidivas y en la distinción entre tumor residual y cambios post-tratamiento (fibrosis, edema, necrosis). La RM es indispensable para la planificación de cirugías preservadoras de extremidad y para el seguimiento a largo plazo.
Hallazgo radiológico característico
0) En 1 minuto
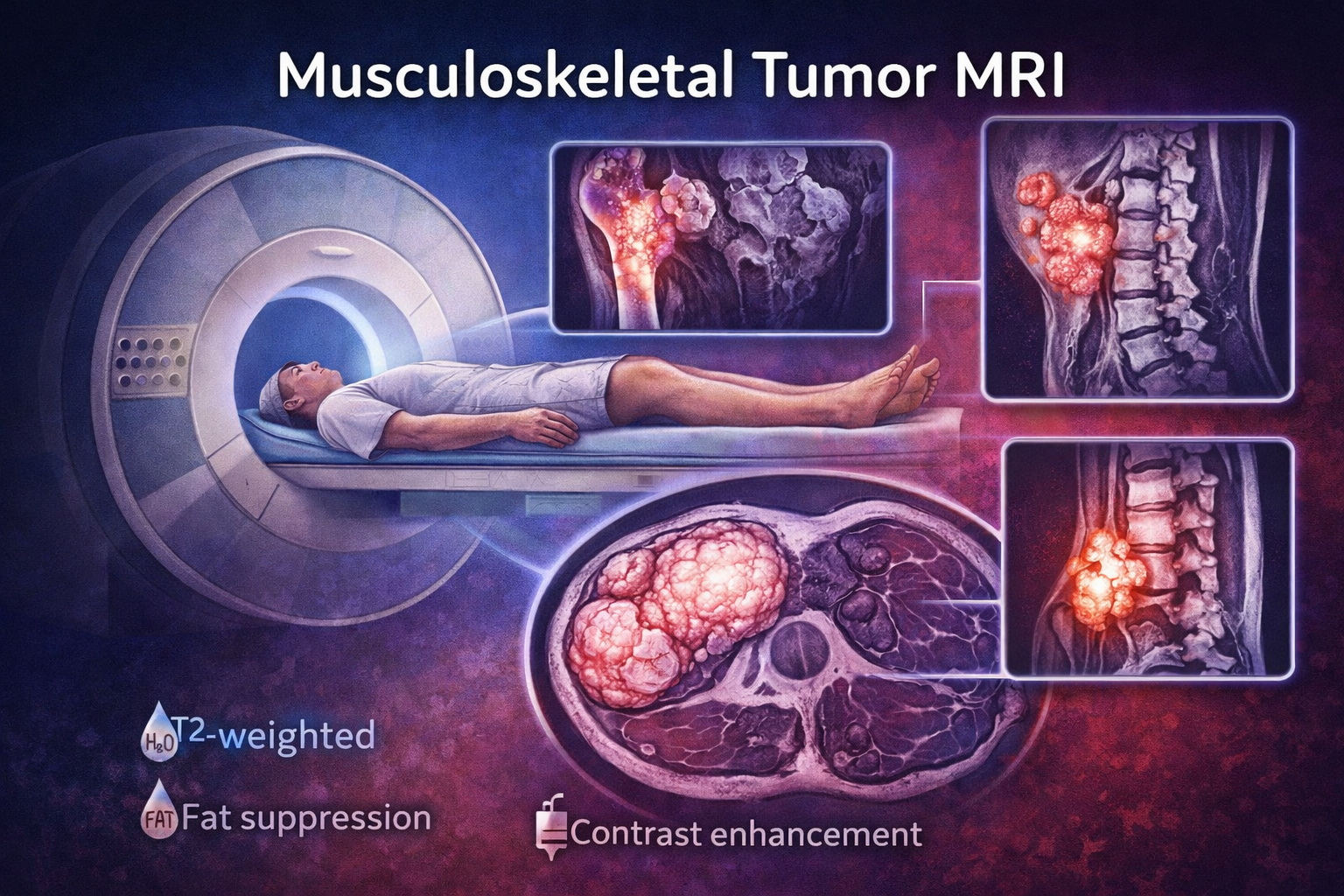
- ✅ Qué es: La resonancia magnética (RM) es la técnica de imagen de elección para la estadificación local de sarcomas óseos y de partes blandas. Proporciona un contraste tisular excepcional y permite la adquisición multiplanar (axial, coronal, sagital).
- ✅ Utilidad principal:
- 🔹 Extensión intraósea: Determina con precisión la longitud de afectación de la médula ósea (fundamental para planificar el nivel de resección).
- 🔹 Skip metástasis: Detecta focos tumorales separados del tumor primario.
- 🔹 Extensión a partes blandas: Evalúa el tamaño de la masa, su relación con el paquete vasculonervioso y los compartimentos musculares.
- 🔹 Relación con articulaciones y fisis: Ayuda a decidir el tipo de resección y reconstrucción.
- ✅ Secuencias básicas: T1 (anatomía, médula grasa), T2 con supresión grasa/STIR (edema, tumor), T1 con contraste (realce, necrosis, viabilidad tumoral).
- ✅ Limitaciones: Baja especificidad para diferenciar tipos histológicos (muchos tumores son hipointensos en T1 e hiperintensos en T2). Dificultad para distinguir tumor viable de cambios post-tratamiento (edema, inflamación, fibrosis). Artefactos por material metálico postquirúrgico.
Pitfall: El error más grave es no realizar una RM adecuada antes de la biopsia o la cirugía. Una RM incompleta (sin incluir toda la extensión del hueso, sin secuencias adecuadas) puede llevar a una planificación quirúrgica incorrecta, con márgenes inadecuados o imposibilidad de realizar cirugía preservadora. La RM debe incluir todo el hueso afectado (para descartar skip metástasis) y utilizar secuencias con supresión grasa para valorar correctamente el edema y la extensión tumoral. Además, la interpretación de los cambios post-tratamiento requiere una RM basal postquirúrgica (a los 3 meses) para comparaciones posteriores.
1) Conceptos básicos de RM en patología tumoral
1.1 Principios físicos y contraste tisular
La RM se basa en la detección de señales de protones (hidrógeno) sometidos a un campo magnético y pulsos de radiofrecuencia. Los diferentes tejidos tienen distintos tiempos de relajación T1 y T2, lo que genera el contraste en las imágenes.
- 🔹 Secuencias potenciadas en T1: Tiempo de repetición (TR) corto y tiempo de eco (TE) corto. La grasa (médula ósea) aparece hiperintensa (blanca). El agua (tumor, edema, inflamación) aparece hipointensa (negra). Útiles para valorar anatomía y reemplazo de la grasa medular por tumor.
- 🔹 Secuencias potenciadas en T2: TR largo y TE largo. El agua (tumor, edema) aparece hiperintensa (blanca). La grasa aparece de intensidad intermedia o baja. Útiles para delimitar el tumor y el edema peritumoral.
- 🔹 Supresión grasa (STIR / Fat Sat): Anula la señal de la grasa, haciendo que el tumor y el edema (hiperintensos en T2) destaquen aún más. Esencial para valorar extensión tumoral y edema.
- 🔹 Contraste (Gadolinio): El tumor sólido viable realza tras la administración de contraste, mientras que las áreas necróticas, quísticas o fibróticas no realzan (o lo hacen escasamente). Ayuda a diferenciar tumor de edema y a guiar biopsias.
1.2 Ventajas de la RM frente a otras técnicas
- ✅ Visualización multiplanar: Permite obtener imágenes en planos axial, coronal, sagital y oblicuos, adaptándose a la anatomía y extensión tumoral.
- ✅ Excelente contraste tisular: Superior a la TC para diferenciar tejidos blandos (músculo, grasa, tumor, vasos, nervios).
- ✅ Sin radiación ionizante: Inocua para el paciente (aunque con contraindicaciones como marcapasos, ciertos implantes metálicos).
- ✅ Útil en presencia de implantes metálicos (no ferromagnéticos): Aunque producen artefactos, la RM puede ser útil en algunos casos (la TC es mejor para valorar detalles óseos).
- ✅ Valoración de la médula ósea: Detecta precozmente el reemplazo de la grasa medular por tumor (mejor que la TC).
2) Técnicas y secuencias en la práctica clínica
2.1 Protocolo estándar para sarcomas óseos y de partes blandas
- 🔹 Campo de visión (FOV) amplio: Debe incluir toda la extensión del hueso afectado (para descartar skip metástasis) y la articulación proximal y distal.
- 🔹 Secuencias obligatorias:
- 🔹 T1 sin contraste: En plano coronal (para valorar extensión longitudinal) y axial (anatomía).
- 🔹 T2 con supresión grasa o STIR: En planos coronal y axial (para delimitar tumor y edema).
- 🔹 T1 con supresión grasa tras contraste: En planos axial y sagital/coronal (para valorar viabilidad tumoral, necrosis y relación con vasos).
- 🔹 Secuencias avanzadas (opcionales):
- 🔹 Difusión (DWI): La restricción de la difusión (bajo ADC) se correlaciona con alta celularidad tumoral. Puede ayudar a diferenciar tumor viable de necrosis y a evaluar respuesta a QT.
- 🔹 Perfusión (DCE-MRI): Evalúa la vascularización tumoral. Cambios en la perfusión pueden predecir respuesta a QT neoadyuvante.
3) Aplicaciones clínicas por tipo de tumor
| Tipo de tumor | Utilidad de la RM | Comentarios |
|---|---|---|
| Tumores óseos primarios (osteosarcoma, sarcoma de Ewing, condrosarcoma) | Estadificación local: extensión intraósea (longitud), skip metástasis, extensión a partes blandas, relación con fisis y articulación, afectación neurovascular. | La TC es superior para valorar matriz tumoral calcificada/osteoblástica. La RM es esencial para planificar cirugía preservadora. |
| Tumores de partes blandas (sarcomas, tumores benignos) | Técnica de elección. Delimita tamaño, extensión, relación con fascias, músculos y paquete neurovascular. Ayuda a caracterizar (grasa, quistes, etc.). | Baja especificidad para diferenciar sarcomas de alto grado de lesiones benignas. La biopsia es necesaria. |
| Tumores de columna | Detecta reemplazo de la médula grasa por tumor (hipointenso en T1, hiperintenso en T2/STIR). Evalúa extensión epidural y afectación de partes blandas paravertebrales. | Muy sensible para metástasis vertebrales. La TC es mejor para valorar destrucción cortical. |
| Metástasis óseas | Alta sensibilidad para detectar metástasis medulares (reemplazo graso). Útil para evaluar respuesta al tratamiento. | La gammagrafía ósea y la PET-TC tienen otras indicaciones complementarias. |
3.1 Tumores de partes blandas: consideraciones específicas
- 🔹 La RM es el estudio de elección para la evaluación de tumores de partes blandas. En la mayoría de los casos identifica, delinea y estadifica estos tumores mejor que la TC.
- 🔹 La mayoría de los sarcomas se presentan como masas hipointensas en T1 (similar al músculo) e hiperintensas en T2, con realce heterogéneo tras contraste.
- 🔹 Las lesiones con contenido graso (lipomas, liposarcomas bien diferenciados) se identifican por su alta señal en T1 y pérdida de señal con supresión grasa.
- 🔹 Las lesiones intramusculares se visualizan mejor en secuencias T2 con supresión grasa.
- 🔹 Limitación: La especificidad de la RM es pobre, ya que muchos tumores (benignos y malignos) tienen patrones de señal similares. No puede reemplazar a la biopsia.
3.2 Tumores óseos: planificación quirúrgica
- 🔹 La RM es fundamental para planificar la cirugía de salvamento de extremidad, proporcionando información sobre:
- 🔹 Distancia desde el extremo proximal del tumor a la articulación: Determina el nivel de resección ósea.
- 🔹 Relación con el paquete vasculonervioso: Decide si es posible la preservación o si se requiere resección y reconstrucción vascular.
- 🔹 Afectación de la fisis: Crucial en pacientes esqueléticamente inmaduros.
- 🔹 La detección de skip metástasis (focos tumorales separados del tumor primario) contraindica la cirugía preservadora convencional.
4) Hallazgos por localización anatómica
4.1 Columna vertebral
- 🔹 La médula ósea normal (grasa) es hiperintensa en T1. La infiltración tumoral (metástasis, mieloma, sarcomas) reemplaza la grasa, apareciendo como áreas hipointensas en T1 e hiperintensas en T2/STIR.
- 🔹 La RM es muy útil para evaluar la extensión epidural y la compresión medular, información crucial para la planificación quirúrgica o radioterápica.
- 🔹 El edema peritumoral y la fractura patológica también son bien valorados.
4.2 Huesos largos (fémur, tibia, húmero)
- 🔹 La secuencia T1 coronal es la más útil para medir la extensión longitudinal del tumor dentro de la médula ósea.
- 🔹 La extensión a partes blandas se valora mejor en T2 con supresión grasa o STIR.
- 🔹 La relación con la fisis y la articulación adyacente debe describirse con precisión.
4.3 Pelvis y cinturas escapulares
- 🔹 La RM es especialmente valiosa en estas localizaciones complejas, donde la anatomía tridimensional es difícil de evaluar con otras técnicas.
- 🔹 Ayuda a determinar la resecabilidad de tumores pélvicos (relación con vasos ilíacos, nervios sacros, vísceras).
5) Seguimiento post-tratamiento: detección de recidiva y cambios post-terapia
- ✅ RM basal post-tratamiento: Se recomienda realizar una RM de control aproximadamente a los 3 meses de la cirugía o de finalizar la radioterapia. Esta imagen sirve como línea base para comparaciones futuras.
- ✅ Cambios post-quirúrgicos y post-radioterapia:
- 🔹 Edema/Inflamación: Áreas hiperintensas en T2/STIR, que pueden persistir durante meses. Disminuyen gradualmente.
- 🔹 Fibrosis: Áreas hipointensas en T2, sin realce significativo tras contraste. Es un signo de buena evolución, aunque no excluye completamente la presencia de tumor residual microscópico.
- 🔹 Hemosiderina: Depósitos de sangre degradada, hipointensos en T2 (especialmente en secuencias de eco de gradiente).
- 🔹 Cambios en médula ósea irradiada: Aumento de la señal en T1 por reemplazo graso de la médula.
- ✅ Sospecha de recidiva:
- 🔹 Debe sospecharse ante la aparición de un nuevo nódulo o masa con realce, o un aumento focal de la señal en T2 con realce asociado, en el contexto de un estudio basal previo.
- 🔹 El crecimiento de una lesión en estudios sucesivos es muy sospechoso.
- 🔹 La RM tiene alta sensibilidad para detectar recidivas, pero especificidad limitada (puede ser difícil diferenciar tumor de cambios inflamatorios/fibróticos). La RM con contraste dinámico y difusión pueden ayudar.
- 🔹 La biopsia puede ser necesaria para confirmar la recidiva.
6) Algoritmo de uso de RM en sarcomas
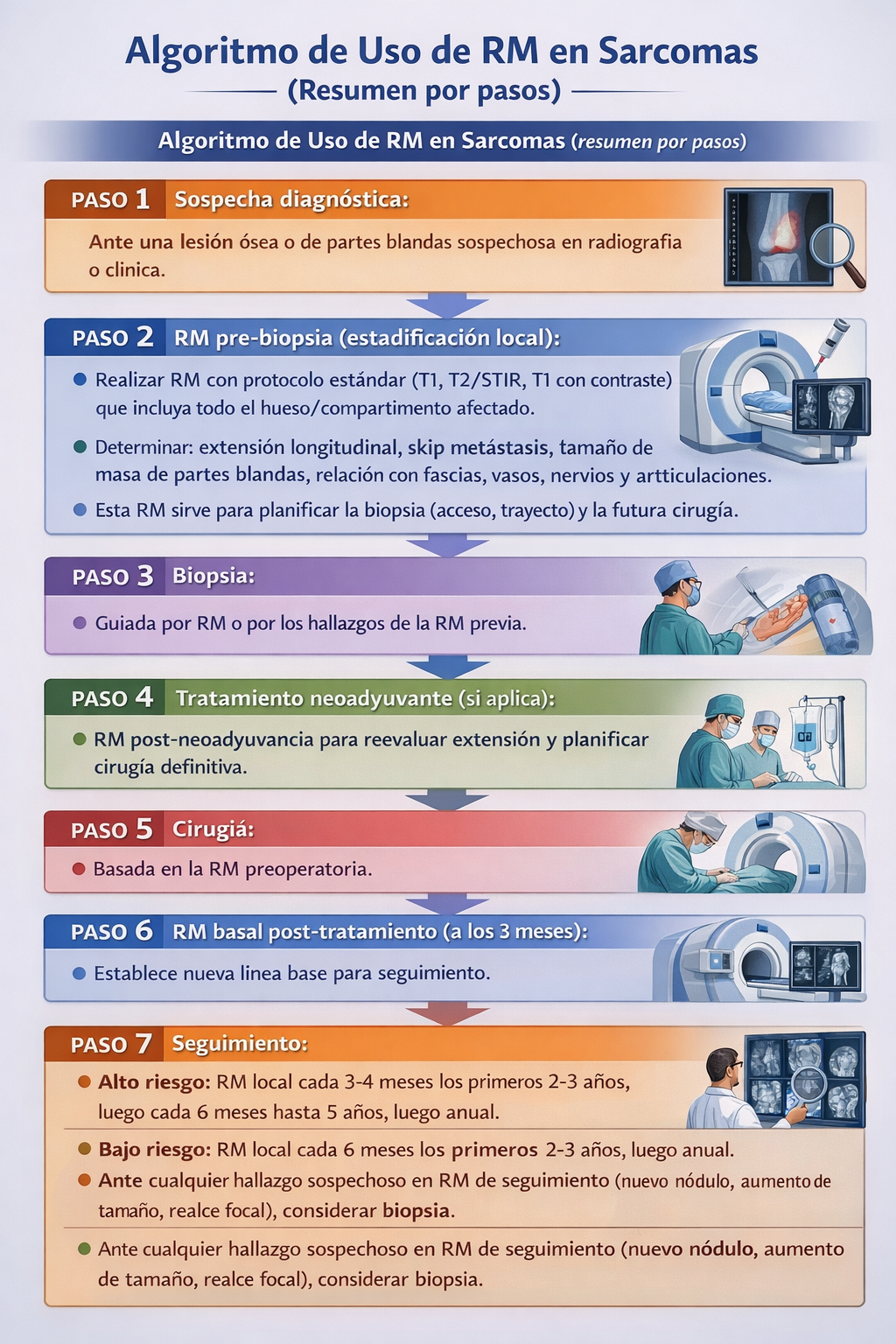
Resumen para la práctica clínica
📌 Indicaciones
- ✅ RM con contraste para estadificación local pre-tratamiento de sarcomas óseos y de partes blandas.
- ✅ RM para planificación quirúrgica (nivel de resección, relación neurovascular, afectación articular).
- ✅ RM de seguimiento para detección precoz de recidivas (con RM basal post-tratamiento a los 3 meses).
🔧 Técnica
- 🔧 Protocolo: T1 coronal (extensión), T2/STIR axial y coronal (edema/tumor), T1 con supresión grasa tras contraste axial y sagital (viabilidad).
- 🔧 Incluir todo el hueso afectado y articulaciones adyacentes en el FOV.
- 🔧 Secuencias avanzadas (DWI, perfusión) en casos seleccionados (respuesta a QT, diagnóstico diferencial).
⚠️ Riesgos
- ⚠️ Artefactos por movimiento o material metálico (prótesis, clips).
- ⚠️ Contraindicaciones: marcapasos, implantes ferromagnéticos, claustrofobia severa.
- ⚠️ Reacciones alérgicas al contraste de gadolinio (raras).
- ⚠️ Nefrogenic systemic fibrosis (en pacientes con insuficiencia renal avanzada).
✅ Resultados
- ✅ Sensibilidad >90% para detectar extensión tumoral local y recidivas.
- ✅ Especificidad moderada (60-80%) para diferenciar tumor viable de cambios post-tratamiento (mejora con secuencias dinámicas y DWI).
7) Bibliografía
Referencias clave
- 📄 Stacy GS, Mahal RS, Peabody TD. Staging of bone tumors: a review with illustrative examples. AJR Am J Roentgenol. 2006;186(4):967-976.
- 📄 Kransdorf MJ, Murphey MD. Imaging of Bone Tumors and Tumor-Like Lesions. Philadelphia: Saunders; 2009.
- 📄 Panicek DM, Gatsonis C, Rosenthal DI, et al. CT and MR imaging in the local staging of primary malignant musculoskeletal neoplasms: Report of the Radiology Diagnostic Oncology Group. Radiology. 1997;202(1):237-246.
- 📄 Vanel D, Verstraete KL, Shapeero LG. Primary tumors of the musculoskeletal system. Radiol Clin North Am. 1997;35(1):213-237.
Seguimiento y recidiva
- 📄 Vanel D, Lacombe MJ, Couanet D, et al. Musculoskeletal tumors: follow-up with MR imaging after treatment with surgery and radiation therapy. Radiology. 1987;164(1):243-245.
- 📄 Del Grande F, Subhawong T, Weber K, et al. Detection of soft-tissue sarcoma recurrence: added value of diffusion-weighted imaging to conventional MRI. Radiology. 2014;271(2):525-533.
