🩸 Mieloma múltiple — Actualización 2026: diagnóstico (SLiM-CRAB), estadificación (R-ISS) y tratamiento actual
El mieloma múltiple es una neoplasia de células plasmáticas caracterizada por proliferación clonal en médula ósea y producción de inmunoglobulina monoclonal (proteína M) y/o cadenas ligeras libres. Su expresión clínica típica se resume en CRAB (hipercalcemia, insuficiencia renal, anemia y lesiones óseas), pero desde la actualización del IMWG el diagnóstico de mieloma activo puede establecerse también con biomarcadores de muy alto riesgo de progresión (SLiM), permitiendo tratar antes de que aparezca daño orgánico irreversible. El abordaje moderno integra imagen de alta sensibilidad (WB-LDCT, PET-TC, RM cuerpo entero), citogenética/FISH, valoración de fragilidad, terapias combinadas con anti-CD38 e inmunoterapias (CAR-T y biespecíficos en recaída), además de medidas de soporte para enfermedad ósea, trombosis e infecciones.
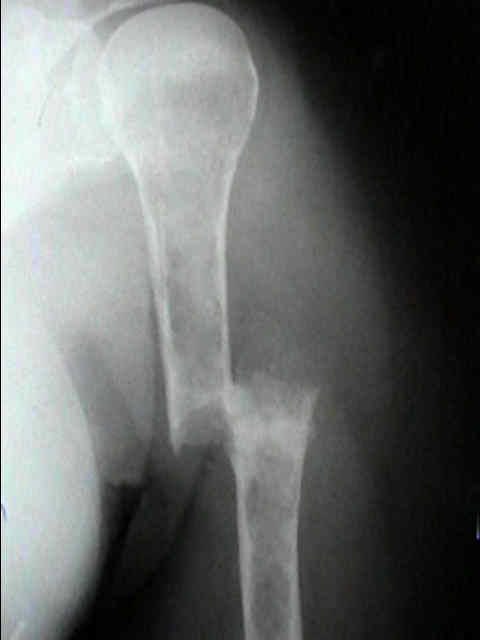
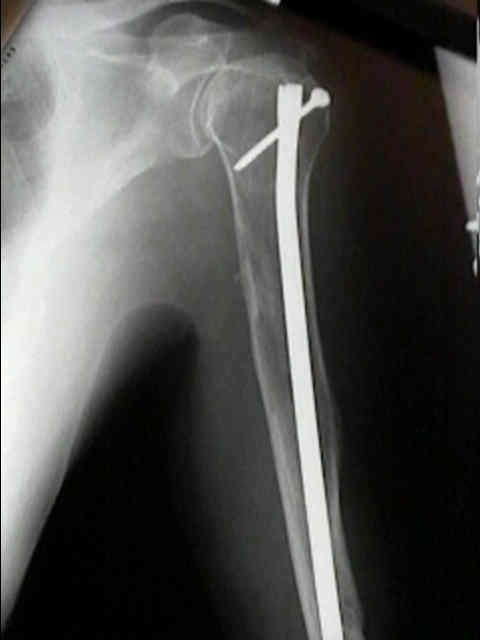
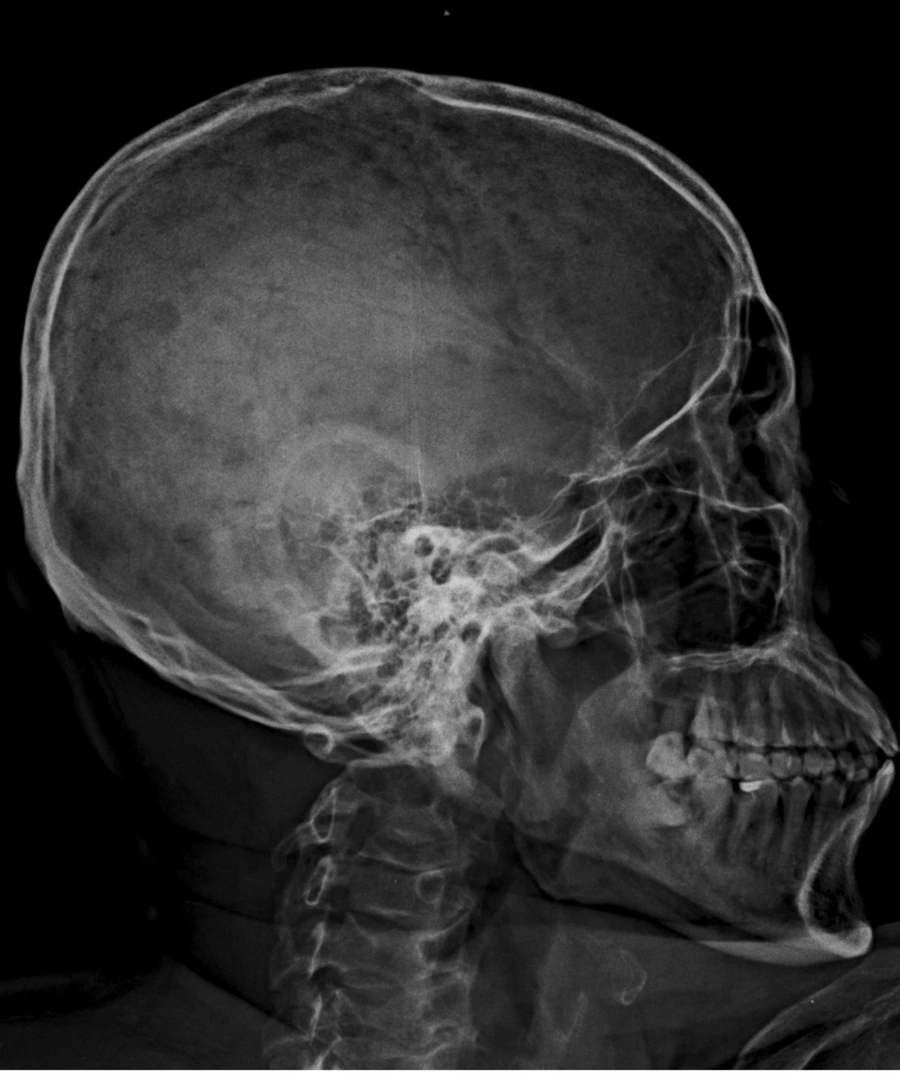
Hallazgo radiológico característico
0) En 1 minuto
- ✅ Qué es: Neoplasia clonal de células plasmáticas con infiltración medular y producción de proteína monoclonal (suero y/o orina).
- ✅ Cuándo “es activo” y hay que tratar: Células plasmáticas clonales ≥10% (o plasmocitoma) + evento definitorio: CRAB o biomarcadores SLiM (alto riesgo de progresión).
- ✅ Pruebas clave iniciales: Hemograma, creatinina/FG, calcio, albúmina, β2-microglobulina, LDH; electroforesis + inmunofijación en suero/orina; cadenas ligeras libres séricas; aspirado/biopsia médula ósea + FISH; imagen de cuerpo entero (WB-LDCT / PET-TC / RM).
- ✅ Riesgo: R-ISS (ISS + LDH + citogenética). Alteraciones de alto riesgo típicas: del(17p), t(4;14), t(14;16) (y con frecuencia ganancia/amplificación 1q).
- ✅ Tratamiento moderno (esquema general): combinaciones tripletes/cuádruples (incl. anti-CD38) ± trasplante autólogo según elegibilidad, y mantenimiento (habitualmente lenalidomida; individualizar en alto riesgo).
- ✅ Soporte imprescindible: prevención de eventos óseos (zoledronato/pamidronato o denosumab), profilaxis trombótica con IMiDs, prevención infecciosa/vacunal, salud renal y control del dolor.
1) Conceptos
1.1 Espectro de gammapatías monoclonales
| Entidad | Clon plasmático | Daño orgánico / evento definitorio | Conducta |
|---|---|---|---|
| MGUS | Bajo | No | Seguimiento |
| Mieloma indolente (SMM) | Intermedio/alto | No (sin MDE) | Seguimiento estrecho; en “alto riesgo”, individualizar |
| Mieloma múltiple activo | ≥10% o plasmocitoma | Sí (CRAB o SLiM) | Tratamiento |
| Plasmocitoma solitario | Lesión única | Sin criterios de mieloma sistémico | Radioterapia local ± cirugía; vigilancia |
1.2 Fisiopatología (resumen útil)
- Proteína monoclonal: IgG/IgA (frecuentes) o cadenas ligeras (Bence-Jones).
- Enfermedad ósea lítica: activación osteoclástica e inhibición osteoblástica → lesiones “en sacabocado”, fracturas y dolor.
- Daño renal: nefropatía por cilindros (cadenas ligeras), hipercalcemia, deshidratación, fármacos nefrotóxicos.
- Inmunodeficiencia: inmunoparesia + tratamientos → infecciones (sobre todo respiratorias).
2) Diagnóstico: criterios actuales (SLiM-CRAB)
2.1 Requisito de base
Se requiere células plasmáticas clonales en médula ósea ≥10% o plasmocitoma demostrado por biopsia, y al menos un evento definitorio de mieloma (MDE).
2.2 Eventos definitorios (MDE): CRAB + SLiM
| Grupo | Criterio | Umbral típico |
|---|---|---|
| CRAB | C Hipercalcemia atribuible al trastorno | >11 mg/dL o >1 mg/dL por encima del LSN |
| R Insuficiencia renal atribuible | ClCr <40 mL/min o creatinina >2 mg/dL | |
| A Anemia atribuible | Hb <10 g/dL o >2 g/dL por debajo del límite inferior | |
| B Lesiones óseas líticas / fracturas por compresión atribuibles | ≥1 lesión lítica (CT/PET-CT/WB-LDCT; típicamente ≥5 mm) | |
| SLiM | S (“Sixty”) plasmocitos clonales en MO | ≥60% |
| Li (“Light chains”) cociente cadenas ligeras libres | Involucrada/no involucrada ≥100 (con involucrada ≥100 mg/L) | |
| M (“MRI”) lesiones focales | >1 lesión focal en RM (habitualmente ≥5 mm) |
Nota: los umbrales pueden matizarse según el contexto clínico y la atribución causal (p. ej., anemia por otras causas).
2.3 Estudio diagnóstico mínimo recomendado
- Sangre: hemograma; creatinina/FG; calcio; albúmina; β2-microglobulina; LDH; proteínas totales; inmunoglobulinas.
- Monoclonalidad: electroforesis + inmunofijación (suero y orina) + cadenas ligeras libres séricas.
- Médula ósea: aspirado + biopsia; citometría; FISH (alto riesgo); (NGS si disponible).
- Imagen: WB-LDCT o PET-TC o RM de cuerpo entero (según disponibilidad/escenario).
3) Estadificación y estratificación de riesgo
3.1 ISS y R-ISS (lo más usado)
- ISS: basado en β2-microglobulina y albúmina.
- R-ISS: integra ISS + LDH + citogenética de alto riesgo (t(4;14), t(14;16), del(17p)).
| R-ISS | Qué combina | Idea clínica |
|---|---|---|
| I | ISS I + LDH normal + sin citogenética alto riesgo | Mejor pronóstico |
| II | No cumple criterios de I ni III | Intermedio |
| III | ISS III + (LDH alta y/o citogenética alto riesgo) | Peor pronóstico |
3.2 Marcadores de alto riesgo (prácticos)
- FISH (alto riesgo clásico): del(17p), t(4;14), t(14;16) (± t(14;20) según panel).
- Frecuente en riesgo aumentado: ganancia/amplificación 1q (interpretación según guías/centro).
- Otros: plasmoblastosis, LDH alta, extramedular, enfermedad de cadenas ligeras agresiva, etc.
4) Presentación clínica
- Dolor óseo (columna, costillas, pelvis), fracturas por fragilidad, pérdida de altura vertebral.
- Anemia y astenia; citopenias si infiltración importante.
- Infecciones (respiratorias) por inmunodeficiencia e hipogammaglobulinemia.
- Insuficiencia renal (desde asintomática a IRA).
- Hipercalcemia (náuseas, estreñimiento, confusión, poliuria).
- Neurología: radiculalgia/compresión medular; neuropatía (por enfermedad o tratamiento).
- Otros: síndrome de hiperviscosidad (raro), amiloidosis AL asociada, trombosis venosa (sobre todo con IMiDs).
5) Estudios de laboratorio
5.1 Perfil básico
- Hemograma: anemia normocítica frecuente; leucopenia/trombocitopenia si enfermedad avanzada.
- Bioquímica: creatinina/FG, urea, calcio, albúmina, LDH, ácido úrico.
- Marcadores de carga/prognóstico: β2-microglobulina, albúmina, LDH.
5.2 Detección y cuantificación del componente monoclonal
- Suero: electroforesis (SPEP) + inmunofijación; cuantificación Ig.
- Orina 24 h: electroforesis + inmunofijación (UPEP/IFE) si procede.
- Cadenas ligeras libres séricas: imprescindible, sobre todo en mieloma de cadenas ligeras/oligosecretor.
5.3 Otros (según escenario)
- Coagulación, ferritina/folato/B12 si anemia mixta, serologías, función tiroidea si precisa.
- Proteinuria, sedimento, y estudio de amiloidosis si sospecha (edemas, macroglosia, cardiopatía restrictiva, etc.).
6) Estudios de imagen
6.1 Qué se recomienda hoy
- WB-LDCT (TC cuerpo entero de baja dosis): más sensible que la serie ósea convencional para lesiones líticas.
- PET-TC (FDG): útil en enfermedad extramedular, evaluación de respuesta y lesiones activas.
- RM (columna o cuerpo entero): excelente para infiltración medular, lesiones focales y compresión medular.
La “serie ósea” clásica puede infraestimar enfermedad; se reserva a contextos concretos cuando no hay técnicas más sensibles.
6.2 Hallazgos típicos
- Radiología/TC: lesiones osteolíticas “en sacabocado”, osteopenia difusa, fracturas vertebrales.
- Gammagrafía ósea: puede ser poco sensible en lesiones puramente líticas (no es la prueba de elección).
- RM: infiltración difusa o focal; útil cuando hay dolor sin lesión evidente en radiografía.
7) Médula ósea, histología y citogenética
- Aspirado/biopsia: cuantificación de plasmocitos y confirmación de clonalidad (inmunofenotipo).
- Citometría: apoyo diagnóstico y, en centros, evaluación de enfermedad mínima residual (MRD).
- FISH: imprescindible para estratificación (del17p, t(4;14), t(14;16), etc.).
- Plasmocitoma: biopsia de la lesión si procede, especialmente si presentación focal/atípica.
8) Tratamiento (visión práctica 2026)
8.1 Principios
- Se individualiza por elegibilidad a trasplante autólogo, fragilidad, comorbilidades (renal/cardiaca/neuropatía), y riesgo biológico.
- Objetivos: respuesta profunda (idealmente MRD negativa cuando sea posible), control del dolor/óseo, preservar función renal y calidad de vida.
8.2 Esquema por escenarios (resumen)
| Escenario | Estrategia típica | Ejemplos (orientativos) |
|---|---|---|
| Nuevo diagnóstico, elegible a trasplante | Inducción (a menudo con anti-CD38) → aféresis → ASCT → consolidación/ mantenimiento | D-VRd / Isa-VRd / VRd; mantenimiento con lenalidomida (ajustar en alto riesgo) |
| Nuevo diagnóstico, no elegible | Tripletes/cuádruples adaptados a edad/fragilidad; duración según tolerancia/respuesta | D-Rd, D-VMP, VRd-lite, Rd (según perfil) |
| Recaída | Elegir según exposición previa y refractariedad (lenalidomida/anti-CD38/PI) | Tripletes con anti-CD38 o carfilzomib/pomalidomida; derivar a ensayos |
| Refractario avanzado | Inmunoterapias | CAR-T anti-BCMA y anticuerpos biespecíficos (BCMA/GPRC5D, etc.), según disponibilidad |
Nota: las combinaciones concretas dependen de aprobaciones locales, líneas previas, toxicidades y guías de tu entorno.
8.3 Soporte (no negociable)
- Trombosis: profilaxis si IMiDs (lenalidomida/pomalidomida) según riesgo.
- Infecciones: vacunación, profilaxis antiviral con inhibidores del proteasoma/anti-CD38 según protocolo; valorar IgIV en infecciones recurrentes + hipogammaglobulinemia.
- Hueso: antirresortivos + calcio/vitamina D si procede, dental previo (ver sección 9).
- Renal: hidratación, evitar nefrotóxicos, tratar hipercalcemia, control rápido de cadenas ligeras con terapia eficaz.
- Dolor: analgesia escalonada + radioterapia/cirugía cuando esté indicado.
9) Enfermedad ósea y ortopedia
9.1 Antirresortivos (IMWG)
Pilar del soporte: zoledronato/pamidronato o denosumab, con monitorización renal y prevención de osteonecrosis mandibular.
- Bisfosfonatos (zoledronato/pamidronato): recomendados en mieloma activo (incluso sin lesiones evidentes en imagen, según contexto).
- Denosumab: alternativa útil, especialmente si insuficiencia renal (vigilar hipocalcemia y suplementar).
- Dental: revisión y tratamiento dental antes de iniciar; evitar extracciones durante el tratamiento si es posible.
9.2 Procedimientos locales
- Radioterapia: dolor localizado, plasmocitoma, compresión medular (junto a otras medidas), control local.
- Vertebroplastia/cifoplastia: dolor vertebral por fractura/colapso sin compresión neurológica significativa.
- Cirugía ortopédica: fracturas patológicas, inestabilidad, lesiones de alto riesgo mecánico; planificación con imagen.
10) Complicaciones y urgencias frecuentes
10.1 Compresión medular
- Clínica: dolor dorsal + déficit motor/sensitivo, alteración esfínteres.
- Actitud: RM urgente, corticoides según protocolo, radioterapia y/o cirugía según estabilidad y lesión.
10.2 Insuficiencia renal
- Causas típicas: nefropatía por cilindros (cadenas ligeras), hipercalcemia, deshidratación, AINEs/contraste.
- Actitud: hidratación, evitar nefrotóxicos, tratar hipercalcemia, iniciar tratamiento antitumoral eficaz cuanto antes.
10.3 Hipercalcemia
- Actitud: hidratación IV, antirresortivos (zoledronato/denosumab según caso), calcitonina en casos seleccionados y control de la enfermedad.
10.4 Infecciones
- Evaluación precoz ante fiebre; umbral bajo para antibióticos en inmunodeprimidos.
- Profilaxis/vacunas según guías locales y fármacos usados (p. ej., riesgo de reactivación viral).
11) Seguimiento y respuesta
- Monitorización: proteína M (suero/orina), cadenas ligeras libres, hemograma, creatinina/FG, calcio, y clínica (dolor, infecciones).
- Respuesta: criterios IMWG (PR/VGPR/CR/sCR) y, si disponible, MRD (citometría/NGS) como marcador de profundidad.
- Imagen: repetir en dolor nuevo, sospecha de progresión ósea/extramedular o para evaluar lesiones metabólicamente activas (PET-TC).
En vida real, la supervivencia ha mejorado de forma marcada (en trasplante-elegibles suele superar 10 años), pero depende mucho del riesgo y del acceso a terapias. Datos poblacionales muestran una supervivencia relativa a 5 años alrededor del 60% en series recientes.
12) Algoritmo práctico (diagnóstico + primera decisión terapéutica)
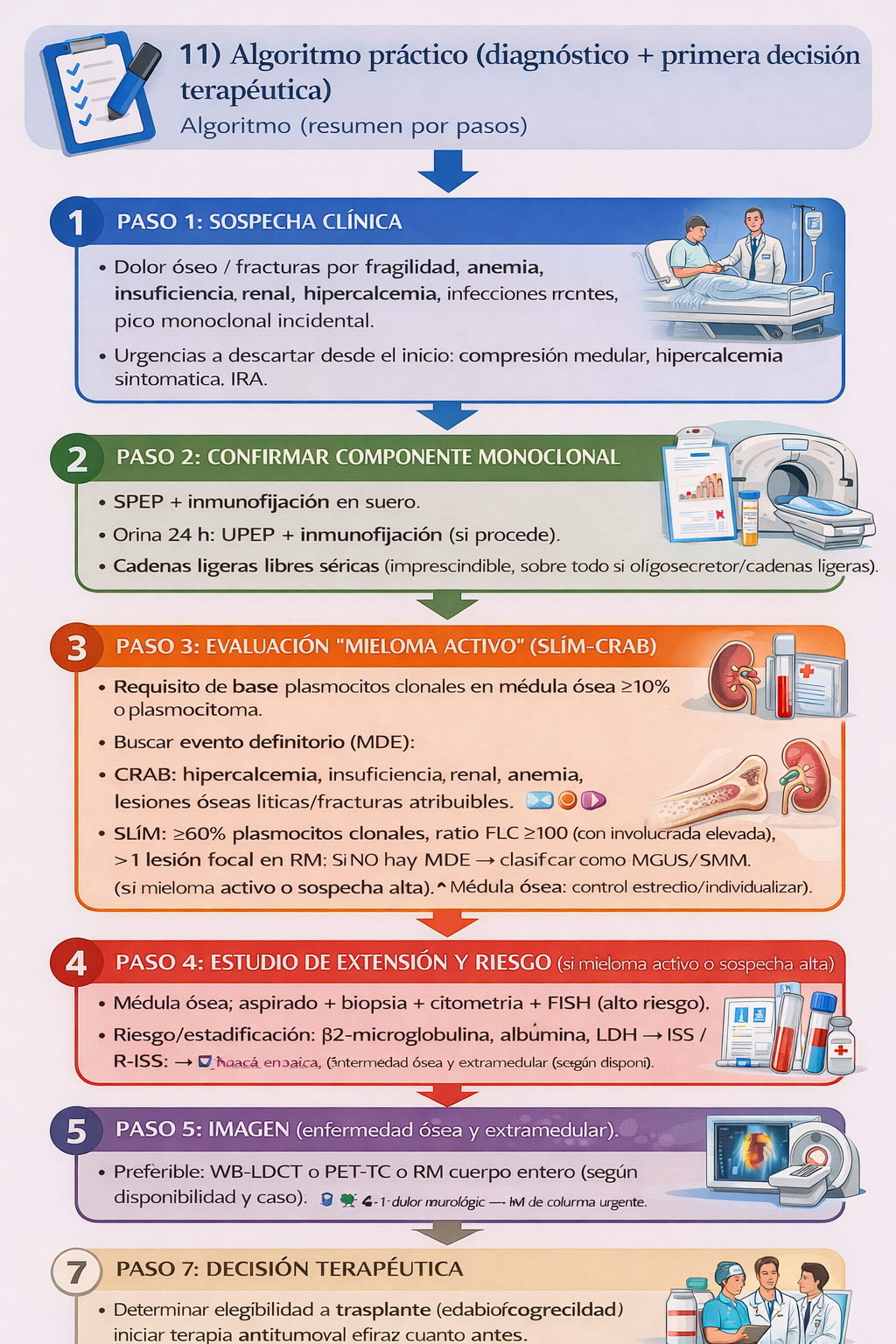
📌 Resumen para la práctica clínica
Indicaciones
- ✅ Confirmación de clonalidad (médula ósea o biopsia) y componente monoclonal (suero/orina + cadenas ligeras libres).
- ✅ Aplicar criterios SLiM-CRAB para decidir si es mieloma activo.
- ✅ Estratificación de riesgo (ISS/R-ISS + FISH + LDH).
- ✅ Imagen de alta sensibilidad (WB-LDCT / PET-TC / RM) para enfermedad ósea y extramedular.
- ✅ Plan terapéutico según elegibilidad a trasplante, fragilidad y comorbilidades.
- ✅ Soporte: antirresortivos, profilaxis trombótica e infecciosa, control renal y del dolor.
Técnica
- 🔧 Suero: SPEP + inmunofijación; cuantificación de Ig.
- 🔧 Orina 24 h: UPEP + inmunofijación si procede.
- 🔧 Cadenas ligeras libres séricas: ratio e involucrada (especialmente en mieloma de cadenas ligeras/oligosecretor).
- 🔧 Médula ósea: aspirado + biopsia; citometría; FISH de alto riesgo.
- 🔧 Imagen: WB-LDCT o PET-TC o RM cuerpo entero según disponibilidad/escenario.
Riesgos
- ⚠️ Confundir MGUS/SMM con mieloma activo o viceversa (no aplicar SLiM-CRAB con rigor).
- ⚠️ Infravalorar enfermedad ósea usando sólo serie ósea cuando hay técnicas más sensibles.
- ⚠️ No pedir FISH/LDH y perder estratificación de alto riesgo.
- ⚠️ Iniciar bisfosfonatos sin evaluación dental o sin monitorización renal/electrolitos.
- ⚠️ No pautar profilaxis trombótica con IMiDs cuando está indicada.
- ⚠️ Retrasar tratamiento en insuficiencia renal por cadenas ligeras o en compresión medular.
Resultados
- ✅ Mejoras sustanciales en supervivencia en la era moderna; en trasplante-elegibles suele superar 10 años en estudios del mundo real.
- ✅ La supervivencia poblacional a 5 años ronda el 60% en series recientes.
- ✅ Los antirresortivos reducen eventos esqueléticos y dolor; vigilar ONM e hipocalcemia.
13) Bibliografía
📘 Guías y criterios
- 📄 Rajkumar SV, et al. International Myeloma Working Group (IMWG) criteria (SLiM-CRAB). The International Myeloma Foundation (recurso clínico).
- 📄 Dimopoulos MA, Terpos E, Boccadoro M, et al. EHA–EMN Evidence-Based Guidelines for diagnosis, treatment and follow-up of multiple myeloma. Nat Rev Clin Oncol. 2025;22:680–700. doi:10.1038/s41571-025-01041-x
- 📄 Palumbo A, et al. Revised International Staging System (R-ISS). J Clin Oncol. 2015. (IMWG report)
🩻 Imagen y hueso
- 📄 Hillengass J, et al. IMWG consensus recommendations on imaging in monoclonal plasma cell disorders. Lancet Oncol. 2019.
- 📄 Terpos E, et al. Treatment of myeloma-related bone disease (IMWG Bone Working Group). 2021 (consenso; PDF).
📑 Revisiones útiles
- 📄 Rajkumar SV. Multiple myeloma: 2024 update on diagnosis, risk-stratification, and management. Am J Hematol. 2024.
- 📄 Zanwar S, et al. Current risk stratification and staging of multiple myeloma. Leukemia. 2025.
- 📄 Besliu C, et al. The evolving landscape in multiple myeloma. (PMCID). 2025.