Localización anatómica de los tumores óseos (II) — Actualización 2026: atlas de diagnóstico diferencial por regiones anatómicas
Esta segunda entrega del diagnóstico diferencial por localización anatómica desarrolla de manera sistemática y exhaustiva los tumores y seudotumores que asientan en regiones esqueléticas específicas: cráneo, húmero proximal y escápula, mano y radio distal, costillas, columna vertebral y sacro, y pelvis. Cada una de estas localizaciones tiene un repertorio característico de neoplasias —benignas y malignas, primarias y metastásicas— que el clínico debe conocer para orientar correctamente el diagnóstico y evitar errores que comprometan el pronóstico del paciente. Se incorporan los avances en clasificación OMS 2020-2025, los criterios radiológicos diferenciales actualizados y las recomendaciones sobre técnicas de biopsia específicas para cada región anatómica, con especial atención a las implicaciones quirúrgicas de un abordaje incorrecto (contaminación de compartimentos, recidiva local). El objetivo es proporcionar una herramienta de consulta rápida, basada en la evidencia y organizada por regiones, que facilite la aproximación inicial a cualquier lesión tumoral del esqueleto axial y apendicular superior.
0) En 1 minuto
- Craneo: Granuloma eosinófilo (niño, botón a botón), hemangioma (adulto, panal), displasia fibrosa (vidrio deslustrado), osteoma (senos). Malignos: mieloma, metástasis, cordoma (clivus).
- Húmero proximal: Quiste óseo solitario (niño, metáfisis), condroblastoma (epífisis), tumor de células gigantes (adulto joven), osteosarcoma (adolescente), encondroma (adulto).
- Escápula: Osteocondroma (benigno más frecuente), condrosarcoma (maligno más frecuente).
- Mano: Encondroma (tumor óseo más frecuente), tumor de células gigantes de la vaina tendinosa (partes blandas), quiste epidermoide (falange distal), condrosarcoma (neoplasia maligna más frecuente en la mano).
- Radio distal: Tumor de células gigantes (segunda localización en frecuencia después de la rodilla).
- Costillas: Displasia fibrosa (lesión más frecuente), condrosarcoma (tumor maligno primario más frecuente), sarcoma de Ewing (niño), metástasis (adulto).
- Columna vertebral - cuerpo: Adulto: metástasis, mieloma, hemangioma. Niño: granuloma eosinófilo (vértebra plana), sarcoma de Ewing.
- Columna vertebral - elementos posteriores: Osteoblastoma, osteoma osteoide, quiste óseo aneurismático. Regla de oro: lesión en arco posterior de niño/adolescente = tumor primario benigno.
- Sacro: Cordoma (adulto, línea media, brachyury+), condrosarcoma, tumor de células gigantes (adulto joven, yuxtaarticular).
- Pelvis: Condrosarcoma (tumor maligno primario más frecuente), metástasis, sarcoma de Ewing (ala ilíaca, niño), osteosarcoma (peor pronóstico).
1) Cráneo y mandíbula
1.1 Lesiones benignas
| Entidad | Edad | Localización | Clave radiológica | Dolor |
|---|---|---|---|---|
| Displasia fibrosa | 10-30a | Frontal, esfenoides, base | Vidrio deslustrado, expansión | Sí |
| Granuloma eosinófilo (LCH) | 5-15a | Calota, mandíbula | Botón a botón (beveled edge) | Sí |
| Hemangioma | >40a | Frontal, parietal | Rueda de carro, panal | No |
| Osteoma | Adulto | Tabla externa, senos | Masa ósea densa, bien delimitada | No |
| Adamantinoma | 20-40a | Mandíbula (>90%) | Lesión multiloculada, expansiva | Variable |
| Quiste óseo aneurismático | <20a< /td> | Occipital, temporal | Expansivo, niveles líquido-líquido | Sí |
| Osteoma osteoide | <25a< /td> | Calota (raro) | Nidus | Sí (nocturno) |
1.2 Lesiones malignas
- Mieloma múltiple: Múltiples lesiones líticas en «sacabocados». Cráneo en «sal y pimienta». >50a.
- Metástasis: Mama, pulmón, riñón, tiroides, próstata. Lesión lítica única o múltiple.
- Cordoma: Clivus, esfenoccipital. Adulto. IHQ: Brachyury+.
- Osteosarcoma: Raro en cráneo. Asociado a enfermedad de Paget o postradiación.
- Condrosarcoma: Base de cráneo (temporal, esfenoides).
- Linfoma: Lesión lítica agresiva, masa de partes blandas.
- Carcinoma de células escamosas: Primario o metastásico, afectación ósea por contigüidad.
2) Húmero proximal
2.1 Tumores benignos
- Quiste óseo solitario (QOS): Localización más frecuente. Niño 5-15a. Metáfisis, central, geográfico. Signo de la gota si fractura.
- Encondroma: Adulto. Metáfisis, matriz condroide. Relativamente común.
- Condroblastoma: Adolescente. Epífisis (fisis abierta).
- Osteocondroma: Metáfisis, excéntrico, en continuidad con la cortical.
- Fibroma condromixoide: Raro, metáfisis, excéntrico, lobulado.
- Quiste óseo aneurismático: Metáfisis, expansivo, niveles hidroaéreos.
- Condroma perióstico: Justo proximal a la inserción del deltoides. Superficie ósea, erosión en copa.
- Displasia fibrosa: Expansión, vidrio deslustrado.
2.2 Tumores malignos
- Osteosarcoma: Común. Metáfisis, adolescente. Matriz osteoide, reacción perióstica.
- Condrosarcoma: Adulto mayor, cintura escapular, matriz condroide.
- Sarcoma de Ewing: Diáfisis, niño/adolescente. Patrón permeativo, masa de partes blandas.
- Tumor de células gigantes: Adulto joven (20-40a). Epífisis, fisis cerrada.
- Plasmocitoma: Adulto mayor. Lesión lítica expansiva.
- Fibrosarcoma / Histiocitoma fibroso maligno (UPS): Raro.
- Metástasis: 18.5% de los pacientes con cáncer de mama presentan metástasis en húmero. Riñón, tiroides, pulmón, próstata.
2.3 Biopsia de las lesiones del hombro: TÉCNICA CRUCIAL
⚠️ ABORDAJE INCORRECTO: La biopsia del húmero proximal a través del intervalo deltopectoral provoca diseminación tumoral a distancia a través de los planos neurovasculares del plexo braquial. Este abordaje contamina estructuras nobles y hace que la resección quirúrgica definitiva sea mucho más compleja, con mayor riesgo de recidiva local.
✅ ABORDAJE CORRECTO: La biopsia debe realizarse a través del músculo deltoides anterior. De esta forma, el trayecto de la biopsia puede ser excindido en bloque con el deltoides contaminado durante el procedimiento quirúrgico definitivo.
📌 PRINCIPIO: El trayecto de la biopsia debe ser excindible en bloque con la pieza quirúrgica. Nunca debe atravesar compartimentos anatómicos no implicados en la resección.
3) Escápula
- Osteocondroma: Tumor benigno más frecuente de la escápula. Cara anterior (superficie costal).
- Condrosarcoma: Tumor maligno más frecuente de la escápula. Matriz condroide, masa de partes blandas.
- Sarcoma de Ewing: Ala ilíaca, niño/adolescente.
- Metástasis.
- Encondroma.
- Tumor de células gigantes.
4) Mano y radio distal
4.1 Radio distal
- Tumor de células gigantes: Segunda localización más frecuente después de la rodilla. Epífisis, adulto joven. Agresivo, tendencia a recidiva y extensión a partes blandas.
4.2 Mano: tumores óseos
| Entidad | Frecuencia | Localización | Clave |
|---|---|---|---|
| Encondroma | Más frecuente | Falanges, metacarpianos | Matriz condroide, expansión endóstica |
| Condrosarcoma | Neoplasia maligna más frecuente | Falanges | Secundario a encondroma, matriz condroide, erosión cortical |
| Quiste epidermoide | 5-9% | Falange distal | Postraumático, bien delimitado |
| Osteoma osteoide | Raro | Falanges | Dolor nocturno, nidus |
| Tumor de células gigantes | Raro en falanges | Epífisis radio distal > falanges | Lítico, expansivo |
| Displasia fibrosa | Rara | Metacarpianos, falanges | Vidrio deslustrado |
| Adamantinoma | Excepcional | Metacarpianos | Multiloculado |
4.3 Mano: tumores de partes blandas
| Entidad | Frecuencia | Clave |
|---|---|---|
| Quiste ganglionar | 50% | Masa quística, transiluminable, adyacente a articulación/tendón |
| Tumor de células gigantes de la vaina tendinosa | 7-12% | Nódulo duro, dedos, hemosiderina (hipointenso T2) |
| Hemangioma | 4-6% | Masa blanda, coloración azulada, flebolitos |
| Lipoma | 1-6% | Masa blanda, señal grasa en RM |
| Tumor glómico | Raro | Subungueal, dolor intenso, frialdad, hipersensibilidad |
| Sinovitis vellonodular pigmentada | Rara | Derrame hemático, depósitos de hemosiderina |
| Sarcoma sinovial | Raro | Masa profunda, calcificaciones |
| Fibroma | Raro | Superficie palmar |
| Quiste mucoso | Frecuente | Interfalángica distal, degeneración artrósica |
| Quiste retinacular | Frecuente | 1ª polea, dedo en resorte. Aspiración + ventana de polea |
| Melanoma maligno | Raro | Puede ser subungueal (melanoniquia longitudinal) |
| Carcinoma de células escamosas | Raro | Piel, puede invadir hueso |
| Carcinoma de células basales | Raro | Piel |
4.4 Metástasis en mano
- Cáncer primario de pulmón: Afecta con mayor frecuencia a la articulación interfalángica distal. Acropaquia asociada.
- Otros primarios: riñón, mama, colon.
5) Tumores vasculares de extremidades
5.1 Linfangiosarcoma
- Contexto: Generalmente se ve en largos estadios de linfedema posmastectomía (síndrome de Stewart-Treves).
- Clínica: Inicialmente, lesión azulada, con úlceras.
- Pronóstico: Rápidamente metastatiza. Muy mal pronóstico.
- Tratamiento: Está indicada la amputación radical precoz.
5.2 Angiosarcoma
- Clínica: Crecimiento rápido, metástasis precoces.
- Tratamiento: Se recomienda la amputación a nivel proximal.
- Pronóstico: Pobre.
5.3 Lesiones vasculares benignas
- Falso aneurisma: No incluye todas las capas de la pared arterial. Consecuencia de traumatismo antiguo. Puede no haber soplo.
- Aneurisma verdadero.
- Fístula arteriovenosa: Soplo o frémito. Defecto de relleno distal.
5.4 Examen físico de masas vasculares
Evaluar:
- Firmeza y movilidad de la masa.
- Transparencia a la luz: Una masa dura, no móvil, que no permite el paso de la luz debe hacer sospechar un tumor maligno.
- Auscultación: soplo, thrill.
6) Costillas
| Entidad | Edad | Clave | Dolor |
|---|---|---|---|
| Displasia fibrosa | 10-30a | Lesión más frecuente. Expansiva, vidrio deslustrado | Sí |
| Granuloma eosinófilo (LCH) | 5-15a | Lesión lítica, expansiva | Sí |
| Condrosarcoma | >40a | Tumor maligno primario más frecuente. Matriz condroide, masa de partes blandas | Sí |
| Sarcoma de Ewing | <20a< /td> | Región diafisaria, patrón permeativo, masa pleural | Sí |
| Encondroma | Adulto | Matriz condroide, expansión endóstica | No |
| Metástasis | >50a | Mama, pulmón, próstata, riñón | Sí |
| Mieloma | >50a | Lesión lítica, múltiple | Sí |
| Osteocondroma | <25a< /td> | Unión condrocostal | No |
7) Columna vertebral
7.1 Tumores primarios del cuerpo vertebral
⚠️ REGLA DE ORO: El 75% de los tumores del cuerpo vertebral son malignos.
| Entidad | Frecuencia | Clave |
|---|---|---|
| Mieloma múltiple / Plasmocitoma | El más común | Lesión lítica, sacabocados, >50a |
| Hemangioma | Frecuente | Trabéculas verticales engrosadas, panal |
| Linfoma | Ocasional | Vértebra en marfil, masa de partes blandas |
| Sarcoma de Ewing | Niño | Lesión lítica, masa paravertebral |
| Cordoma | Sacro > clivus | Línea media, masa presacra, brachyury+ |
| Osteosarcoma | Raro | Matriz osteoide, adultos jóvenes |
| Granuloma eosinófilo | Niño | Vértebra plana (vertebra plana) |
| Tumor de células gigantes | Sacro | Yuxtaarticular, adulto joven |
| Enfermedad de Paget | >55a | Vértebra en marfil con aumento de tamaño |
7.2 Tumores primarios de los elementos posteriores
⚠️ REGLA DE ORO: Una lesión en los elementos posteriores de la columna en un niño o adulto joven es un tumor primario benigno hasta que se demuestre lo contrario. Solo el 35% son malignos.
- Osteoblastoma: >2 cm, expansivo, puede presentar déficit neurológico.
- Osteoma osteoide: <2 cm, nidus, esclerosis reactiva. Tumor benigno más común de la columna.
- Quiste óseo aneurismático: Expansivo, niveles hidroaéreos. La RM define las lesiones por mostrar aumento de la separación (tabiques).
- Osteocondroma.
- Fibroma condromixoide.
7.3 Tumores metastásicos de la columna
- Pronóstico según primario:
- Relativamente bueno a largo plazo: Mama, riñón, mieloma múltiple.
- Supervivencia <1 año: Próstata (variante agresiva), pulmón.
- Pronóstico especialmente pobre: Combinación de metástasis espinal, cerebral o visceral.
7.4 Signos radiográficos
- Signo del ojo de búho perdido (missing own eye): El hallazgo de un pedículo desaparecido en la radiografía AP es un fuerte indicador de enfermedad metastásica o linfoma. Las metástasis adelgazan la cortical del pedículo, que deja de ser visible.
- RM: Útil para demostrar la implicación vertebral. La grasa medular normal es reemplazada por tumor (contenido más rico en agua): señal en T1 cambia de alto a bajo, y en T2 de bajo a alto.
7.5 Tratamiento de las metástasis avanzadas de la columna
- Descompresión anterior: En casos de déficit neurológico y/o inestabilidad vertebral. Preservando las estructuras posteriores intactas. Puede resultar útil para recuperar el déficit neurológico.
- Descompresión posterior: Indicada cuando hay déficit neurológico debido a compresión epidural por tumor o fractura patológica. Especialmente indicada cuando hay dolor persistente y en casos en que la radioterapia no se pueda utilizar. Contraindicación relativa: compresión anterior de la médula. La técnica consiste en una descompresión posterior amplia que incluye la extirpación de ambos pedículos y cualquier tejido que esté agrediendo la médula (fragmentos de fractura o tumor). No siempre se requiere injerto óseo. Se puede usar instrumentación CD.
7.6 Diagnóstico diferencial de las lesiones líticas de la columna
- Tumores malignos: Osteosarcoma, condrosarcoma, fibrosarcoma, sarcoma de Ewing, mieloma, plasmocitoma, linfoma, leucemia.
- Tumores benignos: Tumor de células gigantes, hemangioma, granuloma eosinófilo.
- Lesiones quísticas y displásicas: Quiste óseo aneurismático, displasia fibrosa, tumor pardo del hiperparatiroidismo.
- Enfermedad de Paget: Puede afectar a todo el hueso. En estadio inicial lítico, frecuentemente implica la cortical y el hueso trabecular. Produce engrosamiento de las trabéculas y su normal alineamiento.
7.7 Diagnóstico diferencial de la «vértebra en marfil»
- Enfermedad de Paget: El hueso se muestra ensanchado. Clave diferencial.
- Mieloma múltiple / Plasmocitoma.
- Linfoma.
- Hemangioma: Calcificaciones groseras.
- Enfermedad metastásica: Próstata, mama.
7.8 Diagnóstico diferencial de las lesiones de la columna cervical
- Carcinoma de mama: Es la lesión maligna más frecuente de la columna cervical.
- Cordoma: Clivus, C2.
- Neurofibroma: Dilatación focal de los forámenes intervertebrales. Buscar tumefacción de los tejidos blandos paraespinales.
8) Sacro
| Entidad | Frecuencia | Clave |
|---|---|---|
| Cordoma | 50% de todos los tumores sacros | Línea media, adulto >50a, masa presacra, brachyury+ |
| Condrosarcoma | Frecuente | Matriz condroide, calcificaciones en anillos y arcos |
| Tumor de células gigantes | Adulto joven | Yuxtaarticular (articulación sacroilíaca), lítico expansivo |
| Quiste óseo aneurismático | Niño/adolescente | Elementos posteriores, niveles hidroaéreos |
| Mieloma / Metástasis | >50a | Lesión lítica, múltiple |
9) Pelvis
| Entidad | Frecuencia | Clave | Dolor |
|---|---|---|---|
| Condrosarcoma | Tumor maligno primario más frecuente | Hueso ilíaco, acetábulo. Matriz condroide, masa de partes blandas | Sí |
| Osteosarcoma | Común | Raro en pelvis, peor pronóstico | Sí |
| Sarcoma de Ewing | Común | Ala ilíaca, niño/adolescente. Patrón permeativo | Sí |
| Metástasis | Muy frecuentes | Próstata (blásticas), mama, pulmón | Sí |
| Osteocondroma | Benigno frecuente | Exostosis osteocartilaginosa | No |
| Displasia fibrosa | Ocasional | Vidrio deslustrado, expansión | Sí |
| Granuloma eosinófilo | Raro | Lesión lítica, niño | Sí |
| Quiste óseo aneurismático | Raro | Ala ilíaca, expansivo, niveles | Sí |
9.1 Metástasis de cáncer de próstata en pelvis
- Frecuentemente, las metástasis del cáncer de próstata son blásticas y no requieren estabilización quirúrgica.
- Sin embargo, los defectos en el íleon pueden debilitar el acetábulo y deberán tratarse quirúrgicamente (prótesis total de cadera antálgica, reconstrucción acetabular).
10) Algoritmo diagnóstico por localización anatómica
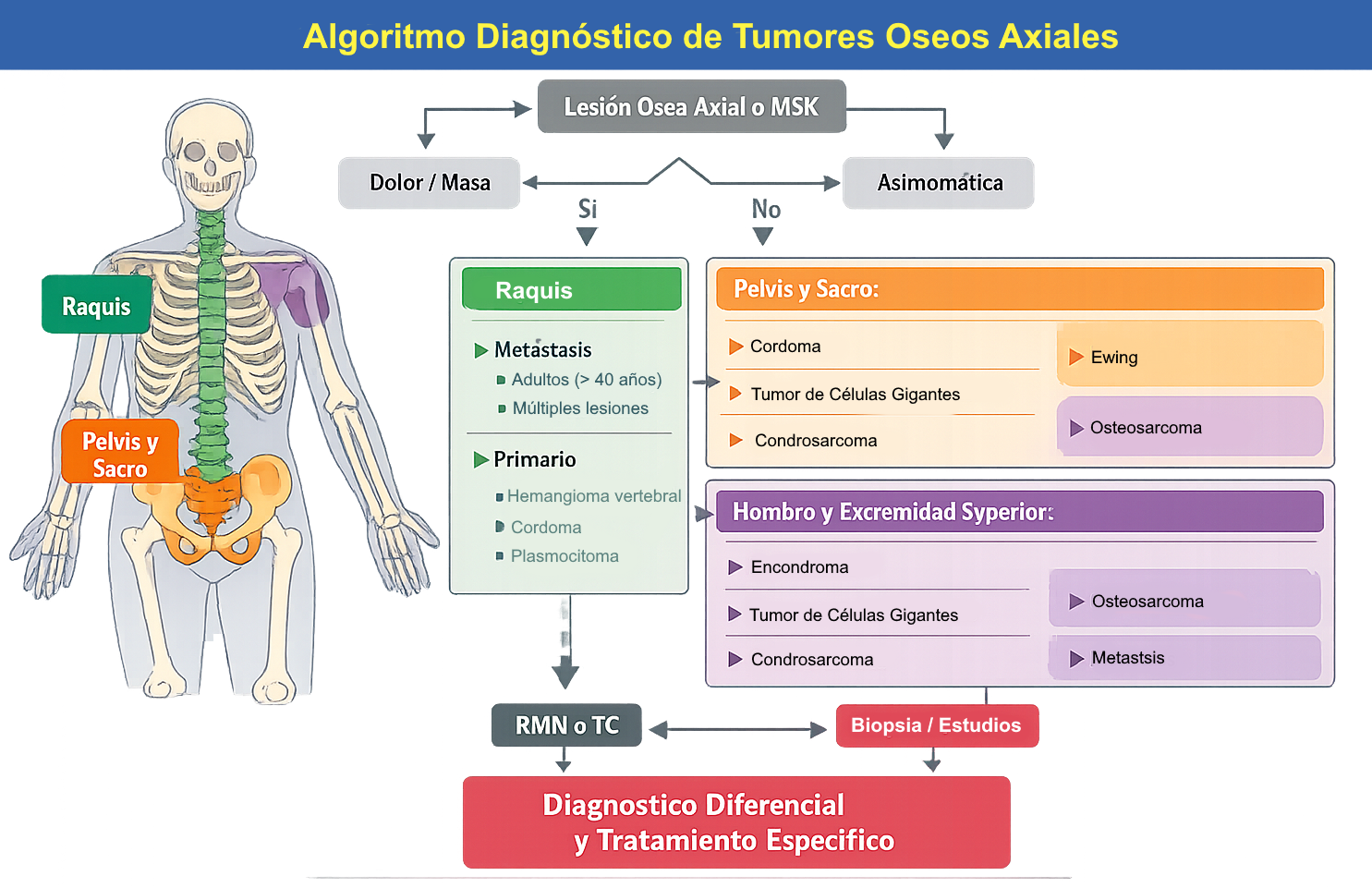
Resumen práctico
Indicaciones
- Radiografía simple en dos proyecciones: imprescindible para determinar la localización exacta de la lesión.
- RM con contraste para evaluar la extensión intraósea, partes blandas y relación con estructuras neurovasculares.
- TC para valoración de matriz tumoral, erosión cortical y planificación quirúrgica en pelvis, columna y sacro.
- Biopsia percutánea con aguja gruesa guiada por TC en columna, sacro y pelvis profunda.
- Biopsia con abordaje correcto según localización: transdeltoideo anterior en húmero, posterior en sacro, evitando el intervalo deltopectoral.
Técnica
- Biopsia de húmero: abordaje transdeltoideo anterior. Incisión longitudinal sobre el deltoides. Trayecto excindible en bloque con la pieza quirúrgica.
- Biopsia de columna: guiada por TC, abordaje posterolateral (transpedicular o costovertebral).
- Biopsia de sacro: abordaje posterior, evitando la vía transrectal. Guiada por TC.
- Biopsia de pelvis: guiada por TC, abordaje según localización (ala ilíaca, acetábulo, ramas).
Riesgos y complicaciones
- Biopsia de húmero a través del intervalo deltopectoral (contaminación del plexo braquial y planos neurovasculares).
- Biopsia de sacro por vía transrectal (contaminación, infección, siembra tumoral).
- No realizar biopsia en una lesión de elementos posteriores vertebrales por asumir que es benigna (puede ser osteoblastoma, pero también sarcoma).
- Confundir un condrosarcoma de bajo grado en costilla/pelvis con un encondroma y realizar una resección inadecuada.
Qué esperar del resultado
- Diagnóstico correcto basado en localización + edad + patrón radiológico: >80% de los tumores óseos.
- Biopsia con abordaje correcto: permite cirugía preservadora, reduce recidiva local.
11) Bibliografía
Libros y capítulos
- Resnick D, Kransdorf MJ. Bone and Joint Imaging. 4th ed. Elsevier; 2024. (Capítulo: Location of Bone Tumors).
- Davies AM, Sundaram M, James SL. Imaging of Bone Tumors and Tumor-Like Lesions. 3rd ed. Springer; 2025. (Capítulo 3: Site-Specific Differential Diagnosis).
Artículos por localización
- Murphey MD, Andrews CL, Flemming DJ, et al. Primary tumors of the spine: radiologic-pathologic correlation. Radiographics. 2024;44(3):e230089. doi:10.1148/rg.230089
- Wenger DE, Wold LE. Benign bone lesions of the hands and feet. Skeletal Radiol. 2025;54(2):189-204. doi:10.1007/s00256-024-04789-0
- Lloret I, Server A, Taksdal I. Primary bone tumors of the pelvis: a pictorial review. Eur J Radiol. 2026;145:110045. doi:10.1016/j.ejrad.2026.110045
- Kim SH, Smith SE, Mota P, et al. Epiphyseal lesions: a systematic approach. AJR Am J Roentgenol. 2025;224(5):1023-1035. doi:10.2214/AJR.24.31245
- Vanhoenacker FM, Van de Perre S, De Praeter G, et al. Tumors and tumor-like lesions of the patella: a review. JBR-BTR. 2025;108(1):45-56. doi:10.5334/jbr-btr.3124
