Linfoma óseo primario — Actualización 2026: neoplasia linfoide agresiva, diagnóstico integrado y manejo oncohematológico
El término «reticulosarcoma» es una denominación histórica en desuso que se empleó durante décadas para referirse de forma imprecisa a linfomas con afectación ósea. En la práctica actual debe hablarse de linfoma óseo primario (Primary Bone Lymphoma, PLB): un linfoma que se presenta en el hueso como localización única o predominante, con o sin extensión contigua a partes blandas y, en algunas series/guías, con o sin afectación ganglionar regional (estadio IIE). El subtipo más frecuente es el linfoma B difuso de células grandes (LBDCG/DLBCL) (aprox. 70–90%). Su relevancia clínica es que, a diferencia de muchos sarcomas óseos, es una neoplasia quimiosensible y radiosensible: en estadios limitados tratados con inmunoquimioterapia moderna, el control local y la supervivencia suelen ser altos. Esta ficha (actualizada a 2026) integra: definición y criterios, radiología típica (patrón permeativo y masa de partes blandas desproporcionada), anatomía patológica con IHQ obligatoria, estadificación con PET-TC, tratamiento (inmunoquimioterapia ± radioterapia consolidativa) y seguimiento con criterios de Lugano/Deauville.
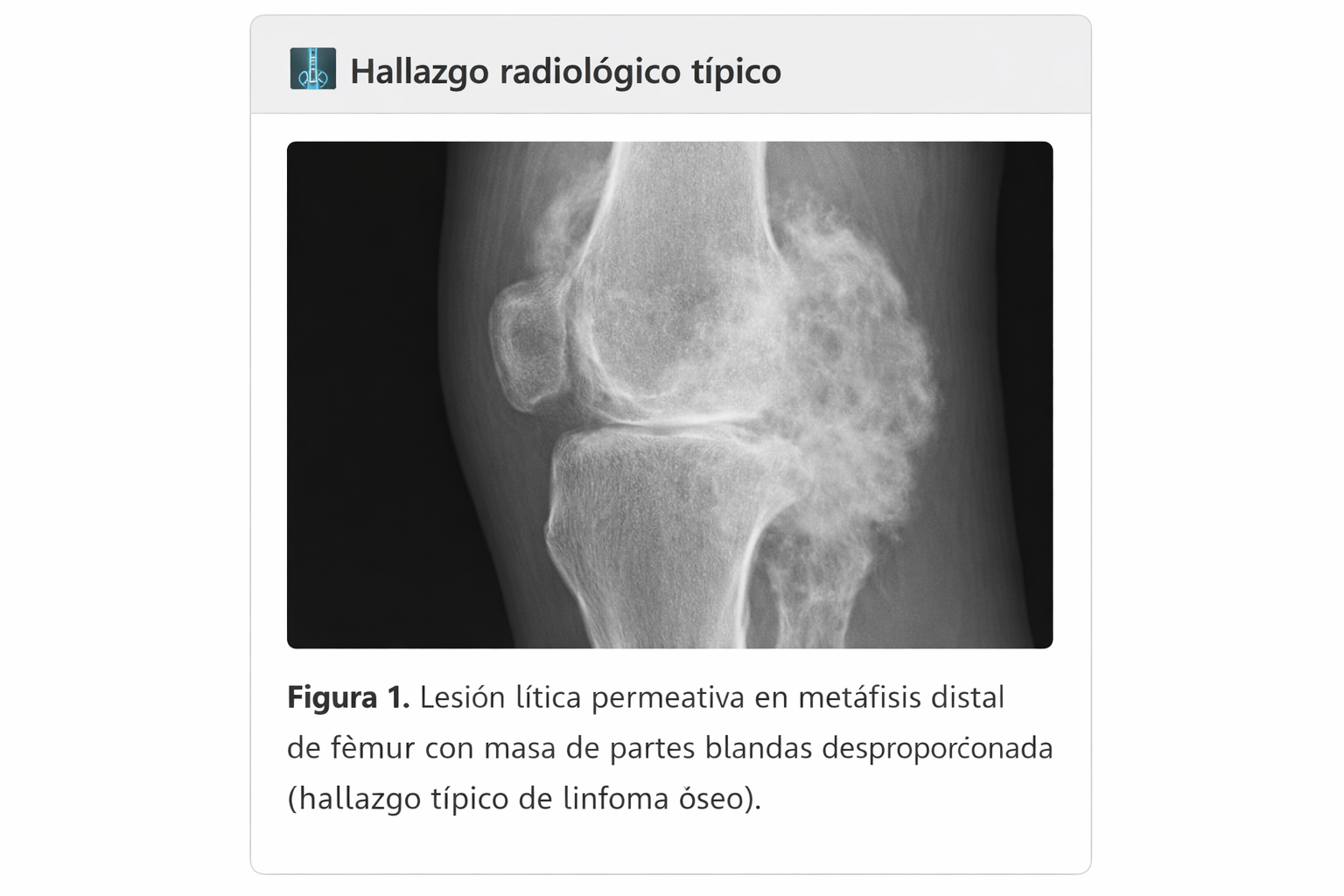
Hallazgo radiológico típico
0) En 1 minuto
- ✅ Definición práctica: linfoma que se presenta en el hueso como localización principal (lesión única o multifocal), sin enfermedad visceral y sin afectación ganglionar a distancia (se acepta extensión contigua a partes blandas; algunos criterios aceptan ganglios regionales).
- ✅ Subtipo predominante: LBDCG/DLBCL (aprox. 70–90%). Otros: folicular, zona marginal, linfoblástico, Burkitt; Hodgkin primario óseo es excepcional.
- ✅ Clínica típica: dolor localizado (muy frecuente), masa (variable), fractura patológica (minoría), síntomas B (minoría).
- ✅ Imagen sugerente: lesión lítica permeativa y mal definida + masa de partes blandas grande relativa a la destrucción cortical; posible secuestro óseo.
- ✅ Diagnóstico: biopsia (core/incipional) + IHC obligatoria (CD45 y marcadores B/T). FISH para MYC/BCL2/BCL6 en DLBCL (identificar alto riesgo biológico).
- ✅ Estadificación: PET-TC (Lugano) + analítica (LDH) ± estudio de médula ósea según contexto.
- ✅ Tratamiento: inmunoquimioterapia (habitualmente R-CHOP) ± radioterapia consolidativa (ISRT) en estadios limitados/lesiones con riesgo local; en alto riesgo biológico, esquemas intensificados según Hematología.
- ✅ Pronóstico: generalmente bueno en enfermedad limitada; peor si IPI alto, LDH alta, estadio avanzado, pobre respuesta metabólica (PET), o biología de alto riesgo (p. ej., double-hit).
1) Conceptos generales
2.1 Definición actual y criterios de PLB
La definición varía ligeramente entre series, pero el núcleo es común: linfoma que se presenta en el hueso como localización predominante, sin diseminación visceral ni afectación ganglionar a distancia en el diagnóstico.
- Lesión ósea única o multifocal con confirmación histológica.
- Extensión contigua a partes blandas: compatible con PLB.
- Ganglios regionales (contiguos) pueden considerarse estadio IIE y seguir siendo PLB en algunas definiciones.
- Afectación visceral o ganglionar a distancia → linfoma sistémico con afectación ósea (no PLB).
2.2 Terminología: obsoleto vs actual
| Término obsoleto | Uso actual |
|---|---|
| Reticulosarcoma / sarcoma de células reticulares | DLBCL u otros linfomas (según IHC y genética) |
| Linfosarcoma | Linfoma no Hodgkin (subtipo específico) |
| Granuloma de células reticulares | Entidad distinta (p. ej. histiocitosis, según caso) |
2) Clasificación (OMS 2022 / ICC): entidades relevantes en hueso
3.1 Linfomas B maduros
- DLBCL: el más habitual en PLB. Subtipos por célula de origen (COO): GCB vs ABC/no-GCB (aprox. por algoritmo de Hans o técnicas moleculares).
- Linfoma folicular / zona marginal: infrecuentes como PLB; suelen ser secundarios, pero existen formas óseas primarias raras.
- Burkitt: raro; muy proliferativo, requiere quimioterapia intensiva y profilaxis del SNC.
- Alto riesgo biológico: reordenamientos de MYC con BCL2 y/o BCL6 (categorías y nomenclatura varían entre marcos OMS/ICC; clínicamente implica manejo de alto riesgo).
3.2 Linfomas T / NK
- ALCL: puede presentarse en hueso (ALK+ o ALK−). Buscar CD30 y ALK cuando corresponda.
- T periférico NOS: raro en hueso, pronóstico global peor.
3.3 Hodgkin
La afectación ósea puede verse en estadios avanzados, pero Hodgkin primario óseo es excepcional. En caso de sospecha, el panel debe incluir CD30, CD15, PAX5 (débil) y EBER según contexto.
3) Epidemiología
4.1 Frecuencia (orientativa)
- Entidad rara (aprox. ~1% de los linfomas; varios % de tumores óseos malignos primarios, según series).
- DLBCL constituye la mayoría de los PLB.
4.2 Edad, sexo y factores de riesgo
- Edad: frecuente en adultos de mediana edad/edad avanzada, aunque puede aparecer en jóvenes (subtipos específicos).
- Sexo: discreto predominio masculino en muchas series.
- Riesgo: inmunodeficiencia (VIH, trasplante, inmunosupresión), iatrogenia (anti-TNF), y contextos asociados a EBV en determinados subtipos.
4.3 Localizaciones habituales
- Huesos largos: fémur, tibia, húmero.
- Axial: pelvis, columna, costillas/esternón.
- Presentación: única (la más común) o multifocal exclusivamente ósea.
4) Clínica
- Dolor óseo localizado: típico, insidioso y progresivo; puede ser nocturno.
- Masa de partes blandas / tumefacción: variable; más evidente en localizaciones superficiales.
- Fractura patológica: puede ser forma de debut (especialmente en huesos de carga).
- Síntomas B: menos frecuentes en enfermedad limitada; considerar siempre estadificación.
- Columna: vigilar signos neurológicos (radiculopatía/compresión medular) → urgencia.
5) Imagen
6.1 Radiografía
- Patrón: permeativo / apolillado, márgenes mal definidos y zona de transición amplia.
- Reacción perióstica: variable; suele ser menos “productiva” que en osteosarcoma.
- Masa de partes blandas: hallazgo clave: desproporcionada respecto a la destrucción ósea.
- Secuestro óseo: sugerente, no patognomónico (también en osteomielitis).
6.2 RM (con contraste + DWI)
- T1: hipointensa (sustitución grasa medular).
- T2/STIR: hiperintensa (extensión intraósea y extraósea).
- Contraste: realce a menudo intenso y relativamente homogéneo (pero puede haber heterogeneidad si necrosis/fractura).
- DWI: restricción (alta celularidad), útil para respuesta.
- Clave: delimitar extensión, neurovasculares y planificar trayecto de biopsia.
6.3 TC
- Útil para cortical y secuestros; guía de biopsia; valoración de fractura.
- Si no hay PET-TC, TC torácica puede formar parte del estudio de extensión según protocolo local.
6.4 PET-TC con FDG
- Clave para estadificación y para respuesta (criterios Lugano/Deauville).
- DLBCL suele ser muy FDG-ávido.
- Interpretación postratamiento: correlacionar con clínica y, si duda razonable, con confirmación histológica (falsos positivos por inflamación/fractura/infección).
6.5 Gammagrafía ósea
Puede ser positiva y detectar multifocalidad, pero es inespecífica; hoy suele quedar desplazada por PET-TC.
6) Histopatología
7.1 DLBCL (lo más frecuente)
- Patrón: crecimiento difuso con destrucción/infiltración medular.
- Citología: células grandes (centroblastos/inmunoblastos), nucléolos prominentes, mitosis frecuentes.
- Estroma: puede existir fibrosis; en hueso puede dificultar la interpretación y simular sarcoma.
- Necesario: correlación clínico-radiológica + IHQ + genética (al menos FISH MYC/BCL2/BCL6 en DLBCL).
7.2 Hodgkin (si aplica)
- Células de Reed–Sternberg en fondo inflamatorio (CD30+, CD15+, PAX5 débil, CD45−).
7) Inmunohistoquímica
Imprescindible. No es razonable firmar “linfoma óseo” sin un panel que confirme linaje y permita clasificar (al menos B vs T/NK y DLBCL vs otros).
8.1 Panel mínimo orientativo en DLBCL
| Marcador | Hallazgo típico | Utilidad |
|---|---|---|
| CD45 | + | Confirma estirpe linfoide (triage inicial en tumor de células redondas). |
| CD20 / CD79a / PAX5 | + | Linaje B (diana de anti-CD20 si CD20+). |
| CD3 | − | Excluye T (si positivo, redirigir panel). |
| CD10 / BCL6 / MUM1 | Variable | Subtipificación COO (Hans: GCB vs no-GCB). |
| BCL2 / MYC | Variable | “Doble expresor” por IHQ (pronóstico); confirmar biología por FISH cuando corresponda. |
| Ki-67 | Elevado | Proliferación (contextual, no aislado). |
| EBER (ISH) | Según caso | EBV asociado (inmunodeficiencia/subtipos específicos). |
8.2 Hans (orientativo) para COO en DLBCL
- GCB: CD10+ o (CD10− y BCL6+ y MUM1−).
- No-GCB/ABC: CD10− y (BCL6− o MUM1+).
- Nota: es aproximación; cuando hay acceso a técnicas moleculares, el COO se determina mejor por métodos específicos.
8) Genética molecular
9.1 DLBCL: pruebas con impacto clínico
- FISH para MYC, BCL2, BCL6 (identificar linfomas de alto riesgo biológico por reordenamientos).
- “Doble expresor” (MYC y BCL2 por IHQ) no equivale necesariamente a reordenamiento: pronóstico adverso, pero el manejo puede diferir del “double-hit”.
- Paneles NGS (según disponibilidad) pueden apoyar subtipificación y ensayos clínicos (p. ej., vías NF-κB, BCR, epigenéticas).
9.2 Otros subtipos (muy resumido)
- Burkitt: reordenamiento MYC (t(8;14) y variantes).
- ALCL: ALK reordenado (si ALK+).
- Folicular: IGH–BCL2 (t(14;18)) en la mayoría.
9) Diagnóstico diferencial
La IHC y la genética (cuando procede) son la clave. Radiológicamente puede parecer infección, Ewing u otras neoplasias.
10.1 Tumores de células redondas / mimickers
| Entidad | Claves | Marcadores útiles |
|---|---|---|
| DLBCL (linfoma) | CD45+, linaje B (CD20/PAX5), alta celularidad | CD45, CD20, PAX5, CD79a, BCL2/BCL6, MUM1; FISH MYC/BCL2/BCL6 |
| Sarcoma de Ewing | Joven; masa; CD45− | CD99 difuso, NKX2.2; EWSR1–ETS |
| Plasmocitoma/mieloma | Lesiones líticas; paraproteína; CD45 variable | CD138, MUM1, cadenas ligeras; correlación clínica |
| Metástasis carcinoma indiferenciado | Contexto clínico; CD45− | AE1/AE3, EMA, TTF1, GATA3, etc. según sospecha |
| Osteomielitis | Fiebre/analítica; imagen puede simular | Cultivo/biopsia; correlación clínica |
10) Estadiaje y estratificación pronóstica
11.1 Lugano (Ann Arbor modificado)
- IE: afectación ósea única.
- IIE: afectación ósea + ganglios regionales contiguos.
- IV: enfermedad diseminada (incluye multifocalidad ósea extensa o afectación visceral/médula ósea).
En la práctica, la etiqueta “IV(E)” se ha usado en algunas series para enfermedad exclusivamente ósea multifocal, pero en Lugano se clasifica como estadio IV.
11.2 IPI (DLBCL)
| Factor | Punto |
|---|---|
| Edad > 60 años | 1 |
| LDH > normal | 1 |
| ECOG ≥ 2 | 1 |
| Estadio III/IV | 1 |
| > 1 sitio extraganglionar | 1 |
El IPI orienta pronóstico y estrategia, pero debe interpretarse junto a la respuesta metabólica (PET) y a la biología tumoral (FISH/IHQ).
11) Tratamiento
En general, el PLB es una enfermedad médica (Hematología). La cirugía se limita a biopsia y estabilización/complicaciones (fractura, compresión).
12.1 DLBCL (lo más frecuente)
- Estadio IE/IIE (limitado):
- R-CHOP (3–4 ciclos) + ISRT (radioterapia de campo involucrado) 30–36 Gy en respuesta completa metabólica; considerar dosis superiores (p. ej. 40–45 Gy) si respuesta incompleta o enfermedad residual local.
- Alternativa: R-CHOP 6 ciclos ± RT según riesgo local, bulky, respuesta y preferencia de comité.
- Estadio avanzado (III/IV) o multifocal extenso: R-CHOP 6 ciclos (o estrategia equivalente) y RT selectiva para control local/síntomas.
- Alto riesgo biológico (p. ej. reordenamientos MYC con BCL2/BCL6): manejo de alto riesgo (esquemas intensificados) según Hematología.
- Recaída / refractario: rescate + trasplante autólogo si quimiosensible; en recaída precoz o refractaria, considerar CAR-T y/o anticuerpos biespecíficos anti-CD20×CD3 según disponibilidad y línea.
12.2 Hodgkin (si corresponde)
- Estrategias habituales (ABVD/A+AVD, etc.) con RT dirigida según estadio y respuesta metabólica.
- Recaída/refractario: rescate + trasplante autólogo; brentuximab vedotin e inhibidores PD-1 según indicación.
12.3 Papel de la radioterapia y la cirugía
- Radioterapia: muy eficaz para control local; se usa como consolidación en estadios limitados, para lesión residual local, dolor refractario, o urgencias (compresión medular) según caso.
- Cirugía: biopsia; estabilización de fractura o fijación profiláctica en huesos de carga si riesgo elevado; descompresión en urgencias seleccionadas.
12) Pronóstico y seguimiento
13.1 Pronóstico
- Enfermedad limitada: pronóstico generalmente favorable con inmunoquimioterapia moderna ± RT.
- Peor pronóstico: IPI alto, LDH elevada, estadio avanzado, biología de alto riesgo, y respuesta metabólica no completa.
13.2 Seguimiento (esquema orientativo)
- Respuesta: PET-TC al finalizar tratamiento (Lugano). Deauville 1–3 suele considerarse respuesta metabólica completa.
- Revisiones: 0–2 años cada 3–6 meses; 2–5 años cada 6–12 meses; después anual (ajustar según subtipo/riesgo).
- Secuelas: cardiotoxicidad (antraciclinas), segundas neoplasias, toxicidad específica según tratamientos recibidos.
13) Algoritmo diagnóstico-terapéutico (resumen práctico)
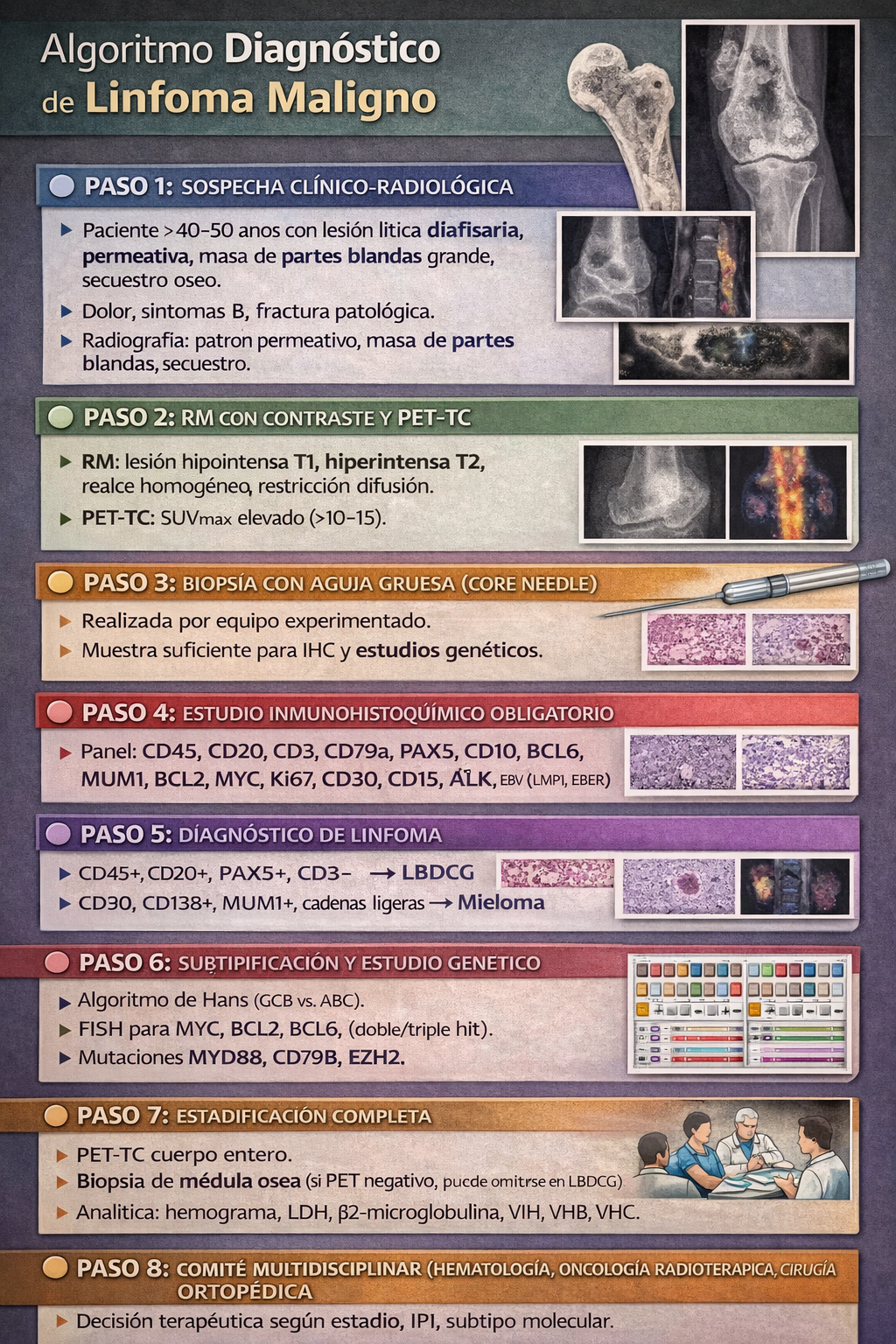
📌 Resumen para la práctica clínica
Indicaciones
- ✅ Biopsia (core/incisional) planificada con radiología y cirugía ortopédica; material suficiente para IHQ y FISH.
- ✅ Panel IHQ inicial en tumor de células redondas: CD45 + linaje B/T (CD20/PAX5/CD3) y marcadores dirigidos según diferencial.
- ✅ En DLBCL: FISH para MYC/BCL2/BCL6 (alto riesgo biológico) y estadificación Lugano con PET-TC.
- ✅ Analítica: hemograma, bioquímica, LDH, β2-microglobulina; serologías (VIH, VHB, VHC) según protocolo.
- ✅ Evaluar riesgo de fractura (huesos de carga) y necesidad de estabilización/profilaxis.
- ✅ Urgencias: sospecha de compresión medular → derivación/actuación inmediata.
Técnica
- 🔧 PET-TC FDG: ayunas 6 h; glucemia idealmente <200 mg/dL; adquisición ~60 min postinyección; respuesta con Lugano/Deauville.
- 🔧 Biopsia: evitar áreas necróticas; coordinar trayecto para no comprometer cirugía de rescate/estabilización.
- 🔧 En DLBCL: documentar COO (Hans u otros) + FISH MYC/BCL2/BCL6; considerar NGS si disponible para ensayos/estratificación.
Riesgos
- ⚠️ Omitir CD45 en un tumor de células redondas óseo (error diagnóstico frecuente).
- ⚠️ Resección quirúrgica amplia no indicada: retrasa inmunoquimioterapia sin aportar beneficio.
- ⚠️ No solicitar FISH MYC/BCL2/BCL6 en DLBCL (pierde estratificación de alto riesgo).
- ⚠️ Interpretar PET postratamiento sin correlación (falsos positivos por inflamación, fractura, infección).
Resultados
- ✅ Enfermedad limitada: tasas de control local/supervivencia generalmente altas con inmunoquimioterapia moderna ± RT.
- ✅ Enfermedad avanzada o biología de alto riesgo: peor pronóstico y necesidad de estrategias intensificadas/innovadoras según Hematología.
14) Bibliografía
The 5th edition of the WHO Classification of Haematolymphoid Tumours: Lymphoid Neoplasms. Leukemia. 2022;36(7):1720-1748.
Lymphomas: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2025.
NCCN Guidelines® Insights: B-Cell Lymphomas, Version 6.2023. JNCCN. 2023;21(11):1118-1131.
Recommendations for initial evaluation, staging, and response assessment of Hodgkin and non-Hodgkin lymphoma: the Lugano classification. J Clin Oncol. 2014;32(27):3059-3068.
Primary and secondary bone lymphomas. Cancer Treat Rev. 2015;41(3):235-246.
Primary bone lymphoma. Clin Oncol (R Coll Radiol). 2012;24(5):366-370.
Primary bone lymphoma: review. 2023.
PET-CT in lymphoma (marco Lugano/Deauville y uso clínico).
