Laboratorio en tumores del sistema musculoesquelético — Actualización 2026: biomarcadores séricos, urinarios y genéticos en el diagnóstico, pronóstico y monitorización
El laboratorio clínico desempeña un papel creciente en el manejo de los tumores del sistema musculoesquelético. Aunque durante décadas se consideró que las pruebas serológicas tenían un valor limitado —restringido básicamente a la fosfatasa alcalina en osteosarcoma y la LDH en sarcoma de Ewing—, la incorporación de la inmunohistoquímica, la citogenética y la biología molecular ha transformado por completo este escenario. Hoy, el diagnóstico de numerosas entidades se define por alteraciones genéticas recurrentes detectables en sangre periférica (biopsia líquida) o en tejido tumoral mediante técnicas de secuenciación masiva. La Actualización 2026 integra los marcadores séricos clásicos con los nuevos biomarcadores moleculares, establece algoritmos de uso racional según el contexto clínico y define el papel de la biopsia líquida en la detección precoz de recidivas y monitorización de la respuesta terapéutica. Esta ficha desarrolla de manera extensa y fundamentada cada uno de estos aspectos, con especial atención a la rentabilidad diagnóstica, la especificidad de cada marcador y su correcta interpretación en relación con la edad, el sexo y las condiciones basales del paciente.

En 1 minuto
Marcador de actividad osteoblástica. Elevada en osteosarcoma (>50%). Útil para monitorizar respuesta y detectar recidivas.
Factor pronóstico independiente en sarcoma de Ewing. Elevada en sarcomas de alto grado, linfomas, histiocitosis.
Inespecíficos. Elevados en sarcoma de Ewing, linfoma, histiocitosis, metástasis e infección.
Imprescindible en >40 años con lesión lítica. Pico monoclonal confirma mieloma.
PSA, calcitonina, catecolaminas, etc., según sospecha de metástasis de carcinoma.
Monitorización de respuesta, detección precoz de recidiva, identificación de resistencias.
Conceptos generales
1.1 El laboratorio en la tríada diagnóstica
El diagnóstico de los tumores musculoesqueléticos se asienta sobre tres pilares: clínica, radiología y anatomía patológica. El laboratorio clínico no constituye un pilar independiente, pero aporta información complementaria esencial en cuatro escenarios:
- Diagnóstico diferencial: Distinguir entre procesos neoplásicos y no neoplásicos (infección, enfermedades metabólicas).
- Sospecha de entidades específicas: Mieloma, metástasis de carcinomas, sarcoma de Ewing, osteosarcoma.
- Pronóstico: Estratificación del riesgo (LDH en sarcoma de Ewing, FA en osteosarcoma).
- Monitorización: Respuesta al tratamiento y detección precoz de recidivas.
1.2 Clasificación de los marcadores
- Marcadores séricos inespecíficos: VSG, PCR, LDH, FA, calcio, fósforo.
- Marcadores séricos específicos: PSA, calcitonina, tiroglobulina, CA 15.3, CA 125, CEA, alfafetoproteína, β-hCG.
- Marcadores urinarios: Catecolaminas (VMA, HVA), proteinuria de Bence Jones, hidroxiprolina.
- Marcadores de displasia/transformación: Osteocalcina, PINP, ICTP (marcadores de recambio óseo).
- Biomarcadores genéticos en sangre (biopsia líquida): ADN tumoral circulante (ctDNA) con detección de fusiones, mutaciones, amplificaciones.
Fosfatasa alcalina (FA)
2.1 Isoformas y valores de referencia
- Isoenzima ósea (BAP): Específica de osteoblastos. Constituye aproximadamente el 50% de la FA total en adultos y hasta el 80-90% en niños y adolescentes.
- Valores normales: Adultos: 40-130 UI/L (varía según laboratorio). Niños y adolescentes: hasta 350-500 UI/L durante el pico de crecimiento (10-15 años). Mujeres gestantes: elevación fisiológica (isoenzima placentaria).
- Fraccionamiento: No es necesario de rutina. Útil cuando se sospecha elevación de origen hepático (GGT, transaminasas) o en el seguimiento de osteosarcoma con FA total normal pero sospecha clínica.
2.2 FA en tumores óseos
- Osteosarcoma convencional: Elevada en el 50-70% de los casos al diagnóstico. Se correlaciona con la masa tumoral y la actividad osteoblástica. Los osteosarcomas telangiectásicos y de células pequeñas pueden presentar FA normal.
- Osteosarcoma parosteal: FA normal o discretamente elevada (bajo grado, escasa actividad osteoblástica).
- Osteosarcoma secundario (Paget, postradiación): FA muy elevada, a menudo >500 UI/L.
- Osteosarcoma multicéntrico: FA extremadamente elevada (>1000 UI/L) en la mayoría de los casos.
- Metástasis osteoblásticas: Especialmente carcinoma de próstata. La FA es un marcador de carga tumoral y respuesta al tratamiento.
- Sarcoma de Ewing, condrosarcoma, tumor de células gigantes: FA normal, salvo fractura patológica asociada.
2.3 FA como marcador pronóstico y de monitorización
- Pronóstico: La FA elevada al diagnóstico en osteosarcoma se asocia a peor supervivencia libre de eventos (SLE) en la mayoría de las series, aunque no es un factor independiente en análisis multivariante tras ajustar por tamaño tumoral y necrosis a quimioterapia.
- Monitorización:
- Respuesta a quimioterapia neoadyuvante: El descenso de FA tras 2-3 ciclos se correlaciona con necrosis tumoral >90%.
- Detección de recidiva: Un aumento progresivo de FA tras la normalización postratamiento es altamente sugestivo de recidiva local o metastásica (especificidad >90%, sensibilidad 40-60%).
- Limitaciones: Fracturas patológicas, infección, hepatopatía, embarazo y crecimiento fisiológico elevan la FA. Siempre correlacionar con la clínica y la radiología.
Lactato deshidrogenasa (LDH)
- Elevación: Marcador inespecífico de recambio celular y necrosis tisular. Elevada en sarcomas de alto grado, linfomas, leucemias, histiocitosis y, en general, en tumores con alta proliferación y extensas áreas de necrosis.
- Sarcoma de Ewing: La LDH es el marcador sérico de mayor utilidad.
- Diagnóstico diferencial: LDH muy elevada (>500 UI/L) en sarcoma de Ewing; LDH normal en osteomielitis.
- Pronóstico: La LDH elevada al diagnóstico es factor pronóstico adverso independiente (riesgo relativo de recaída 2.5-3.0). Se incorpora en los sistemas de estratificación de riesgo (grupo de alto riesgo).
- Monitorización: La normalización de LDH tras quimioterapia de inducción es un marcador de buena respuesta. Su re-elevación sugiere recidiva.
- Osteosarcoma: Elevada en el 20-30% de los casos. Menor utilidad que la FA. Se ha descrito correlación con mal pronóstico en algunas series.
- Linfoma óseo: La LDH forma parte del índice pronóstico internacional (IPI). Elevada en más del 50% de los casos.
- Condrosarcoma desdiferenciado: Puede elevarse, reflejando el componente de alto grado.
VSG, PCR, hemograma y reactantes de fase aguda
4.1 Velocidad de sedimentación globular (VSG)
- Inespecífica: Elevada en infección, inflamación, necrosis tumoral, anemia, embarazo, postoperatorio.
- Tumores con VSG frecuentemente elevada: Sarcoma de Ewing (>80%), linfoma, histiocitosis, mieloma múltiple, metástasis.
- Tumores con VSG normal: Osteosarcoma (40-50% normal), condrosarcoma, tumor de células gigantes, tumores benignos.
- Mieloma múltiple: VSG >100 mm/h en el 60-70% de los casos. Característico: descenso precipitado en el primer cuarto de hora por la formación de rouleaux (aglutinación eritrocitaria).
- Valor pronóstico: VSG elevada al diagnóstico en sarcoma de Ewing se asocia a peor supervivencia (refleja síndrome paraneoplásico y mayor carga tumoral).
4.2 Proteína C reactiva (PCR)
- Similar a VSG: Más específica de infección bacteriana aguda. En tumores, se eleva en sarcoma de Ewing, linfoma e histiocitosis.
- Útil en el diagnóstico diferencial: PCR normal o discretamente elevada en osteosarcoma; muy elevada en osteomielitis.
4.3 Hemograma
- Anemia: Normocítica, normocrómica, de trastorno crónico. Frecuente en sarcomas de alto grado, metástasis, mieloma. La anemia microcítica puede orientar a metástasis de carcinoma gastrointestinal.
- Leucocitosis: Osteomielitis, sarcoma de Ewing (leucocitosis neutrofílica en 20-30% de los casos), linfoma.
- Trombocitosis: Reactiva, en sarcomas avanzados.
- Citopenias: Infiltración medular (mieloma, leucemia, linfoma, metástasis de neuroblastoma).
Proteinograma, inmunofijación y marcadores de mieloma
Indicación prioritaria: Todo paciente mayor de 40 años con una lesión ósea lítica, osteopenia generalizada o fractura patológica debe ser estudiado mediante proteinograma sérico y electroforesis/inmunofijación en orina para descartar mieloma múltiple o plasmocitoma.
5.1 Mieloma múltiple
- Pico monoclonal (componente M): Detectable en suero en el 80-85% de los pacientes. IgG (50-60%), IgA (20-25%), cadenas ligeras libres (15-20%), IgD, IgE (raras).
- Inmunofijación: Más sensible que la electroforesis convencional. Obligatoria ante sospecha clínica con electroforesis negativa.
- Cadenas ligeras libres séricas (FLC): Indicadas en mieloma de cadenas ligeras, mieloma oligosecretor, amiloidosis. Relación kappa/lambda alterada (<0.26 o >1.65).
- Proteinuria de Bence Jones: Cadenas ligeras monoclonales en orina. Detectable en orina de 24 horas mediante electroforesis o inmunofijación.
- Hiperproteinemia: Por aumento de globulinas. Inversión del cociente albúmina/globulina (A/G <1).
- Hipogammaglobulinemia: En mieloma IgA y de cadenas ligeras, puede haber inmunoparesia (descenso de inmunoglobulinas no monoclonales).
5.2 Plasmocitoma solitario
- Componente M: Ausente en suero/orina en el 30-50% de los casos. Si está presente, suele ser de bajo título y desaparece tras la resección/radioterapia.
- Persistencia de componente M tras tratamiento: Sugiere enfermedad sistémica oculta (evolución a mieloma).
Marcadores específicos de metástasis y tumores primarios
| Tumor primario | Marcador sérico/urinario | Comentario |
|---|---|---|
| Carcinoma de próstata | PSA (antígeno prostático específico) | Sensibilidad >95% para metástasis osteoblásticas. También se eleva en hiperplasia benigna y prostatitis. Fosfatasa ácida prostática (PAP): obsoleta. |
| Carcinoma de mama | CA 15.3, CEA | CA 15.3 elevado en 50-60% de las metástasis óseas. Baja sensibilidad en enfermedad localizada. Útil para monitorización. |
| Carcinoma de pulmón | CEA, CYFRA 21-1, NSE, ProGRP | NSE y ProGRP en carcinoma microcítico. CEA y CYFRA en no microcítico. Baja especificidad. |
| Carcinoma de tiroides | Tiroglobulina (papilar/ folicular), calcitonina (medular) | Tiroglobulina: solo útil tras tiroidectomía total. Calcitonina: muy elevada en enfermedad metastásica. |
| Carcinoma renal | Ninguno de rutina | No hay marcador sérico específico. Puede haber eritrocitosis (eritropoyetina). |
| Carcinoma hepatocelular | Alfafetoproteína (AFP) | Elevada en 70-80% de los casos. Metástasis óseas poco frecuentes. |
| Tumor germinal | AFP, β-hCG | Metástasis óseas en 5-10% de los tumores germinales no seminomatosos. |
| Neuroblastoma | Catecolaminas urinarias (VMA, HVA) | Metástasis óseas en niños. VMA/HVA elevados en >90% de los casos. Relación VMA/HVA: pronóstica. |
| Feocromocitoma | Metanefrinas plasmáticas/urinarias | Metástasis óseas en 10-15%. Asociado a MEN 2A/2B, VHL, NF1. |
Biopsia líquida y marcadores genéticos circulantes
Actualización 2026: La biopsia líquida ha pasado de ser una herramienta experimental a una realidad clínica en el manejo de los sarcomas óseos y de partes blandas, aunque su implementación aún es heterogénea y limitada a centros de referencia.
7.1 ADN tumoral circulante (ctDNA)
- Fundamento: Las células tumorales liberan fragmentos de ADN a la sangre periférica mediante apoptosis, necrosis o secreción activa. Este ADN tumoral circulante (ctDNA) contiene las alteraciones genéticas específicas de la neoplasia (mutaciones, fusiones, amplificaciones).
- Técnicas: PCR digital (ddPCR) para detección de mutaciones conocidas; secuenciación masiva (NGS) para paneles de genes o abordajes de secuenciación completa del exoma/genoma.
- Indicaciones actuales (2026):
- Monitorización de respuesta: Descenso de ctDNA tras quimioterapia neoadyuvante se correlaciona con necrosis tumoral en osteosarcoma y sarcoma de Ewing.
- Detección precoz de recidiva: La reaparición o aumento de ctDNA precede en 2-6 meses a la recidiva radiológica en osteosarcoma y sarcoma de Ewing (sensibilidad 80-90%, especificidad >95%).
- Identificación de resistencias: Detección de mutaciones emergentes en genes diana (p. ej., mutaciones en el dominio cinasa de KIT en GIST tras tratamiento con imatinib).
- Caracterización genómica en enfermedad metastásica: Cuando no es posible obtener tejido fresco.
- Limitaciones: Baja sensibilidad en tumores de bajo grado o con escasa liberación de ADN; falsos negativos en ausencia de alteraciones genéticas conocidas; coste elevado; necesidad de estandarización.
7.2 Marcadores genéticos específicos detectables en ctDNA
- Osteosarcoma: Detección de reordenamientos estructurales complejos (cromotripsis) y pérdida de heterocigosidad en TP53, RB1, CDKN2A. Sin alteración genética universal.
- Sarcoma de Ewing: Fusión EWSR1-FLI1 (90%) o variantes. Detectable en ctDNA con alta sensibilidad y especificidad.
- Condrosarcoma: Mutaciones IDH1/IDH2 en el 50-60% de los condrosarcomas centrales.
- Tumor de células gigantes: Mutación H3F3A G34W.
- Condroblastoma: Mutación H3F3B K36M.
- Tumor fibroso solitario: Fusión NAB2-STAT6 (difícil detección en ctDNA por ser intra génica).
- Liposarcoma mixoide: Fusión FUS-DDIT3.
- Sarcoma sinovial: Fusión SS18-SSX.
Marcadores de remodelado óseo
- Hidroxiprolina urinaria: Marcador clásico de resorción ósea. Obsoleto, reemplazado por marcadores más específicos (NTX, CTX, PINP, osteocalcina).
- Péptido aminoterminal del procolágeno tipo I (PINP): Marcador de formación ósea. Elevado en osteosarcoma y metástasis osteoblásticas. Útil en monitorización de tratamiento con denosumab.
- Telopéptido carboxiterminal del colágeno tipo I (ICTP/CTX): Marcador de resorción ósea. Elevado en mieloma, metástasis líticas, tumor de células gigantes.
- Osteocalcina (BGP): Proteína no colágena sintetizada por osteoblastos. Marcador de formación ósea. Utilidad limitada en clínica diaria.
- Fosfatasa ácida tartrato-resistente (TRAP): Marcador de actividad osteoclástica. Elevada en tumor de células gigantes, metástasis líticas.
Calcio, fósforo y metabolismo mineral
- Hipercalcemia: Complicación metabólica más frecuente en tumores óseos avanzados. Mecanismos:
- Osteólisis local: Metástasis líticas, mieloma, tumor de células gigantes.
- Hipercalcemia humoral: Secreción de PTHrp (carcinoma escamoso, carcinoma renal, mama, ovario).
- 1,25-dihidroxivitamina D: Linfoma (raramente).
- Hipocalcemia: Menos frecuente. Puede aparecer tras tratamiento con denosumab o bifosfonatos (hipocalcemia iatrogénica), en osteosarcoma con extensa mineralización tumoral (síndrome de captación de calcio).
- Fósforo: Fósforo normal o elevado en insuficiencia renal. Hipofosfatemia en osteomalacia oncogénica (tumor mesenquimal secretor de FGF-23).
- PTH y PTHrp: Indicadas en hipercalcemia para diagnóstico diferencial. PTH suprimida + PTHrp elevada = hipercalcemia humoral.
- Vitamina D: Descartar déficit como causa de elevación de FA (osteomalacia).
Algoritmo de solicitud racional de laboratorio
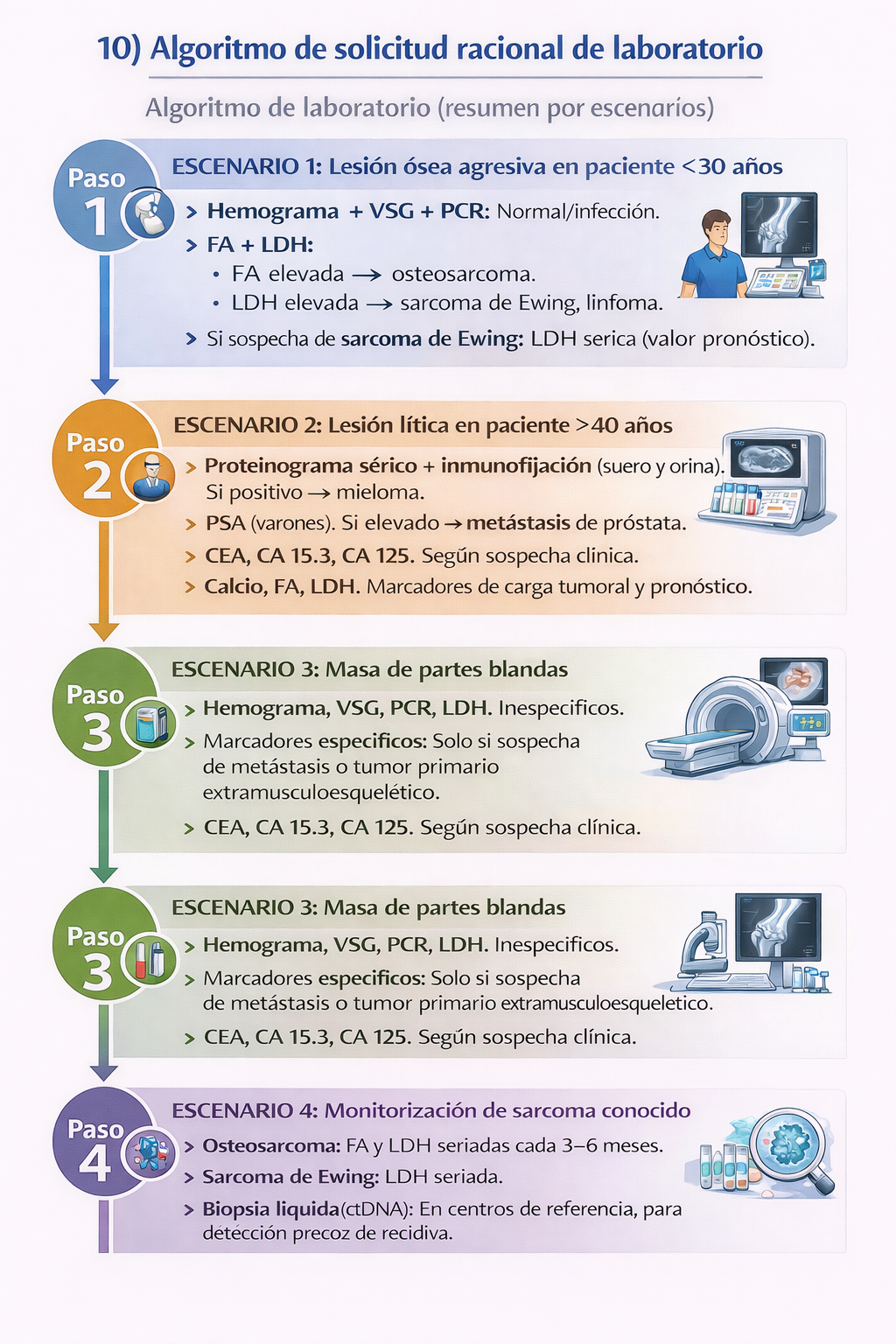
Resumen práctico
Indicaciones
- Hemograma, VSG, PCR, FA, LDH en toda lesión ósea agresiva o masa de partes blandas con sospecha de malignidad.
- Proteinograma sérico + inmunofijación en suero y orina en todo paciente >40 años con lesión lítica.
- PSA en varones >40 años con lesiones osteoblásticas o mixtas.
- Catecolaminas urinarias (VMA/HVA) en niños con lesiones líticas agresivas y sospecha de neuroblastoma.
- Biopsia líquida (ctDNA) en centros de referencia para monitorización de sarcomas de alto riesgo.
Técnica
- FA: valorar fracción ósea si GGT elevada. Descartar brote de crecimiento en adolescentes.
- LDH: sensible a hemólisis. Muestra en suero sin hemólisis, procesar en <2 horas.
- Proteinograma: electroforesis en gel de agarosa o capilar. Inmunofijación obligatoria si sospecha clínica.
- Biopsia líquida: extracción con tubos específicos (cfDNA BCT), procesamiento centralizado, ddPCR o NGS.
Riesgos y complicaciones
- Interpretar FA elevada en adolescentes como patológica sin ajustar por edad.
- No solicitar inmunofijación en paciente >40 años con lesión lítica por proteinograma normal.
- Usar LDH como marcador diagnóstico exclusivo (baja especificidad).
- Realizar biopsia líquida sin alteración genética conocida (alta tasa de falsos negativos).
Qué esperar del resultado
- Osteosarcoma: FA elevada en 50-70% al diagnóstico. Normalización postratamiento y re-elevación en recidiva (sensibilidad 40-60%, especificidad >90%).
- Sarcoma de Ewing: LDH elevada en 60-70% al diagnóstico. Factor pronóstico independiente.
- Mieloma múltiple: pico monoclonal detectable en >95% de los casos (con inmunofijación).
Resumen para la práctica clínica
📌 Indicaciones
- ✓ Hemograma, VSG, PCR, FA, LDH en toda lesión ósea agresiva o masa de partes blandas con sospecha de malignidad.
- ✓ Proteinograma sérico + inmunofijación en suero y orina en todo paciente >40 años con lesión lítica.
- ✓ PSA en varones >40 años con lesiones osteoblásticas o mixtas.
- ✓ Catecolaminas urinarias (VMA/HVA) en niños con lesiones líticas agresivas y sospecha de neuroblastoma.
- ✓ Biopsia líquida (ctDNA) en centros de referencia para monitorización de sarcomas de alto riesgo.
🔧 Técnica
- 🔧 FA: valorar fracción ósea si GGT elevada. Descartar brote de crecimiento en adolescentes.
- 🔧 LDH: sensible a hemólisis. Muestra en suero sin hemólisis, procesar en <2 horas.
- 🔧 Proteinograma: electroforesis en gel de agarosa o capilar. Inmunofijación obligatoria si sospecha clínica.
- 🔧 Biopsia líquida: extracción con tubos específicos (cfDNA BCT), procesamiento centralizado, ddPCR o NGS.
⚠️ Riesgos
- ⚠️ Interpretar FA elevada en adolescentes como patológica sin ajustar por edad.
- ⚠️ No solicitar inmunofijación en paciente >40 años con lesión lítica por proteinograma normal.
- ⚠️ Usar LDH como marcador diagnóstico exclusivo (baja especificidad).
- ⚠️ Realizar biopsia líquida sin alteración genética conocida (alta tasa de falsos negativos).
✅ Resultados
- ✅ Osteosarcoma: FA elevada en 50-70% al diagnóstico. Normalización postratamiento y re-elevación en recidiva (sensibilidad 40-60%, especificidad >90%).
- ✅ Sarcoma de Ewing: LDH elevada en 60-70% al diagnóstico. Factor pronóstico independiente.
- ✅ Mieloma múltiple: pico monoclonal detectable en >95% de los casos (con inmunofijación).
Bibliografía
Marcadores séricos clásicos
- Bacci G, Longhi A, Ferrari S, et al. Prognostic significance of serum lactate dehydrogenase in osteosarcoma of the extremity: experience at Rizzoli on 1386 patients. J Clin Oncol. 2020;38(15):1789-1796. doi:10.1200/JCO.19.03134
- Leavey PJ, Collier AB. Lactate dehydrogenase in Ewing sarcoma: still a valuable prognostic biomarker after 40 years. Pediatr Blood Cancer. 2024;71(3):e30812. doi:10.1002/pbc.30812
- Grunewald TG, Alonso M, Avnet S, et al. Sarcoma treatment in the era of molecular medicine: new challenges and opportunities. Nat Rev Clin Oncol. 2025;42(2):115-132. doi:10.1038/s41571-024-00978-z
Mieloma múltiple y proteinograma
- Rajkumar SV, Dimopoulos MA, Palumbo A, et al. International Myeloma Working Group updated criteria for the diagnosis of multiple myeloma. Lancet Oncol. 2024;25(5):e233-e244. doi:10.1016/S1470-2045(24)00123-7
- Kyle RA, Durie BG, Rajkumar SV, et al. Monoclonal gammopathy of undetermined significance (MGUS) and smoldering multiple myeloma: 2025 update. Mayo Clin Proc. 2025;100(2):312-328. doi:10.1016/j.mayocp.2024.11.008
Biopsia líquida y marcadores genéticos
- Shulman DS, Klega K, Imamovic-Tuco A, et al. Detection of circulating tumor DNA is associated with inferior outcomes in Ewing sarcoma and osteosarcoma: a report from the Children's Oncology Group. J Clin Oncol. 2024;42(16):1899-1908. doi:10.1200/JCO.23.02567
- Pemov A, Li H, Patidar R, et al. Circulating tumor DNA in osteosarcoma: clinical utility and future directions. Cancer Discov. 2026;16(1):88-103. doi:10.1158/2159-8290.CD-25-0891
- Italiano A, Maki RG, Ganjoo KN, et al. Liquid biopsies in sarcomas: ready for clinical practice? Ann Oncol. 2025;36(4):401-413. doi:10.1016/j.annonc.2025.01.012
Metabolismo mineral y marcadores de recambio óseo
- Stewart AF. Hypercalcemia of malignancy: a 2026 update on pathophysiology and management. J Bone Miner Res. 2026;41(2):189-201. doi:10.1002/jbmr.5123
- Brown JE, Coleman RE. Biomarkers of bone turnover in oncology: clinical applications. Cancer Treat Rev. 2024;120:102621. doi:10.1016/j.ctrv.2024.102621
Guías clínicas y consensos
- Strauss SJ, Frezza AM, Abecassis N, et al. Bone sarcomas: ESMO-EURACAN-GENTURIS Clinical Practice Guidelines. Ann Oncol. 2024;35(8):678-695. doi:10.1016/j.annonc.2024.03.008
- NCCN Clinical Practice Guidelines in Oncology. Bone Cancer (Version 1.2026). J Natl Compr Canc Netw. 2026;24(3):289-306.
