Histiocitoma Fibroso Benigno Profundo (Deep Fibrous Histiocytoma): Actualización Diagnóstica y Terapéutica 2026
El histiocitoma fibroso benigno profundo (también denominado deep fibrous histiocytoma / deep benign fibrous histiocytoma) es una neoplasia benigna de partes blandas profundas, incluida por la WHO 2020 (5ª ed.) en el grupo de los “so-called fibrohistiocytic tumours”. Su comportamiento habitual es indolente, con posibilidad de recidiva local si la exéresis es marginal o incompleta y con metástasis rara descrita en series seleccionadas.
Definición y clasificación actual (WHO 2020)
Terminología actualizada (WHO 2020)
- 📌 Nombre recomendado (inglés): Deep fibrous histiocytoma / Deep benign fibrous histiocytoma
- 📌 Nombre habitual (español): Histiocitoma fibroso benigno profundo (HFBP)
- 📌 Sinónimos: Fibrohistiocitoma profundo; Histiocitoma profundo; Tumor fibrohistiocítico profundo benigno
- 📌 Categoría WHO: Benigno (grupo: “so-called fibrohistiocytic tumours”)
- 📌 Código ICD-O: 8831/0 (incluye “deep benign fibrous histiocytoma” como sinónimo/relacionado en ICD-O-3.2)
El dermatofibroma es frecuente y se sitúa en dermis con extensión variable a subcutis. El HFBP es raro y se define por una localización subcutánea profunda o en partes blandas profundas (y, en casos excepcionales, localizaciones viscerales), con mayor relevancia clínica por el diagnóstico diferencial con sarcomas de bajo grado y DFSP.
Conceptos actuales sobre histogénesis
Se considera una neoplasia de células fusiformes/ovoides con diferenciación fibroblástica-histiocítica. No hay factores etiológicos consistentes; la asociación con traumatismo previo es anecdótica y no demuestra causalidad.
Epidemiología y características demográficas
| Parámetro | Datos (series clínicas publicadas) | Comentarios |
|---|---|---|
| Edad | 6–84 años (mediana ~37) | Predomina en adultos; puede verse en niños |
| Sexo | Varones > mujeres (aprox. 41/28 en una serie amplia) | Ligero predominio masculino |
| Localización | Extremidades (~58%) > cabeza/cuello (~22%) > tronco (~11%) | También descrito en retroperitoneo/mediastino/pelvis (~9%) |
| Tamaño | 0,5–25 cm (mediana ~3 cm) | Los casos profundos “centrales” pueden alcanzar gran tamaño |
| Frecuencia | Entidad rara | No hay cifras poblacionales robustas por baja incidencia y sesgo de derivación |
Presentación clínica y hallazgos físicos
Características clínicas típicas
- 🔹 Crecimiento: lento, progresivo
- 🔹 Síntomas: a menudo asintomático; dolor ocasional si es grande o en localización confinada
- 🔹 Exploración: masa firme, habitualmente bien delimitada; piel suprayacente normal
Localizaciones menos frecuentes (pero descritas)
- Retroperitoneo / mediastino / pelvis: pueden debutar con gran tamaño
- Visceral: casos aislados publicados (p. ej., riñón)
- Cabeza y cuello: relevante por complejidad quirúrgica y control local
Evaluación clínica inicial
Registrar tamaño, planos, relación con estructuras neurovasculares y síntomas. Si es profunda (> fascia) o >5 cm, aplicar circuito estándar de “masa de partes blandas” (RM + biopsia con aguja gruesa en unidad con experiencia).
Diagnóstico por imagen: enfoque práctico
Ecografía
Útil como primer escalón en masas subcutáneas: lesión sólida, bien delimitada, con vascularización variable. No permite un diagnóstico específico.
Resonancia Magnética (RM)
- T1: iso- a discretamente hipointensa respecto a músculo
- T2: variable (desde hiperintensa hasta baja/intermedia si hay componente fibroso/hialinizado)
- Realce: variable (frecuentemente evidente)
- Morfología: tendencia a lesión bien circunscrita; ocasional pseudocápsula
La RM es clave para planificar la biopsia/exéresis y para valorar signos de agresividad (necrosis, infiltración franca, etc.).
TC
Complementaria en localizaciones profundas “centrales” (retroperitoneo/mediastino/pelvis) y para planificación quirúrgica. La TC torácica puede considerarse en lesiones grandes/atípicas o tras recidivas, dado que la metástasis es rara pero descrita.
Histopatología e inmunohistoquímica (criterios prácticos)
Macroscopia
- Apariencia: nódulo bien circunscrito, a veces encapsulado/pseudocapsulado
- Color: blanco-grisáceo a amarillo-marrón
- Necrosis: inusual (si existe, obliga a reevaluar y muestrear ampliamente)
Microscopia
- Patrón estoriforme con células fusiformes/ovoides blandas
- Infiltrado linfocitario variable
- Células gigantes / foam cells en una proporción significativa de casos
- Vasos tipo hemangiopericitoma-like y hialinización estromal pueden observarse
- Mitosis: variable (mediana alrededor de 3/10 HPF; algunos casos pueden mostrar recuentos altos sin comportarse como sarcoma)
Existen variantes atípicas (pleomorfismo focal) dentro del espectro; la correlación clínico-radiológica y el muestreo adecuado son esenciales.
Panel inmunohistoquímico orientativo (con notas de interpretación)
| Marcador | Patrón esperado (orientativo) | Clave práctica |
|---|---|---|
| CD68 | Positivo (a menudo focal) | Apoya diferenciación histiocítica; no es específico |
| CD163 | Positivo (variable) | Útil como marcador histiocítico; tampoco es absoluto |
| Factor XIIIa | Frecuentemente positivo (variable) | Ayuda en el eje DF/DFSP, pero con excepciones |
| CD34 | Variable (puede ser positivo en un subgrupo) | No usar “CD34+ = DFSP” como regla. Integrar con morfología y, si procede, FISH |
| SMA | Variable (focal en parte de los casos) | Diferenciación miofibroblástica ocasional |
| Desmina | Habitualmente negativa; rara positividad focal | No excluye si es mínima/focal; revisar diferencial si es difusa |
| S100 / SOX10 | Negativos | Ayuda a excluir tumores neurales/melanocíticos |
| STAT6 | Negativo (si positivo nuclear fuerte, pensar en SFT) | Para excluir SFT cuando el patrón vascular confunde |
| Ki-67 | Bajo en la mayoría | Apoya comportamiento indolente (si alto, reevaluar) |
Estudios moleculares (cuándo sí aportan)
No hay una alteración genética única “obligatoria” para HFBP. En la práctica, el estudio molecular se reserva para: (1) descartar DFSP (FISH/RT-PCR para COL1A1::PDGFB) si la morfología/inmuno lo sugieren, y (2) descartar miméticos concretos (p. ej., SS18-SSX en sarcoma sinovial) cuando el caso es atípico.
Diagnóstico diferencial crítico
- DFSP: infiltrativo, CD34 habitualmente difuso; confirmar con COL1A1::PDGFB si hay duda
- UPS (antes “MFH”): atipia marcada, mitosis atípicas, necrosis frecuente
- SFT: STAT6 nuclear; fusión NAB2-STAT6
Diferencial ampliado (según morfología / inmuno)
| Entidad | Claves morfológicas | Marcadores / prueba |
|---|---|---|
| Sarcoma sinovial | Monomórfico, patrón sólido/bifásico variable | TLE1; SS18-SSX |
| Leiomiosarcoma | Fascículos, núcleos “puro habano” | Desmina/SMA/h-caldesmon difusos |
| Fibromatosis (desmoide) | Infiltrativo, colágeno abundante | β-catenina nuclear; CTNNB1 |
| Schwannoma | Antoni A/B, Verocay | S100 / SOX10 difusos |
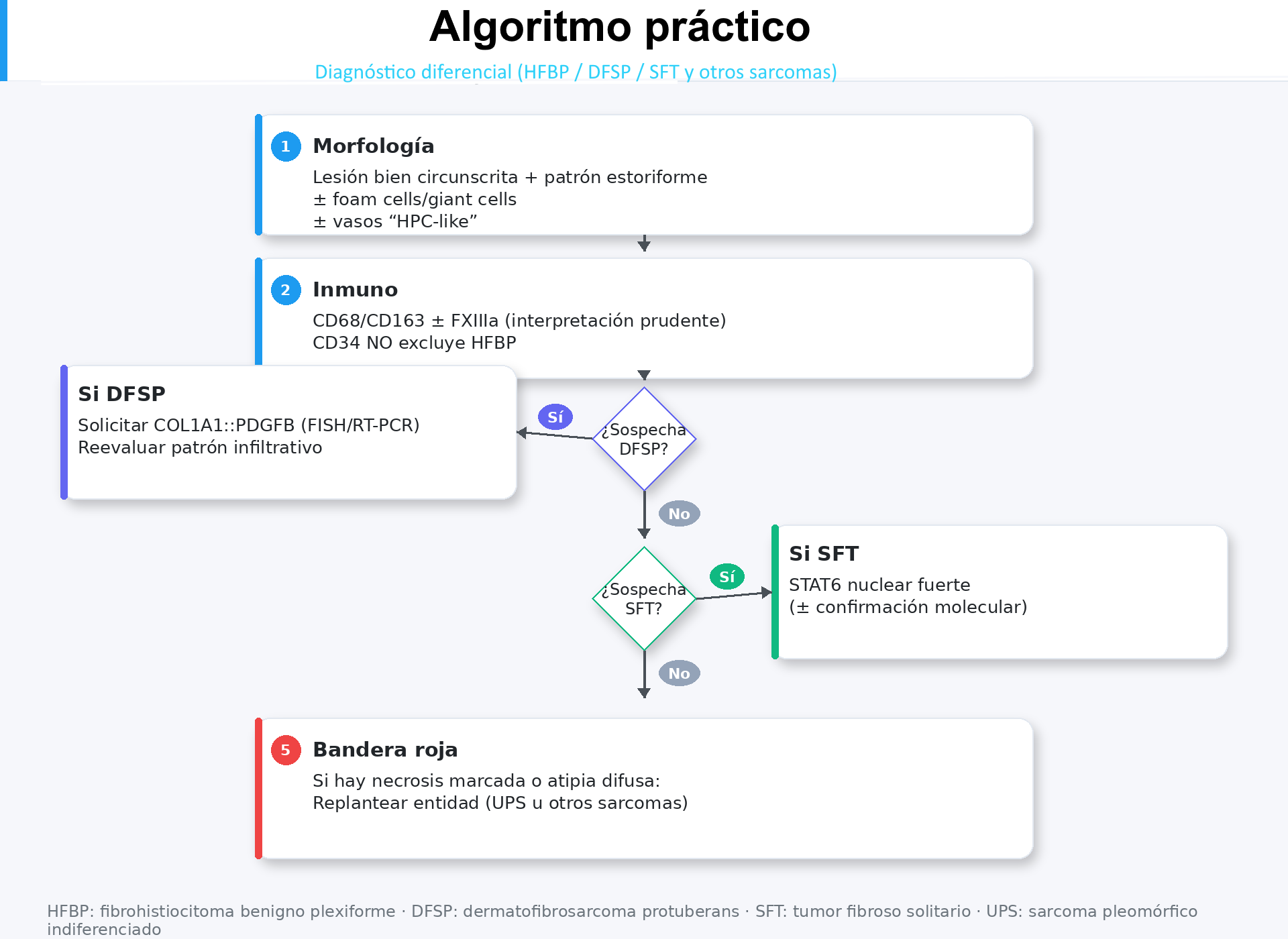
- Morfología: lesión bien circunscrita + estoriforme ± foam cells/giant cells ± vasos “HPC-like”.
- Inmuno: CD68/CD163 ± FXIIIa con interpretación prudente; CD34 no excluye HFBP.
- Si sospecha DFSP: solicitar COL1A1::PDGFB (FISH/RT-PCR) y reevaluar patrón infiltrativo.
- Si sospecha SFT: STAT6 nuclear fuerte (± confirmación molecular).
- Si hay necrosis marcada/atipia difusa: replantear entidad (UPS u otros sarcomas).
Tratamiento actual: estándares razonables
7.1 Cirugía
- Objetivo: evitar exéresis marginal/incompleta (principal factor asociado a recidiva)
- “Wide margins” tipo sarcoma: no son obligatorios de rutina si se logra resección completa preservando función
- Planificación: RM preoperatoria + circuito de tumor de partes blandas si profunda / >5 cm
7.2 Márgenes y riesgo de recidiva
| Situación | Descripción | Conducta |
|---|---|---|
| Exéresis completa | Márgenes libres | Seguimiento clínico; imagen si profunda/alto riesgo de recidiva |
| Exéresis marginal / incompleta | Márgenes afectados o duda de radicalidad | Re-exéresis si es factible (reduce claramente recidiva) |
| Recidiva | Reaparición local | Re-exéresis; reevaluar diagnóstico (muestreo amplio + diferencial) |
7.3 Radioterapia
No está indicada de forma rutinaria. Solo se valora en escenarios excepcionales (p. ej., múltiples recidivas no resecables o localizaciones críticas donde no puede lograrse control local quirúrgico sin morbilidad inaceptable), siempre tras discusión multidisciplinar.
7.4 Terapia sistémica
No tiene papel establecido en HFBP típico. Si existe comportamiento biológico atípico (p. ej., metástasis) se maneja de forma individualizada en comité, y lo primero es reconfirmar diagnóstico (morfología + inmuno + pruebas moleculares dirigidas).
Pronóstico, seguimiento y complicaciones
8.1 Recidiva local
Factores que obligan a seguimiento más estrecho: lesión profunda “central”, gran tamaño, recidiva previa, necrosis o atipia significativa, o incertidumbre diagnóstica.
8.2 Metástasis
8.3 Seguimiento recomendado (práctico)
| Situación | Examen clínico | Imagen local | Imagen torácica |
|---|---|---|---|
| Exéresis completa, superficial/subcutánea | Cada 6–12 meses (2–3 años) | Solo si clínica | No rutinaria |
| Profundo / grande / recidivado | Cada 6 meses (2–3 años), luego anual hasta 5 años | RM anual 2–3 años (según riesgo) | Considerar TC/Rx según riesgo/atipia |
| Atípico o comportamiento agresivo | Individualizar en comité | RM programada | TC torácica según protocolo |
Este esquema es deliberadamente prudente para lesiones profundas/atípicas por la rareza de la entidad y la existencia de metástasis descrita en series seleccionadas.
8.4 Complicaciones potenciales
- Recidiva local (principal complicación si resección no completa)
- Morbilidad quirúrgica en localizaciones complejas
- Diagnóstico erróneo (sobre-tratamiento como sarcoma o infra-tratamiento como lesión banal)
- Ansiedad del paciente asociada a control evolutivo
Bibliografía y recursos
Clasificación WHO / revisiones
- WHO Classification of Tumours Editorial Board. Soft Tissue and Bone Tumours. 5th ed. Lyon: IARC; 2020.
- Sbaraglia M, et al. The 2020 WHO Classification of Soft Tissue Tumours (resumen/revisión). Histopathology. 2020.
Serie clínica clave
- Gleason BC, Fletcher CDM. Deep “benign” fibrous histiocytoma: clinicopathologic analysis of 69 cases indicating occasional metastatic potential. Am J Surg Pathol. 2008;32(3):354–362.
Inmunohistoquímica
- West KL, et al. Factor XIIIa y CD34 (marcadores útiles con excepciones) en fibrohistiocíticos/DFSP. J Cutan Pathol. 2014.
- Doyle LA, et al. STAT6 como marcador de SFT y su rendimiento frente a miméticos. Mod Pathol. 2014.
Codificación
- ICD-O-3.2 (OMS/IARC). Morfología 8831/0 (incluye “deep benign fibrous histiocytoma” como sinónimo/relacionado).
Resumen práctico
Indicaciones
- Masa de partes blandas profunda o subcutánea con crecimiento lento y morfología sugestiva de lesión fibrohistiocítica.
- Lesión que requiere diferencial con DFSP y sarcomas de bajo grado.
- Recidiva local tras exéresis previa marginal/incompleta.
- Localizaciones complejas (cabeza/cuello, retroperitoneo/mediastino/pelvis) para planificación en unidad especializada.
Técnica
- RM con contraste para caracterización y planificación (especialmente si profunda o >5 cm).
- Biopsia con aguja gruesa (core biopsy) si la lesión es profunda / >5 cm / sospechosa.
- Correlación morfológica + panel inmunohistoquímico (CD68, CD163, FXIIIa, CD34, STAT6, S100/SOX10, SMA ± otros según caso).
- Si hay duda con DFSP: FISH/RT-PCR para COL1A1::PDGFB.
- Exéresis completa con confirmación histológica de márgenes libres.
Riesgos y complicaciones
- Recidiva local asociada a exéresis marginal o incompleta (en series clínicas, ~20% en ese escenario).
- Morbilidad quirúrgica en localizaciones profundas/centrales.
- Dificultad diagnóstica por solapamiento morfológico e inmuno con DFSP/SFT/sarcomas de bajo grado.
- Metástasis rara descrita en series seleccionadas (posible sesgo de consulta), más probable en tumores grandes y/o con necrosis/atipia.
Qué esperar del resultado
- Pronóstico global excelente tras exéresis completa.
- Control local alto cuando se evita la resección marginal/incompleta.
- Metástasis: evento raro, pero obliga a vigilancia prudente en tumores profundos/grandes/atípicos.
- Calidad de vida generalmente buena tras tratamiento adecuado.
Resumen para la práctica clínica
📌 Indicaciones
- ✓ Masa de partes blandas profunda o subcutánea con crecimiento lento y morfología sugestiva de lesión fibrohistiocítica.
- ✓ Lesión que requiere diferencial con DFSP y sarcomas de bajo grado.
- ✓ Recidiva local tras exéresis previa marginal/incompleta.
- ✓ Localizaciones complejas (cabeza/cuello, retroperitoneo/mediastino/pelvis) para planificación en unidad especializada.
🔧 Técnica
- 🔧 RM con contraste para caracterización y planificación (especialmente si profunda o >5 cm).
- 🔧 Biopsia con aguja gruesa (core biopsy) si la lesión es profunda / >5 cm / sospechosa.
- 🔧 Correlación morfológica + panel inmunohistoquímico (CD68, CD163, FXIIIa, CD34, STAT6, S100/SOX10, SMA ± otros según caso).
- 🔧 Si hay duda con DFSP: FISH/RT-PCR para COL1A1::PDGFB.
- 🔧 Exéresis completa con confirmación histológica de márgenes libres.
⚠️ Riesgos
- ⚠️ Recidiva local asociada a exéresis marginal o incompleta (en series clínicas, ~20% en ese escenario).
- ⚠️ Morbilidad quirúrgica en localizaciones profundas/centrales.
- ⚠️ Dificultad diagnóstica por solapamiento morfológico e inmuno con DFSP/SFT/sarcomas de bajo grado.
- ⚠️ Metástasis rara descrita en series seleccionadas (posible sesgo de consulta), más probable en tumores grandes y/o con necrosis/atipia.
✅ Resultados
- ✅ Pronóstico global excelente tras exéresis completa.
- ✅ Control local alto cuando se evita la resección marginal/incompleta.
- ✅ Metástasis: evento raro, pero obliga a vigilancia prudente en tumores profundos/grandes/atípicos.
- ✅ Calidad de vida generalmente buena tras tratamiento adecuado.
