Hemangioendotelioma — Actualización 2026
Tumor vascular de malignidad intermedia (OMS 2020), caracterizado por proliferación de células endoteliales con apariencia epitelioide o fusiforme, que muestra un comportamiento biológico situado entre el hemangioma benigno y el angiosarcoma de alto grado. Aunque su potencial metastásico suele ser limitado, es variable según el subtipo y la localización; tiene capacidad de recidiva local y, en una minoría de casos, puede producir metástasis a distancia. La multifocalidad es una característica distintiva, especialmente en la forma epitelioide.
En 1 minuto
Tumor vascular de malignidad intermedia, con potencial metastásico bajo a moderado pero recidiva local frecuente. No es angiosarcoma.
Hemangioendotelioma epitelioide (HEE). >80% de casos óseos.
Adultos jóvenes (20-30 años), ligero predominio masculino.
Multifocalidad en 25-50%, a menudo confinada a un miembro (enfermedad multicéntrica).
Huesos largos (metáfisis/diáfisis), columna, cráneo, pelvis.
Lesión lítica, expansiva, a veces con patrón trabeculado o "en panal". Sin reacción perióstica.
Translocación WWTR1-CAMTA1 (≈90% HEE) o YAP1-TFE3. ¡Diana terapéutica!
Resección amplia en lesiones solitarias. Radioterapia para localizaciones complejas. Vigilancia en multifocal indolente.
Definición y concepto actual (OMS 2020/2023)
Conceptos clave
- No es un angiosarcoma: El angiosarcoma es de alto grado, con marcada atipia, mitosis abundantes y necrosis. El hemangioendotelioma es de grado intermedio.
- No es una malformación: Es una neoplasia verdadera (proliferación clonal).
- Multifocalidad ≠ metástasis: Las lesiones múltiples en un mismo miembro o región suelen ser enfermedad multicéntrica (diseminación intralinfática/hematógena regional), no metástasis a distancia. El pronóstico suele ser mejor que en enfermedad metastásica verdadera.
Sinónimos (obsoletos, evitar)
- Sarcoma hemangioendotelial
- Angiosarcoma de bajo grado
- Hemangioendotelioma maligno
Uso correcto: Denominar siempre según la variante específica (ej., "Hemangioendotelioma epitelioide").
Clasificación OMS 2020 de Tumores Vasculares de Malignidad Intermedia
| Entidad | Localización típica | Genética | Comportamiento |
|---|---|---|---|
| Hemangioendotelioma epitelioide (HEE) | Hueso, partes blandas, pulmón, hígado | Fusión WWTR1-CAMTA1 (≈90%) Fusión YAP1-TFE3 (5-10%) |
Intermedio. Metástasis en 20-30%. Supervivencia 5 años: 70-80%. |
| Hemangioendotelioma kaposiforme | Retroperitoneo, piel, tejido blando profundo (niños) | No conocida | Intermedio. Asociado a fenómeno de Kasabach-Merritt (coagulopatía de consumo). |
| Hemangioendotelioma retiforme | Piel y tejido subcutáneo (extremidades) | No conocida | Intermedio. Recidiva local frecuente. Metástasis raras. |
| Hemangioendotelioma compuesto | Tejido subcutáneo (extremidades) | No conocida | Intermedio. Recidiva local. Metástasis excepcionales. |
| Hemangioendotelioma de células fusiformes | Hueso, tejido blando | No conocida | Intermedio. Menos agresivo que HEE. |
Nota: El hemangioendotelioma epitelioide es, con diferencia, la variante más relevante en ortopedia oncológica.
Epidemiología y manifestaciones clínicas
| Parámetro | Datos | Comentario práctico |
|---|---|---|
| Frecuencia | <1% de todos los tumores óseos malignos | Entidad muy rara. Más frecuente en partes blandas que en hueso. |
| Edad | Pico 20-30 años (rango: 10-75) | En formas multifocales, pacientes 10 años más jóvenes. |
| Sexo | Ligero predominio masculino (1.5:1) | |
| Localización ósea |
|
La multifocalidad es una característica distintiva del HEE óseo. |
| Síntomas |
|
La duración de los síntomas es muy variable: desde semanas hasta años. |
| Partes blandas | Tejido subcutáneo profundo de extremidades, tronco, cabeza y cuello. | Clínica: masa palpable, a veces dolorosa. Crecimiento lento. |
Estudios de imagen — Hallazgos y protocolo 2026
Radiografía simple
- Lesión lítica pura, bien o mal definida según agresividad.
- Patrón expansivo: Puede simular "pompa de jabón" o panal de abeja (trabeculado grosero).
- Cortical: Adelgazada, puede estar expandida. Destrucción parcial en lesiones agresivas.
- Reacción perióstica: Ausente en la mayoría de casos (clave diferencial con sarcoma de Ewing u osteosarcoma).
- Masa de partes blandas: Infrecuente.
Tomografía Computarizada (TC)
- Evalúa mejor el patrón trabeculado y la integridad cortical.
- ¿Puede mostrar matriz osteoide? No. Si hay, pensar en osteosarcoma.
- Útil para biopsia guiada y planificación quirúrgica.
Resonancia Magnética (RM)
- Señal: Heterogénea. Hipo/isointenso en T1, hiperintenso en T2 (componente vascular).
- Realce: Moderado a intenso, heterogéneo, con contraste.
- Patrón: Pueden verse niveles líquido-líquido (por quistes hemorrágicos).
- Multifocalidad: La RM de extremidad completa es muy recomendable para detectar lesiones satélite o multicéntricas en el mismo hueso/miembro.
Medicina Nuclear
- Gammagrafía ósea (Tc-99m): Aumento de captación. Útil para cribado de enfermedad multifocal.
- PET/TC con 18F-FDG: Herramienta útil para estadificación según disponibilidad y contexto clínico. El HEE suele tener baja avidez metabólica (SUV bajo). Una captación muy alta debe hacer sospechar angiosarcoma.
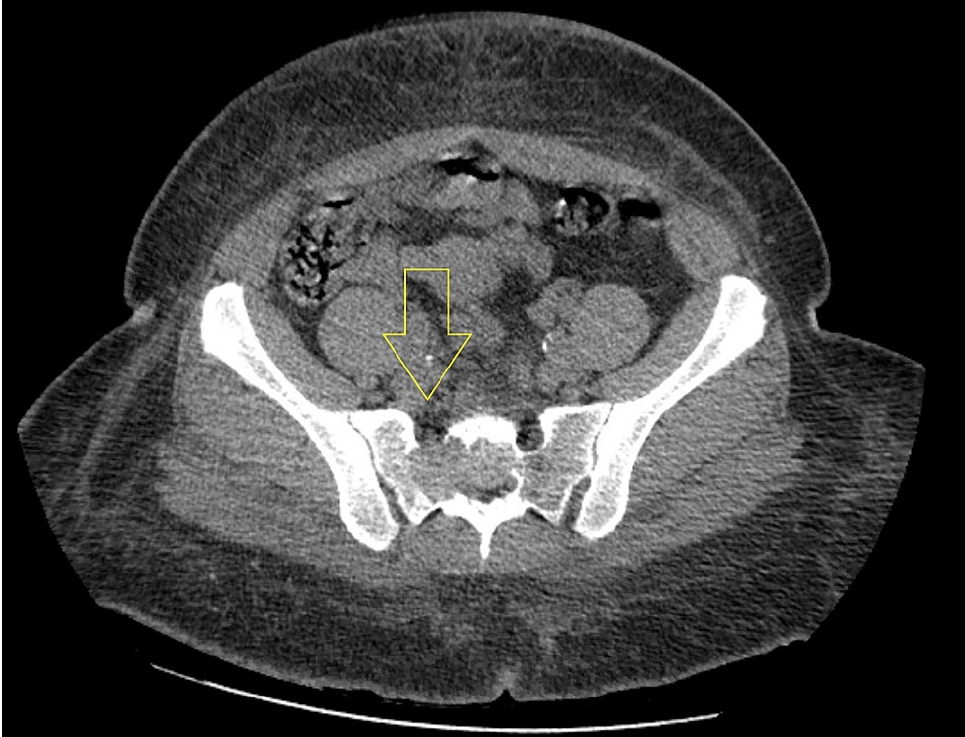
- Radiografía simple de la zona afectada.
- RM de extremidad completa (o del segmento óseo completo) con contraste para evaluar extensión local y multifocalidad.
- Estadificación sistémica (PET/TC corporal total o alternativas según protocolo local: gammagrafía ósea + TC tórax/abdomen) para descartar otras localizaciones.
Histopatología, inmunohistoquímica y genética molecular
Hallazgos macroscópicos
- Masa hemorrágica, blanda, rojo-oscura.
- Puede estar bien circunscrita o tener márgenes infiltrativos.
- Septos fibrosos que atraviesan el tumor.
Hallazgos microscópicos (HEE)
- Células epitelioides: Grandes, citoplasma eosinófilo abundante, núcleo vesicular.
- Dispuestas en cordones, nidos o células individuales.
- Vacuolas citoplasmáticas que ocasionalmente contienen eritrocitos (lumen vascular primitivo).
- Estroma: Fibroso a mixoide, a veces hialino (puede simular matriz condroide).
- Atipia: Leve a moderada. Mitosis: <5 por 10 CGA (en HEE).
- Necrosis: Infrecuente (si es extensa, sospechar angiosarcoma).
- Infiltrado inflamatorio crónico (linfocitos, células plasmáticas).
Inmunohistoquímica (IHC)
- CD31 + (membrana): Marcador endotelial más sensible.
- ERG + (nuclear): Específico y sensible.
- FLI1 + (nuclear).
- Factor VIII (FvW) + (citoplasma granular): Menos sensible.
- Queratinas: Focalmente + en 30% (¡cuidado con confundir con carcinoma!).
- S100, EMA, Desmina: Negativos (para diferencial).
Genética molecular (¡esencial!)
- Fusión WWTR1-CAMTA1 (t(1;3)): Presente en >90% de HEE. Muy específica (no se encuentra en otros sarcomas vasculares). Detectable por FISH o NGS.
- Fusión YAP1-TFE3 (t(X;11)): Presente en 5-10% de HEE (variante). Asociada a morfología más fusiforme y a veces translocación X;11.
- Mutaciones: No hay mutaciones recurrentes en BRAF, RAS, etc.
Utilidad clínica: Confirmar diagnóstico, diferenciar de mimickers y, potencialmente, guiar terapia dirigida.
Diagnóstico diferencial crítico
Diferencial radiológico
Lesión lítica expansiva en adulto joven:
- Tumor de células gigantes (TCG): Subarticular, epífisis, bordes no escleróticos, más agresivo.
- Quiste óseo aneurismático (QOA): Niveles líquido-líquido, expansivo, edad <20 años.
- Metástasis lítica: >40 años, antecedente oncológico, multifocal no regional.
- Fibrosarcoma / HFM (actual SIP): Patrón más agresivo, permeativo, sin patrón trabeculado.
- Linfoma óseo: Masa de partes blandas desproporcionada.
- Plasmocitoma: >40 años, lesión perforada, proteinograma.
Diferencial histopatológico
- Metástasis de carcinoma (renal, tiroides, pulmón): IHC: queratinas +, EMA +, CD31/ERG -. Morfología similar.
- Melanoma: S100 +, SOX10 +, HMB45 +, MelanA +.
- Angiosarcoma: Ver criterios de alto grado.
- Condrosarcoma mixoide: Matriz condroide, S100 +.
- Adamantinoma: Patrón bifásico (epitelial + fibroso), queratinas +, CD31 -.
- Osteosarcoma telangiectásico: Osteoide tumoral +, CD31 -.
- Sarcoma epitelioide: INI1 pérdida, queratinas +, CD31 -.
Clave para el diagnóstico: IHC endotelial (CD31, ERG) + FISH para fusión WWTR1-CAMTA1 o YAP1-TFE3. Esto distingue al HEE de TODOS sus mimickers.
Tratamiento — Abordaje multimodal 2026
Lesión solitaria accesible (huesos largos, pelvis, escápula)
- Resección quirúrgica amplia (margen R0): Estándar. Reduce el riesgo de recidiva local (aprox. de 30% a <10% en series).
- Curetaje ± adyuvantes: No recomendado. Alta tasa de recidiva. Reservar solo para localizaciones donde la resección amplia cause morbilidad severa (ej., acetábulo), y complementar con radioterapia.
- Reconstrucción: Según localización: prótesis megaprótesis, aloinjerto, artroplastia.
Localizaciones complejas (columna, base cráneo, acetábulo)
- Radioterapia: Opción muy utilizada en control local cuando la cirugía en bloque no es factible. Dosis orientativa: 50-60 Gy en fraccionamiento convencional. En series publicadas se describe buen control local.
- Cirugía: Descompresión y estabilización si hay déficit neurológico o inestabilidad. La resección completa (en bloque) es ideal pero no siempre factible.
- Radioterapia postoperatoria: Indicada si márgenes positivos o cercanos.
Enfermedad multifocal (múltiples lesiones en un miembro)
- Observación vigilante: Opción válida si las lesiones son asintomáticas, estables y de bajo grado. Muchos pacientes tienen curso indolente.
- Radioterapia: Para lesiones sintomáticas, en localizaciones críticas (columna).
- Amputación: Solo si dolor refractario, fracturas patológicas múltiples, o imposibilidad de control local con cirugía conservadora + RT. Es excepcional.
- Quimioterapia: Evidencia limitada en enfermedad multifocal estable. Considerar solo si progresión clara o enfermedad metastásica.
Enfermedad metastásica (pulmón, hígado)
- Tratamiento sistémico: No hay un estándar. Se han usado regímenes de sarcoma (doxorrubicina, ifosfamida, pazopanib).
- Inhibidores de tirosina quinasa: Sorafenib, sunitinib han mostrado actividad en casos aislados.
- Inmunoterapia: Casos aislados con respuesta a anti-PD1 (pembrolizumab).
- Metastasectomía: Indicada si enfermedad oligometastásica.
Algoritmo práctico resumido
- Diagnóstico confirmado (biopsia + IHC + genética).
- Estadificar: ¿Enfermedad solitaria, multifocal regional o metastásica?
- Localización accesible y lesión solitaria → Resección amplia (R0).
- Localización compleja (columna, base cráneo) → Radioterapia definitiva (50-60 Gy) y/o cirugía si inestabilidad/déficit.
- Multifocal asintomática → Observación. RT paliativa para lesiones sintomáticas.
- Metástasis → Considerar metastasectomía y/o terapia sistémica (ensayo clínico si disponible).
Pronóstico y seguimiento
| Factor | Pronóstico favorable | Pronóstico desfavorable |
|---|---|---|
| Tipo | HEE variante YAP1-TFE3 (mejor pronóstico) | HEE convencional WWTR1-CAMTA1 (riesgo metastásico 20-30%) |
| Localización | Hueso (multifocal regional) | Hígado, pulmón (peor pronóstico) |
| Tamaño | < 3 cm | > 5 cm |
| Actividad mitótica | < 2 mitosis/10 CGA | > 3 mitosis/10 CGA |
| Atipia nuclear | Ausente/leve | Moderada/marcada |
| Necrosis | Ausente | Presente |
| Resección quirúrgica | Margen amplio (R0) | Margen intralesional (R1/R2) |
Datos de supervivencia (HEE óseo, series modernas 2020-2025)
- Supervivencia global a 5 años: 70-80%.
- Supervivencia libre de enfermedad a 5 años: 60-70%.
- Recidiva local: 10-20% (más frecuente si curetaje o márgenes inadecuados).
- Metástasis a distancia: 20-30%. Principalmente pulmón, hígado, hueso.
- Transformación a angiosarcoma: Rara (<5%). Asociada a peor pronóstico.
Seguimiento orientativo (adaptar a protocolos locales y al riesgo)
- Primeros 2 años (máximo riesgo): Examen físico y RM local cada 3-4 meses. TC tórax cada 6 meses.
- Años 2-5: Cada 6 meses.
- > 5 años: Anual (riesgo de recidiva tardía y metástasis).
- PET/TC: Solo si sospecha de recidiva o nuevas lesiones.
Novedades y perspectivas futuras (2026)
- Diagnóstico molecular como estándar: La detección de fusiones WWTR1-CAMTA1 y YAP1-TFE3 por FISH o NGS es ahora imprescindible para confirmar el diagnóstico y diferenciarlo de mimickers.
- Implicaciones pronósticas de la genética: La variante YAP1-TFE3 parece tener mejor pronóstico que la WWTR1-CAMTA1. Esto puede influir en la agresividad del tratamiento.
- Terapias dirigidas en desarrollo:
- Inhibidores de CAMTA1: En fase preclínica.
- Inhibidores de TFE3: Sin agentes específicos aún.
- Inhibidores de angiogénesis: Bevacizumab, sorafenib, sunitinib han mostrado actividad en casos aislados de enfermedad metastásica.
- Ensayos clínicos y series contemporáneas: Pazopanib y otros antiangiogénicos se han evaluado en enfermedad avanzada en diferentes cohortes retrospectivas y estudios clínicos en centros de referencia.
- Radioterapia de protones: Mayor precisión y menor toxicidad en localizaciones complejas (columna, base cráneo), especialmente en pacientes jóvenes.
Resumen para la práctica clínica
📌 Indicaciones
- ✓ Lesión lítica (a veces trabeculada 'en panal') en adulto joven, con dolor insidioso ± tumefacción.
- ✓ Multifocalidad regional (múltiples focos en un mismo hueso/miembro) con sospecha de enfermedad multicéntrica.
- ✓ Lesiones líticas en hueso axial (columna/pelvis/cráneo) donde la resección en bloque puede ser inviable.
- ✓ Duda diagnóstica con metástasis, TCG, QOA, linfoma, plasmocitoma o angiosarcoma.
- ✓ Planificación de tratamiento local (resección amplia vs radioterapia vs observación) según accesibilidad y patrón de enfermedad.
🔧 Técnica
- 🔧 Radiografía inicial + RM con contraste para extensión local.
- 🔧 RM del segmento óseo completo o extremidad completa para detectar lesiones satélite/multifocalidad.
- 🔧 TC si se necesita definir cortical/trabeculación y para planificar biopsia o resección.
- 🔧 Biopsia (core/incisional) con trayecto planificado resecable.
- 🔧 Patología experta + correlación clínico-radiológica.
- 🔧 IHC mínima: CD31, ERG, FLI1 (± factor VIII); panel de exclusión según caso.
- 🔧 Molecular imprescindible: confirmar WWTR1–CAMTA1; si negativo, buscar YAP1–TFE3.
- 🔧 Estadificación: TC de tórax + estudio sistémico según protocolo (PET/TC o alternativa).
- 🔧 Resección amplia (R0) en lesión solitaria resecable.
- 🔧 Radioterapia en localizaciones complejas (columna, base cráneo).
- 🔧 Observación vigilante en multifocal regional indolente.
⚠️ Riesgos
- ⚠️ Recidiva local (más frecuente con márgenes intralesionales o curetaje).
- ⚠️ Infradiagnóstico de angiosarcoma si no se integra clínica-imagen-patología y no se hace molecular.
- ⚠️ Sobrediagnóstico como metástasis o carcinoma si hay queratinas focales (HEE puede ser focalmente CK+).
- ⚠️ Fractura patológica o riesgo estructural en lesiones líticas extensas.
- ⚠️ Complicaciones de reconstrucción (cemento/injerto/osteosíntesis/megaprótesis) según defecto.
- ⚠️ Morbilidad neurológica/vascular en localizaciones axiales complejas.
✅ Resultados
- ✅ Curso variable: muchos casos indolentes, pero un subgrupo progresa o metastatiza.
- ✅ Control local alto con resección amplia R0 o radioterapia bien indicada.
- ✅ Metástasis posibles (pulmón/hígado/hueso) incluso tardías: requiere seguimiento prolongado.
- ✅ Multifocalidad regional no implica necesariamente mal pronóstico como la enfermedad metastásica verdadera.
- ✅ Seguimiento más estrecho los 2–3 primeros años, y luego vigilancia a largo plazo.
Referencias clave (2020–2026)
Clasificación y concepto
- WHO Classification of Tumours Editorial Board. Soft Tissue and Bone Tumours. 5th ed. Lyon: IARC; 2020. [Capítulo: Hemangioendotelioma epitelioide].
- Doyle LA, et al. Epithelioid hemangioendothelioma: an update. Surg Pathol Clin. 2022.
- Rosenbaum E, et al. The 2020 WHO classification of soft tissue tumors: what is new? Am J Surg Pathol. 2021.
Genética y diagnóstico molecular
- Antonescu CR, et al. WWTR1-CAMTA1 fusion is a consistent finding in epithelioid hemangioendothelioma. Genes Chromosomes Cancer. 2020.
- Flucke U, et al. YAP1-TFE3 epithelioid hemangioendothelioma: a clinicopathologic and molecular study. Mod Pathol. 2021.
- Shon W, et al. Molecular testing in vascular tumors: a practical guide. J Am Acad Dermatol. 2023.
Manejo y tratamiento
- Stacchiotti S, et al. Epithelioid hemangioendothelioma, an ultra-rare cancer: a consensus paper from the community of experts. ESMO Open. 2021.
- Mack LA, et al. Surgery and radiotherapy for epithelioid hemangioendothelioma of bone: a systematic review. J Surg Oncol. 2022.
- Frezza AM, et al. Systemic treatment in advanced epithelioid hemangioendothelioma: a retrospective international study. Eur J Cancer. 2023.
Imagen y diagnóstico diferencial
- Errani C, et al. Imaging features of epithelioid hemangioendothelioma of bone. Skeletal Radiol. 2020.
- Rajiah P, et al. Imaging of primary vascular tumors of bone. Radiol Clin North Am. 2022.
