Fibrosarcoma Óseo — Actualización 2026
Tumor maligno primario del hueso poco frecuente, derivado de células fibroblásticas y definido por la producción de haces entrelazados de colágeno, sin diferenciación osteogénica. Supone un desafío diagnóstico por su presentación osteolítica pura, lo que lo sitúa en el diferencial de múltiples lesiones agresivas. La última clasificación de la OMS y los avances en tratamiento multimodal han modificado su pronóstico y manejo.
En 1 minuto
Adultos 30-60 años (media ~50). Dolor y tumefacción de semanas/meses. Hasta 25% debutan con fractura patológica.
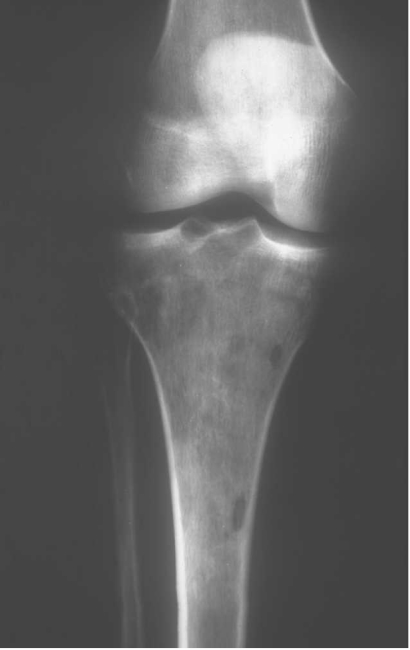
Metáfisis de huesos largos (>50% rodilla). Lesión lítica pura, agresiva (permeativa/moteada), sin matriz. Masa de partes blandas frecuente. "Secuestro óseo" sugerente.
Sarcoma de alto grado. Diagnóstico de exclusión (descartar osteogénesis tumoral). Manejo: QT neoadyuvante + cirugía con márgenes amplios ± RT.
Definición y clasificación (OMS 2020/2023)
Clasificación práctica
- Fibrosarcoma central (convencional): Origen en la cavidad medular. Es la forma más frecuente.
- Fibrosarcoma perióstico (raro): Origen en la superficie ósea, con mejor pronóstico relativo. Su existencia como entidad separada sigue en debate.
- Fibrosarcoma secundario (30-40%): Surge sobre lesión preexistente: displasia fibrosa, enfermedad de Paget, infarto óseo, post-radiación (ej., TCG irradiado), osteomielitis crónica.
Conceptos modernos (qué NO es)
- No es un osteosarcoma fibroblástico: Este último sí produce osteoide, aunque sea mínimo.
- No es un fibrohistiocitoma maligno óseo (HFM): El HFM tiene un patrón estoriforme e histiocitos pleomórficos; hoy muchos se reclasifican como sarcomas indiferenciados de alto grado.
- No es un diagnóstico "cajón de sastre": Es un diagnóstico de exclusión tras descartar otros sarcomas fusocelulares.
Epidemiología y manifestaciones clínicas
| Parámetro | Datos | Comentario práctico |
|---|---|---|
| Frecuencia | ~2-5% de los sarcomas óseos primarios | Tumor raro. La incidencia ha bajado por mejor reclasificación. |
| Edad | Amplio rango (10-80 años). Pico: 4ª-6ª década. | En <20 años es raro; pensar primero en osteosarcoma o sarcoma de Ewing. |
| Sexo | Ligero predominio masculino (1.3:1) | No es un factor determinante. |
| Localización clásica | Metáfisis de huesos largos (65%). Fémur (35%), Tibia (20%), Húmero (10%). | Región de la rodilla (fémur distal + tibia proximal) >50% de casos. |
| Presentación clínica | Dolor (85%), tumefacción (70%). Fractura patológica inicial (20-25%). | Síntomas inespecíficos de semanas a meses. La fractura patológica es una presentación clásica. |
| Formas secundarias | 30-40% de casos | Antecedente clave: displasia fibrosa, Paget, radioterapia previa (>5 años después). |
Estudios de imagen: hallazgos y protocolo
Radiografía / TC: hallazgos clave
Patrón lítico puro y agresivo: geográfico (tipo IB/IC de Lodwick) o permeativo/motado. Ausencia de esclerosis reactiva y de matriz osteoide/cartilaginosa. Bordes mal definidos. Destrucción cortical y masa de partes blandas (80%). Signo del "secuestro óseo": fragmento de cortical o esponjosa atrapado en la masa tumoral (sugerente, no patognomónico).
RM y PET/TC: rol actual
RM es obligatoria para estadificación local: evalúa extensión intraósea (edema medular), partes blandas, relación neurovascular. Señal heterogénea en T2, realce intenso y heterogéneo con gadolinio. PET/TC con 18F-FDG es estándar para estadificación sistémica (alta avidez SUVmax) y valorar respuesta a quimioterapia neoadyuvante.
| Modalidad | Hallazgos principales | Utilidad práctica |
|---|---|---|
| Radiografía | Lítica pura, agresiva, sin matriz. Posible fractura patológica. | Estudio inicial. Sospecha de malignidad. Guía para solicitar RM. |
| TC (sin contraste) | Detalle de destrucción cortical, "secuestro óseo", ausencia de calcificaciones. | Planificación biopsia (vía segura). Evaluar fractura. |
| RM (con contraste) | Extensión intra/extraósea, edema reactivo, relación anatómica. | Estadificación local obligatoria. Planificación quirúrgica. |
| PET/TC | Alta avidez metabólica (SUVmax elevado). Detección de metástasis. | Estadificación sistémica. Valorar respuesta a QT. |
Histopatología, gradación y biomarcadores
Hallazgos microscópicos clásicos
- Patrón "en espiga de trigo" (herringbone): Haces entrelazados de células fusiformes.
- Células: Fibroblastos atípicos, fusiformes, con grados variables de pleomorfismo, mitosis y necrosis.
- Matriz: Cantidad variable de colágeno (hialinizado en bajos grados).
- Criterio clave: Ausencia de osteoide/hueso tumoral producido directamente por las células neoplásicas.
Inmunohistoquímica (IHC) esencial
- Vimentina (+): Marcador mesenquimal.
- Actina músculo liso (±): Focal positivo en algunos casos.
- SATB2, Osteocalcina, Osterix (-): Marcadores osteoblásticos deben ser negativos para excluir osteosarcoma.
- CD34, S100, SOX10, EMA (-): Para excluir otros sarcomas fusocelulares.
- Ki-67: Alto índice proliferativo en grados altos.
Gradación (sistema FNCLCC / OMS)
- Grado 1 (Bien diferenciado): Celularidad baja, atipia mínima, mitosis escasas, colágeno abundante. Difícil de distinguir de lesiones fibrosas benignas (fibroma desmoplástico).
- Grado 2 (Moderadamente diferenciado): Celularidad y atipia moderadas. Patrón clásico.
- Grado 3 (Pobremente diferenciado): Alta celularidad, atipia marcada, mitosis frecuentes, necrosis. Comportamiento más agresivo.
>90% de los fibrosarcomas primarios son de alto grado (G2/G3). Los de bajo grado suelen ser secundarios (ej., de displasia fibrosa).
Algoritmo diagnóstico y de manejo inicial
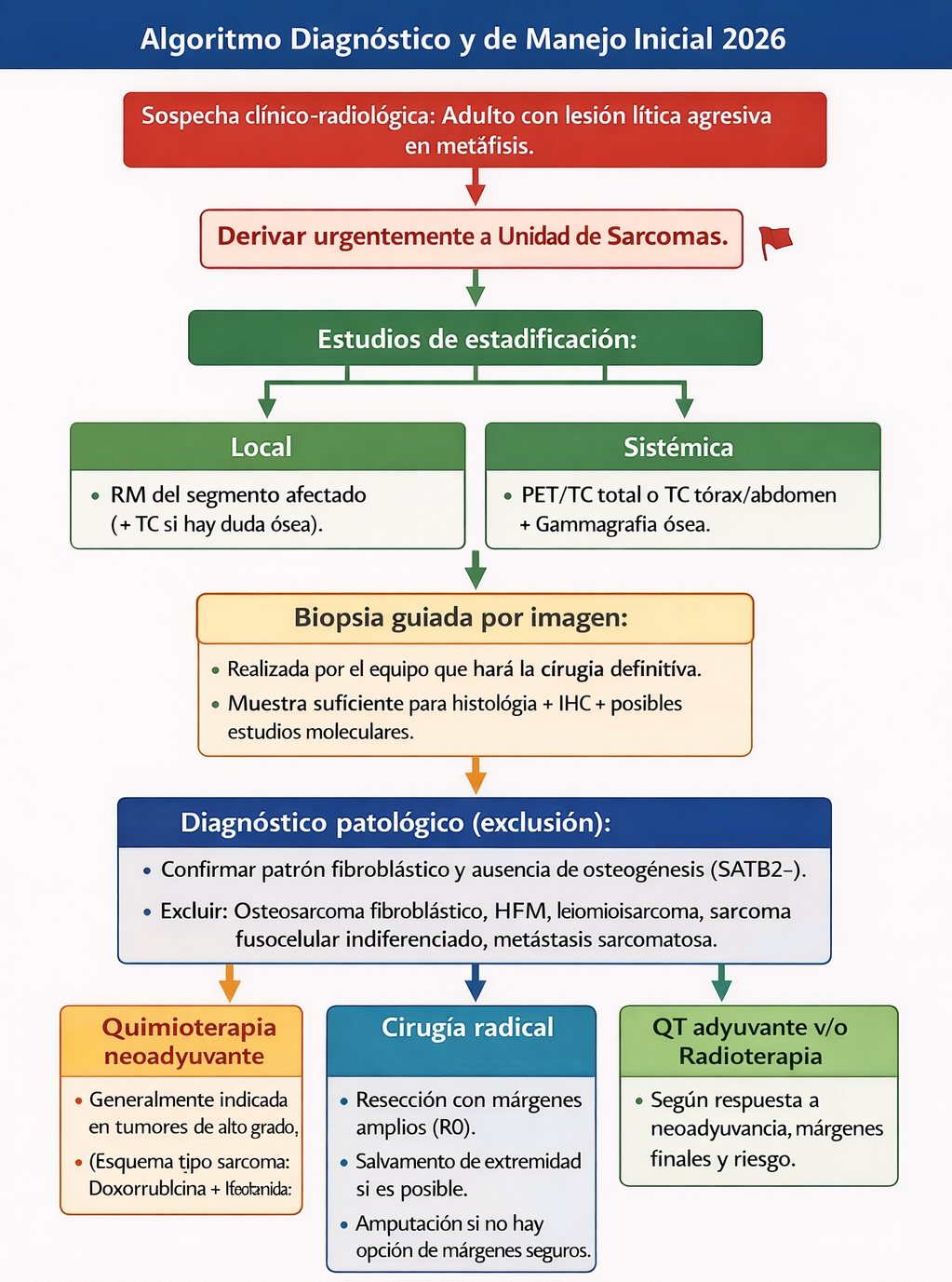
- Sospecha clínico-radiológica: Adulto con lesión lítica agresiva en metáfisis. Derivar urgentemente a Unidad de Sarcomas.
- Estudios de estadificación:
- Local: RM del segmento afectado (+ TC si hay duda ósea).
- Sistémica: PET/TC total o TC tórax/abdomen + Gammagrafía ósea.
- Biopsia guiada por imagen:
- Realizada por el equipo que hará la cirugía definitiva.
- Muestra suficiente para histología + IHC + posibles estudios moleculares.
- Diagnóstico patológico (exclusión):
- Confirmar patrón fibroblástico y ausencia de osteogénesis (SATB2-).
- Excluir: Osteosarcoma fibroblástico, HFM, leiomiosarcoma, sarcoma fusocelular indiferenciado, metástasis sarcomatosa.
- Decisión multidisciplinar (Comité de Tumores):
- Quimioterapia neoadyuvante: Generalmente indicada en tumores de alto grado (esquema tipo sarcoma: Doxorrubicina + Ifosfamida +/- otros).
- Cirugía radical: Resección con márgenes amplios (R0). Salvamento de extremidad si es posible. Amputación si no hay opción de márgenes seguros.
- QT adyuvante y/o Radioterapia: Según respuesta a neoadyuvancia, márgenes finales y riesgo.
Diagnóstico diferencial crítico
Diferencial radiológico (lesiones líticas agresivas)
- Osteosarcoma (fibroblástico o telangiectásico): El gran mimicker. Edad más joven, pero puede ser idéntico en imagen. Requiere exclusión histológica.
- Metástasis ósea (carcinoma renal, tiroides): Más común en >40 años, puede ser lítica pura. Buscar tumor primario.
- Mieloma múltiple / Plasmocitoma solitario: Edad avanzada, lesiones "perforadas", proteínas en orina.
- Linfoma óseo primario: Lítico, a menudo con gran masa de partes blandas desproporcionada a la destrucción ósea.
- Tumor de células gigantes (agresivo): Subarticular, en esqueleto maduro. Bordes no escleróticos pero menos permeativos.
- Infección agresiva (osteomielitis): Clínica febril, signos inflamatorios.
Diferencial histopatológico principal
- Osteosarcoma fibroblástico: La línea es fina. Clave IHC: SATB2+ (marcador osteoblástico nuclear). Buscar focos de osteoide tumoral.
- Fibrohistiocitoma maligno óseo (ahora "sarcoma indiferenciado de alto grado"): Patrón estoriforme, células histiocíticas pleomórficas.
- Leiomiosarcoma óseo (raro): Células fusiformes con citoplasma eosinófilo. Clave IHC: actina de músculo liso (SMA) ++, desmina +, h-caldesmona +.
- Fibroma desmoplástico (benigno): Baja celularidad, sin atipia, mitosis raras. Puede ser localmente agresivo pero no metastatiza.
- Schwannoma maligno/sarcoma neurogénico: Relación con nervio. Clave IHC: S100+ (focal), SOX10+.
Tratamiento multimodal — Estándar
1. Quimioterapia Neoadyuvante (Inducción)
Indicada en la mayoría de fibrosarcomas de alto grado. Objetivos: tratar micrometástasis, reducir volumen tumoral (para facilitar cirugía conservadora), evaluar respuesta histológica.
- Esquemas habituales: Basados en regímenes para sarcoma de partes blandas de alto grado:
- Doxorrubicina + Ifosfamida (AI).
- Gemcitabina + Docetaxel (en segundas líneas o subtipos).
- Participación en ensayos clínicos con nuevas combinaciones.
- Evaluación de respuesta: Con RM y/o PET/TC post-quimioterapia.
2. Cirugía Radical
Objetivo: resección completa con márgenes amplios (R0). Es el pilar del tratamiento local.
- Salvamento de extremidad: Estándar actual. Implica resección en bloque del tumor + reconstrucción (prótesis modular masiva, aloinjerto, combinación).
- Amputación: Indicada si no es posible obtener márgenes oncológicos seguros con cirugía conservadora (compromiso neurovascular masivo, infección, extensión muy distal).
- Cirugía de metástasis: En casos seleccionados de enfermedad oligometastásica (pulmón), la metastasectomía puede mejorar la supervivencia.
3. Quimioterapia Adyuvante
Se recomienda completar el tratamiento quimioterápico (generalmente los mismos fármacos) tras la cirugía, especialmente si hubo buena respuesta a la neoadyuvancia o en tumores de alto riesgo (necrosis <90%, márgenes cercanos).
4. Radioterapia (RT)
Papel adyuvante para mejorar el control local en casos de:
- Márgenes quirúrgicos positivos (R1) o muy cercanos donde la re-resección no es posible.
- Respuesta patológica pobre a QT neoadyuvante.
- Tumores irresecables de entrada (RT definitiva +/- QT).
- Tratamiento paliativo de metástasis dolorosas.
Técnica: IMRT/VMAT/Protones para precisión y menor toxicidad.
Pronóstico y seguimiento a largo plazo
| Factor pronóstico | Pronóstico favorable | Pronóstico desfavorable |
|---|---|---|
| Grado histológico | Grado 1 (bajo) | Grado 3 (alto) |
| Tamaño tumoral | < 8 cm | > 8 cm |
| Enfermedad metastásica | Ausente al diagnóstico (M0) | Presente al diagnóstico (M1) |
| Resección quirúrgica | Margen amplio (R0) | Margen contaminado (R1/R2) |
| Respuesta a QT neoadyuv. | Necrosis tumoral >90% (buena respuesta) | Necrosis tumoral <90% (mala respuesta) |
| Localización | Extremidades (resecable) | Axial (columna, pelvis) |
Supervivencia (datos de series modernas con tratamiento multimodal)
- Supervivencia global a 5 años: ~60-70% para enfermedad localizada (M0) de alto grado tratada con QT + cirugía.
- Supervivencia a 5 años para enfermedad metastásica (M1): <20%.< /li>
- Fibrosarcoma secundario: Suele tener peor pronóstico debido al retraso en el diagnóstico.
Protocolo de seguimiento recomendado (NCCN/ESMO 2025)
- Primeros 2-3 años (alto riesgo de recidiva): Historia, examen físico, Rx/RM local y TC tórax cada 3-4 meses.
- Años 3-5: Cada 6 meses.
- > 5 años: Anualmente (riesgo bajo pero no nulo de recidiva tardía).
- PET/TC: Solo si sospecha de recidiva o nueva sintomatología.
Vigilar: Dolor local nuevo, masa, síntomas constitucionales, disnea (metástasis pulmonar).
Novedades y perspectivas futuras
Avances diagnósticos
- Perfil molecular y clasificación: Se buscan firmas genéticas que distingan fibrosarcoma óseo "puro" de otros sarcomas fusocelulares y guíen el tratamiento.
- Biopsia líquida: En investigación para monitorizar enfermedad mínima residual y detectar recidivas.
- IA en imagen: Algoritmos para diferenciar lesiones líticas agresivas en radiografías/TC.
Avances terapéuticos
- Inmunoterapia: Ensayos con inhibidores de puntos de control (pembrolizumab, nivolumab) en sarcomas, con respuestas variables. Se buscan biomarcadores predictivos.
- Terapias dirigidas: En fibrosarcomas con alteraciones específicas (ej., reordenamientos NTRK, mutaciones en genes de la vía RAS-MAPK).
- QT más precisa: Estratificación del riesgo y desintensificación de QT en tumores de bajo riesgo con buena respuesta.
- Radioterapia de protones: Mayor uso en localizaciones complejas (columna, base de cráneo) para reducir toxicidad.
Referencias clave (2020–2026)
Clasificación y patología
- WHO Classification of Tumours Editorial Board. Soft Tissue and Bone Tumours. 5th ed. Lyon: IARC; 2020. [Clasificación de referencia].
- Lopez G, et al. Molecular profiling of primary bone fibrosarcoma reveals key pathways and potential therapeutic targets. Mod Pathol. 2023.
- Gronchi A, et al. Soft tissue and visceral sarcomas: ESMO-EURACAN-GENTURIS Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021 (actualización 2024). [Incluye consideraciones para sarcomas fusocelulares].
Manejo y tratamiento
- NCCN Guidelines. Bone Cancer (Version 3.2025). National Comprehensive Cancer Network. [Guía de práctica clínica actualizada].
- ESMO Guidelines. Bone sarcomas: clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021 (y actualizaciones).
- von Mehren M, et al. NCCN Guidelines Insights: Soft Tissue Sarcoma, Version 2.2024. J Natl Compr Canc Netw. 2024. [Tratamiento sistémico aplicable].
Imagen y respuesta
- European Society of Musculoskeletal Radiology (ESSR). Guidelines for the diagnostic management of incidental solitary bone lesions on CT and MRI in adults. Skeletal Radiol. 2022.
- Meyer HJ, et al. The Role of PET/CT in Bone Sarcomas. Diagnostics (Basel). 2023.
Investigación y futuro
- Tawbi HA, et al. Pembrolizumab in advanced soft-tissue sarcoma and bone sarcoma (SARC028): a multicentre, two-cohort, single-arm, open-label, phase 2 trial. Lancet Oncol. 2022 (y estudios posteriores).
- ClinicalTrials.gov. Ensayos en curso para "bone fibrosarcoma" y "undifferentiated pleomorphic sarcoma of bone". [Recurso para opciones de investigación].
Resumen para la práctica clínica
📌 Indicaciones
- ✓ Lesión lítica agresiva metafisaria en adulto (sospecha de sarcoma).
- ✓ Confirmación histológica de fibrosarcoma tras biopsia y exclusión de osteosarcoma.
- ✓ Planificación de tratamiento multimodal (QT neoadyuvante + cirugía ± RT).
- ✓ Estadificación local y sistémica para determinar resecabilidad y pronóstico.
🔧 Técnica
- 🔧 Radiografía y RM para caracterización y extensión local.
- 🔧 PET/TC para estadificación sistémica y evaluación de respuesta.
- 🔧 Biopsia guiada por imagen, con IHC (SATB2 negativo) y gradación.
- 🔧 Quimioterapia neoadyuvante basada en antraciclinas/ifosfamida.
- 🔧 Cirugía con márgenes amplios (R0) y reconstrucción cuando sea posible.
- 🔧 Radioterapia adyuvante en casos de alto riesgo local (márgenes R1).
⚠️ Riesgos
- ⚠️ Recidiva local (mayor si márgenes inadecuados o mala respuesta a QT).
- ⚠️ Metástasis a distancia (principalmente pulmonares), especialmente en alto grado.
- ⚠️ Toxicidad de quimioterapia (mielosupresión, cardiotoxicidad, nefrotoxicidad).
- ⚠️ Complicaciones quirúrgicas (infección, fallo de reconstrucción, daño neurovascular).
✅ Resultados
- ✅ Supervivencia global a 5 años: 60-70% para enfermedad localizada tratada adecuadamente.
- ✅ Control local superior con cirugía R0 y buena respuesta a QT neoadyuvante.
- ✅ Las recurrencias, cuando ocurren, requieren rescate quirúrgico y/o radioterapia.
- ✅ Seguimiento estrecho los primeros 2-3 años para detectar recidiva/metástasis precoz.
