Última revisión:
Sistemas de Estadificación Quirúrgica
La estadificación de tumores musculoesqueléticos es un proceso multidimensional que integra datos histológicos, radiológicos y clínicos para predecir el comportamiento biológico, planificar el tratamiento quirúrgico y determinar el pronóstico. Los sistemas actuales (AJCC 8ª edición, MSTS/Enneking) han evolucionado desde los modelos clásicos, incorporando nuevos factores pronósticos y validación en estudios multicéntricos. Esta guía compara sistemáticamente ambos enfoques y proporciona algoritmos para su aplicación práctica en la toma de decisiones multidisciplinar.
1) Introducción y principios de estadificación
Objetivos de la estadificación oncológica:
- • Predecir pronóstico (supervivencia, riesgo de metástasis).
- • Guiar selección terapéutica (cirugía conservadora vs. radical, quimioterapia neoadyuvante/adyuvante).
- • Establecer grupos homogéneos para investigación clínica y comparación de resultados.
- • Facilitar comunicación entre especialistas (cirujanos, oncólogos, patólogos, radiólogos).
Componentes fundamentales de cualquier sistema
- • G (Grado histológico): diferenciación celular, actividad mitótica, necrosis.
- • T (Tumor primario): tamaño, extensión local, relación con barreras anatómicas.
- • N (Nódulos linfáticos): metástasis regionales (menos frecuente en sarcomas).
- • M (Metástasis): enfermedad a distancia (pulmón > hueso > otros).
2) Principios fundamentales de estadificación
Grado histológico (G) — definiciones actuales
| Grado | Definición histológica | Criterios prácticos (FNCLCC para partes blandas) |
|---|---|---|
| G1 (Bajo) | Bien diferenciado, escasas mitosis, necrosis < 50% | Puntuación total 2-3 (diferenciación 1 + mitosis 1-2 + necrosis 0) |
| G2 (Intermedio) | Moderadamente diferenciado | Puntuación total 4-5 |
| G3 (Alto) | Pobremente diferenciado/indiferenciado, mitosis frecuentes, necrosis ≥ 50% | Puntuación total 6-8 |
| G4 (Siempre alto) | Sarcoma de Ewing, osteosarcoma convencional, tumor desmoide (en hueso) | Definido por tipo histológico específico |
Nota: El sistema FNCLCC es estándar para sarcomas de partes blandas; para hueso se usan criterios específicos por tumor.
Importancia del tamaño tumoral (T)
- • Puntos de corte: tradicionalmente 5 cm (8 cm para tumores óseos en AJCC).
- • Medición: diámetro mayor en RM/TC (idealmente con contraste si aplica).
- • Significado pronóstico: mayor tamaño → mayor riesgo metastásico.
- • Localización: superficial vs profunda a fascia (clave en partes blandas).
Factores pronósticos emergentes (opcional)
- • Respuesta a quimioterapia neoadyuvante (necrosis tumoral %).
- • Biología molecular: translocaciones, mutaciones (MDM2, CDK4), índice Ki-67.
- • Imagen avanzada: PET/SUVmax, perfusión por RM, radiómica.
3) Compartimentos quirúrgicos (concepto Enneking)
Concepto clave de Enneking (1980): Los tejidos musculoesqueléticos están organizados en compartimentos anatómicos definidos por barreras naturales (hueso cortical, fascia, cápsula articular, periostio) que restringen la diseminación tumoral.
Compartimentos quirúrgicos (clasificación MSTS)
| Tipo | Definición | Ejemplos |
|---|---|---|
| Intracompartimental (T1) | Confinado dentro de barreras naturales |
|
| Extracompartimental (T2) | Extensión más allá de barreras originales |
|
Importancia quirúrgica del concepto compartimental
- • Resección intracompartimental: puede permitir márgenes más conservadores.
- • Resección extracompartimental: requiere márgenes más amplios, posible sacrificio de estructuras.
- • Planificación preoperatoria: RM/TC esencial para definir relación con barreras.
- • Implicaciones pronósticas: T2 asociado con mayor riesgo de recidiva local.
4) Sistemas de estadificación principales
Sistemas principales en uso actual
| Sistema | Aplicación principal | Ventajas | Limitaciones |
|---|---|---|---|
| AJCC 8ª edición (2017) | Tumores óseos y de partes blandas | Universalmente aceptado, actualizado regularmente, integra datos moleculares | Complejidad, requiere patología especializada |
| MSTS (Enneking) | Planificación quirúrgica | Simple, orientado al cirujano, define márgenes | Menos detalle pronóstico, menos usado en estudios |
| FNCLCC | Sarcomas de partes blandas | Reproducible, validado pronósticamente | No aplica a tumores óseos |
Recomendación práctica: Usar AJCC para estadificación pronóstica y comunicación entre centros, y MSTS para planificación quirúrgica específica. Ambos sistemas son complementarios.
5) AJCC 8ª edición (tumores óseos)
AJCC 8ª edición (2017) — Tumores óseos malignos
| Variable | Categorías | Definición |
|---|---|---|
| T (Tumor) | T1, T2, T3 | T1: ≤ 8 cm T2: > 8 cm T3: tumor discontinuo en mismo hueso |
| N (Nódulos) | N0, N1 | N0: no ganglios regionales N1: metástasis en ganglios (raro, peor pronóstico) |
| M (Metástasis) | M0, M1a, M1b | M0: sin metástasis M1a: pulmonar M1b: otras (ósea, visceral) |
| G (Grado) | G1, G2, G3 | Basado en tipo histológico específico: G1: condrosarcoma grado I, cordoma convencional G2: osteosarcoma de bajo grado, condrosarcoma grado II G3: osteosarcoma convencional, sarcoma de Ewing, condrosarcoma grado III |
Estadios AJCC para tumores óseos
| Estadio | Grado | T | N | M | Ejemplos típicos |
|---|---|---|---|---|---|
| IA | G1, GX | T1 | N0 | M0 | Condrosarcoma grado I ≤8 cm |
| IB | G1, GX | T2, T3 | N0 | M0 | Condrosarcoma grado I >8 cm |
| IIA | G2, G3 | T1 | N0 | M0 | Osteosarcoma convencional ≤8 cm |
| IIB | G2, G3 | T2 | N0 | M0 | Osteosarcoma convencional >8 cm |
| III | G2, G3 | T3 | N0 | M0 | Tumores discontinuos mismo hueso |
| IVA | Cualquiera | Cualquiera | N0 | M1a | Metástasis solo pulmonares |
| IVB | Cualquiera | Cualquiera | N1 o cualquiera | M1b | Metástasis múltiples o ganglionares |
Cambios importantes AJCC 8ª vs ediciones anteriores:
- • Nuevos puntos de corte: 8 cm en lugar de 5 cm para tumores óseos.
- • Subclasificación M1: distinción pronóstica entre metástasis pulmonares y otras.
- • Incorporación de datos moleculares: especialmente en tumores de bajo grado.
6) AJCC 8ª edición (partes blandas)
AJCC 8ª edición — Sarcomas de partes blandas (extremidades y tronco)
| Variable | Categorías | Definición |
|---|---|---|
| T (Tumor) | T1, T2, T3, T4 | T1: ≤ 5 cm (T1a superficial, T1b profundo) T2: > 5 y ≤ 10 cm (T2a/b) T3: > 10 y ≤ 15 cm T4: > 15 cm |
| N (Nódulos) | N0, N1 | N0: no ganglios regionales N1: metástasis ganglionares (peor pronóstico que M1 en algunos) |
| M (Metástasis) | M0, M1 | M0: sin metástasis M1: metástasis a distancia |
| G (Grado FNCLCC) | G1, G2, G3 | G1: bien diferenciado (puntuación 2-3) G2: moderado (puntuación 4-5) G3: pobre/indiferenciado (puntuación 6-8) |
Estadios AJCC para partes blandas
| Estadio | Grado | T | N | M | 5‑year survival* |
|---|---|---|---|---|---|
| IA | G1 | T1 | N0 | M0 | 90‑95% |
| IB | G1 | T2, T3, T4 | N0 | M0 | 85‑90% |
| II | G2 | T1 | N0 | M0 | 75‑80% |
| IIIA | G2 | T2 | N0 | M0 | 65‑70% |
| IIIB | G3 | T1, T2 | N0 | M0 | 50‑60% |
| IVA | Cualquiera | Cualquiera | N1 | M0 | 25‑35% |
| IVB | Cualquiera | Cualquiera | Cualquiera | M1 | 10‑20% |
*Supervivencia aproximada según series modernas con tratamiento multimodal.
Consideraciones especiales para retroperitoneo:
- • Puntos de corte diferentes: T1 ≤ 5 cm, T2 5‑10 cm, T3 10‑15 cm, T4 > 15 cm.
- • Peor pronóstico: estadio por estadio vs extremidades.
- • Importancia de márgenes R0: factor pronóstico independiente crítico.
7) Sistema MSTS (Enneking)
Filosofía del sistema MSTS (Musculoskeletal Tumor Society): Sistema quirúrgico diseñado por Enneking et al. (1980) para guiar la extensión de resección basado en comportamiento biológico (grado) y anatomía local (compartimentalización).
Componentes del sistema MSTS
| Componente | Categorías | Definición | Implicación quirúrgica |
|---|---|---|---|
| G (Grado) | G0, G1, G2 | G0: benigno G1: bajo grado G2: alto grado |
Define agresividad biológica |
| T (Sitio) | T0, T1, T2 | T0: encapsulado (benignos) T1: intracompartimental T2: extracompartimental |
Define márgenes necesarios |
| M (Metástasis) | M0, M1 | M0: sin metástasis M1: con metástasis |
Cambia objetivos terapéuticos |
Estadios quirúrgicos MSTS (malignos)
| Estadio | Grado | Sitio (T) | Metástasis | Cirugía recomendada |
|---|---|---|---|---|
| IA | G1 (bajo) | T1 (intra) | M0 | Márgenes amplios (puede ser conservadora) |
| IB | G1 (bajo) | T2 (extra) | M0 | Márgenes amplios (posible amputación) |
| IIA | G2 (alto) | T1 (intra) | M0 | Márgenes radicales (conservadora posible con QT) |
| IIB | G2 (alto) | T2 (extra) | M0 | Márgenes radicales (frecuente amputación) |
| III | Cualquiera | Cualquiera | M1 | Paliativa (o citorreductiva selectiva) |
Estadios para tumores benignos (MSTS)
| Estadio | Comportamiento | Ejemplos | Tratamiento |
|---|---|---|---|
| 1 (Latente) | Asintomático, no crece, puede regresar | Quiste óseo no osificante, osteocondroma solitario | Observación |
| 2 (Activo) | Sintomático, crece lentamente, expansivo | Tumor de células gigantes, osteoblastoma | Curetaje + adjuvantes |
| 3 (Agresivo) | Crecimiento rápido, destructivo local | Osteoblastoma agresivo, GCT recurrente | Resección marginal/amplia |
8) Comparativa entre sistemas
Comparación directa: AJCC vs MSTS
| Aspecto | AJCC (8ª ed.) | MSTS (Enneking) | Recomendación práctica |
|---|---|---|---|
| Propósito principal | Pronóstico, estadificación universal | Planificación quirúrgica | Usar ambos: AJCC para pronóstico, MSTS para cirugía |
| Grado (G) | 3‑4 niveles (G1‑G3/G4) | 2 niveles (G1‑G2) + benignos | AJCC más detallado para estudios |
| Tamaño (T) | Múltiples puntos corte (5,8,10,15 cm) | Conceptual: intra vs extracompartimental | AJCC más objetivo para pronóstico |
| Metástasis (M) | Subclasificada (M1a/b) | Presente/ausente | AJCC más informativo para metástasis |
| Facilidad de uso | Complejo, requiere especialización | Simple, intuitivo para cirujanos | MSTS ideal para decisiones intraoperatorias |
| Validación pronóstica | Amplia, estudios multicéntricos | Limitada, más experiencia clínica | AJCC preferible para investigación |
| Integración con QT/RT | Óptima (diseñado para multimodalidad) | Limitada (enfocado en cirugía) | AJCC para decisiones oncología médica |
Correlación aproximada entre sistemas:
- • AJCC I/II ≈ MSTS IA/IB (tumores de bajo grado)
- • AJCC III ≈ MSTS IIA/IIB (tumores de alto grado sin metástasis)
- • AJCC IV ≈ MSTS III (enfermedad metastásica)
- • Nota: La correlación no es perfecta debido a diferencias en definiciones de T y G.
9) Aplicación práctica clínica
Flujo de trabajo práctico para estadificación
- 1 Evaluación clínica inicial: síntomas, tiempo de evolución, examen físico.
- 2 Estudios de imagen:
- RX: evaluación ósea básica.
- RM local: tamaño preciso, relación con compartimentos, neurovascular.
- TC tórax/abdomen: estadificación a distancia (mínimo TC tórax).
- PET/TC opcional: en casos seleccionados (alto grado, sospecha metastásica).
- 3 Biopsia: guiada por imagen, trayecto resecable, muestra suficiente para:
- Diagnóstico histológico específico.
- Grado (FNCLCC para partes blandas, sistema específico para hueso).
- Estudios moleculares si indicado (MDM2, SYT‑SSX, etc.).
- 4 Asignación de estadio:
- AJCC: registrar T, N, M, G y estadio grupal.
- MSTS: determinar grado y compartimentalización.
- 5 Reunión multidisciplinaria: consenso sobre tratamiento basado en estadio.
Errores frecuentes en estadificación (y cómo evitarlos)
| Error | Consecuencia | Solución |
|---|---|---|
| Medición incorrecta de T | Sobrestadificación o infraestadificación | Usar RM con contraste, medir diámetro mayor en corte axial |
| Confusión en grado histológico | Tratamiento inadecuado (QT innecesaria u omitida) | Revisión por patólogo especializado, usar sistemas estandarizados |
| No evaluar adecuadamente M | Cirugía radical cuando hay metástasis | TC tórax obligatorio, considerar PET en alto riesgo |
| Ignorar compartimentalización | Márgenes inadecuados, recidiva local | Analizar relación con fascia, hueso cortical, espacios en RM |
| No considerar profundidad | Infraestadificación en partes blandas | Especificar siempre superficial vs. profundo a fascia |
Checklist pre‑estadificación:
- ☑ RM local con contraste disponible (medidas precisas).
- ☑ TC tórax (abdomen/pelvis si retroperitoneo o histología específica).
- ☑ Informe de patología con diagnóstico específico y grado.
- ☑ Estudios moleculares completados si indicados.
- ☑ Imágenes revisadas en sesión multidisciplinaria.
10) Algoritmo de toma de decisiones
Algoritmo integrado de estadificación y decisión terapéutica
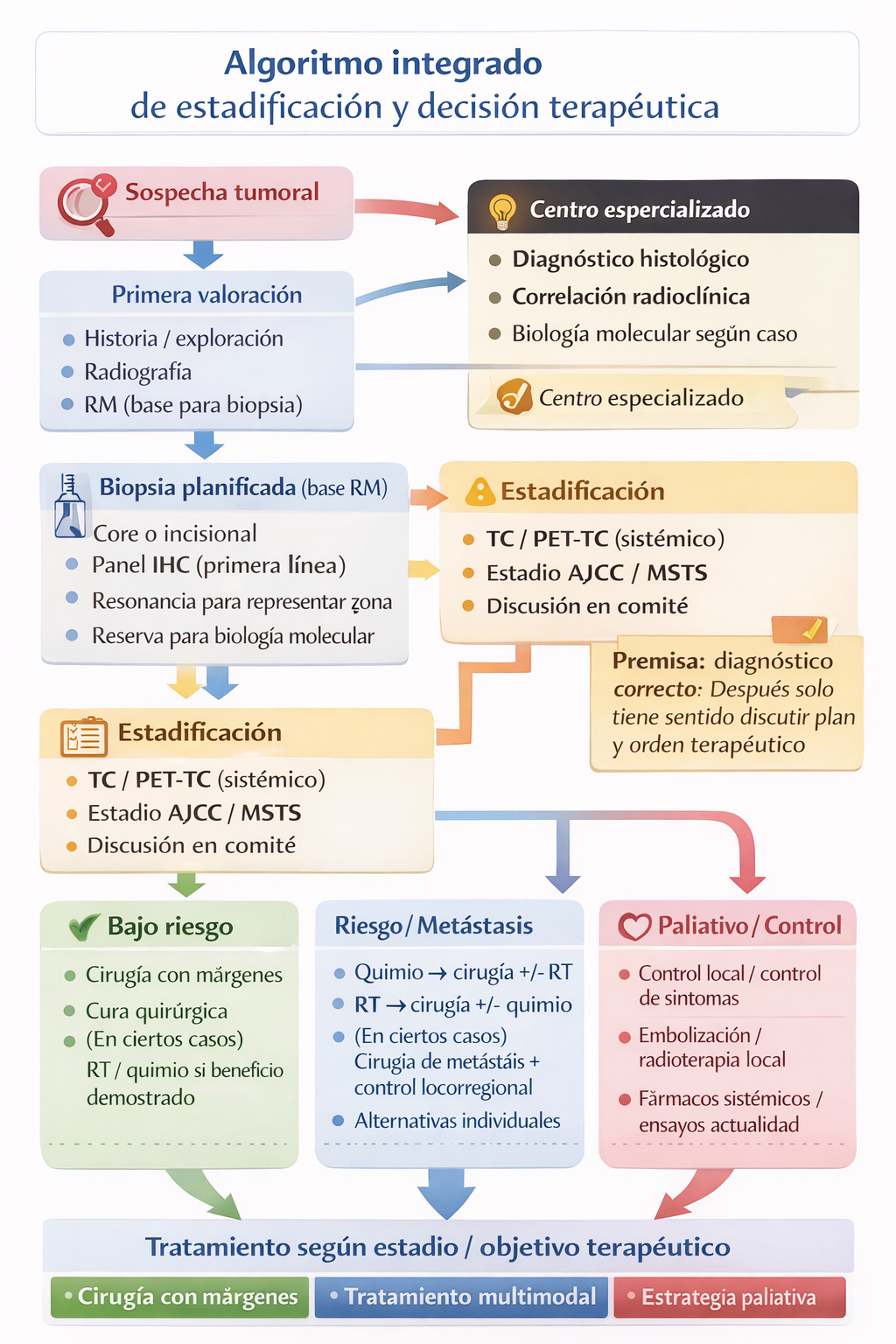
Ver algoritmo en texto (fallback)
Caracterizar tamaño, relación con estructuras, compartimentalización
• Biopsia guiada → diagnóstico + grado
• TC tórax (abdomen si retroperitoneo)
• RM local detallada (compartimentos)
• AJCC: T, N, M, G → estadio I‑IV
• MSTS: Grado (G1/G2) + sitio (T1/T2) + M
• Cirugía con márgenes amplios (R0)
• QT no rutinaria (excepto histologías específicas)
• Pronóstico favorable
• QT neoadyuvante considerada
• Cirugía radical (márgenes amplios/radicales)
• Posible QT adyuvante
• RT en márgenes comprometidos
• Tratamiento sistémico primario
• Cirugía citorreductiva selectiva
• RT paliativa
• Cuidados de soporte
5) Seguimiento según riesgo
- • Estadios I: RM local + TC tórax 6‑12 meses
- • Estadios II‑III: seguimiento estrecho (3‑6 meses primeros 2 años)
- • Estadio IV: según respuesta a tratamiento sistémico
Variables de decisión clave en comité multidisciplinario:
- • Edad y comorbilidades (tolerancia a tratamientos agresivos).
- • Localización anatómica específica (resecabilidad, morbilidad esperada).
- • Respuesta a QT neoadyuvante (si se administra).
- • Preferencias del paciente (calidad de vida vs. extensión de tratamiento).
- • Disponibilidad de técnicas reconstructivas avanzadas.
Resumen para la práctica clínica
Indicaciones
- ✓ Evaluación preoperatoria de tumores musculoesqueléticos primarios.
- ✓ Planificación de extensión de resección quirúrgica (márgenes).
- ✓ Selección de pacientes para quimioterapia neoadyuvante/adyuvante.
- ✓ Estimación pronóstica y consejo al paciente.
- ✓ Estratificación para estudios clínicos y registro de resultados.
Técnica
- 🔧 Estadificación imagenológica completa: RM local, TC tórax (mínimo).
- 🔧 Biopsia guiada por imagen con trayecto resecable.
- 🔧 Evaluación histopatológica por especialista con gradación estandarizada.
- 🔧 Asignación dual de estadio: AJCC (pronóstico) + MSTS (quirúrgico).
- 🔧 Decisión en comité multidisciplinario tumoral.
Riesgos
- ⚠️ Sobrestadificación (tratamiento excesivo, morbilidad innecesaria).
- ⚠️ Infraestadificación (tratamiento insuficiente, mayor riesgo recidiva/metástasis).
- ⚠️ Error en determinación de márgenes quirúrgicos necesarios.
- ⚠️ Omisión de estudios de extensión (metástasis no detectadas).
- ⚠️ Interpretación errónea de grado histológico.
Resultados
- ✅ Estadio preciso que guía tratamiento óptimo multimodal.
- ✅ Comunicación estandarizada entre especialistas y centros.
- ✅ Predicción pronóstica basada en evidencia.
- ✅ Base para seguimiento personalizado según riesgo.
- ✅ Datos homogéneos para evaluación de resultados e investigación.
Bibliografía actualizada (2015‑2024)
Amin MB, Edge SB, et al. Springer, 2017.
5th ed. IARC, 2020.
A system for the surgical staging of musculoskeletal sarcoma. Clin Orthop Relat Res. 1980;153:106‑120.
Soft tissue and visceral sarcomas: ESMO‑EURACAN‑GENTURIS Clinical Practice Guidelines. Ann Oncol. 2021;32(11):1348‑1365.
Update on survival in osteosarcoma. Orthop Clin North Am. 2016;47(1):283‑292.
Postoperative nomogram for 12‑year sarcoma‑specific death. J Clin Oncol. 2002;20(3):791‑796.
Soft tissue sarcoma nomograms and their incorporation into practice. Cancer. 2017;123(15):2802‑2820.
Soft Tissue Sarcoma, Version 2.2018, NCCN Guidelines. J Natl Compr Canc Netw. 2018;16(5):536‑563.
The 2020 WHO Classification of Bone Tumours: What's new? Pathologica. 2021;113(2):70‑84.
Estadificación de tumores musculoesqueléticos
AJCC 8ª ed. · MSTS (Enneking) · Compartimentos · Algoritmos
