Última revisión:
Control a largo plazo
El seguimiento a largo plazo de los pacientes tratados por un tumor óseo o de partes blandas es un componente fundamental
del manejo oncológico. El objetivo no es solo detectar recidivas locales o metástasis en fases precoces, sino también
monitorizar las complicaciones tardías del tratamiento (toxicidades de quimioterapia, radioterapia, problemas funcionales
asociados a la reconstrucción quirúrgica) y garantizar la reintegración funcional y psicosocial del paciente.
El sistema de control debe individualizarse en función del histotipo tumoral, la edad,
la localización, el tratamiento recibido (cirugía, quimioterapia, radioterapia)
y el riesgo de recidiva. Para considerar a un paciente “curado” se propone estar libre de enfermedad
durante más de 10 años (no solo 5), especialmente en tumores con potencial de recidiva tardía como el condrosarcoma,
el tumor fibroso solitario o el sarcoma fibromixoide de bajo grado.
1) Principios generales
El seguimiento a largo plazo debe ser individualizado. Los factores que influyen en la frecuencia y el tipo de controles incluyen:
el histotipo tumoral (algunos tumores recidivan tardíamente, como el condrosarcoma, el tumor fibroso solitario
o el sarcoma fibromixoide de bajo grado), el grado histológico, la respuesta a la quimioterapia
(en tumores quimiosensibles), la calidad de los márgenes quirúrgicos, la localización
y el tratamiento adyuvante recibido.
Es esencial mantener una comunicación fluida con el paciente, explicándole la importancia del seguimiento, los signos de alarma
que debe vigilar y el horizonte temporal esperado (hasta 10 años o más en tumores de alto riesgo). Un seguimiento estructurado
mejora la detección precoz de recidivas y metástasis, optimiza el manejo de las complicaciones y contribuye a la reintegración
funcional y psicosocial.
2) Cronograma orientativo en tumores malignos
El cronograma que se presenta a continuación es orientativo y debe adaptarse al riesgo individual. Los controles incluyen exploración clínica, radiografía de la localización primaria y radiografía de tórax (o TC de tórax según el riesgo y las guías locales). En los primeros años la frecuencia es mayor; después se espacia progresivamente si no hay evidencia de enfermedad.
| Periodo postratamiento | Frecuencia recomendada | Observaciones |
|---|---|---|
| 0–2 años | Cada 2–3 meses | Mayor riesgo de recidiva local y metástasis. |
| 3º–4º año | Cada 4–5 meses | Riesgo intermedio; se espacian controles. |
| 5º año | Semestrales | Periodo de transición hacia controles anuales. |
| 5º–10º año | Anuales | Vigilancia prolongada por recidivas tardías (condrosarcoma, SFT, LGFMS). |
Idea práctica: el seguimiento debe adaptarse al riesgo (tipo tumoral, respuesta, márgenes, localización y situación clínica). Los pacientes con tumores de alto riesgo o subtipos con recidiva tardía requieren vigilancia más allá de los 5 años.
3) Algoritmo práctico de seguimiento
Esquema orientativo de seguimiento. Ajustar a histotipo, estadio, márgenes, respuesta y protocolos del centro. La clave es mantener un seguimiento escalonado y, ante cualquier discordancia o sospecha, salir de la rutina y pasar a estudio dirigido.
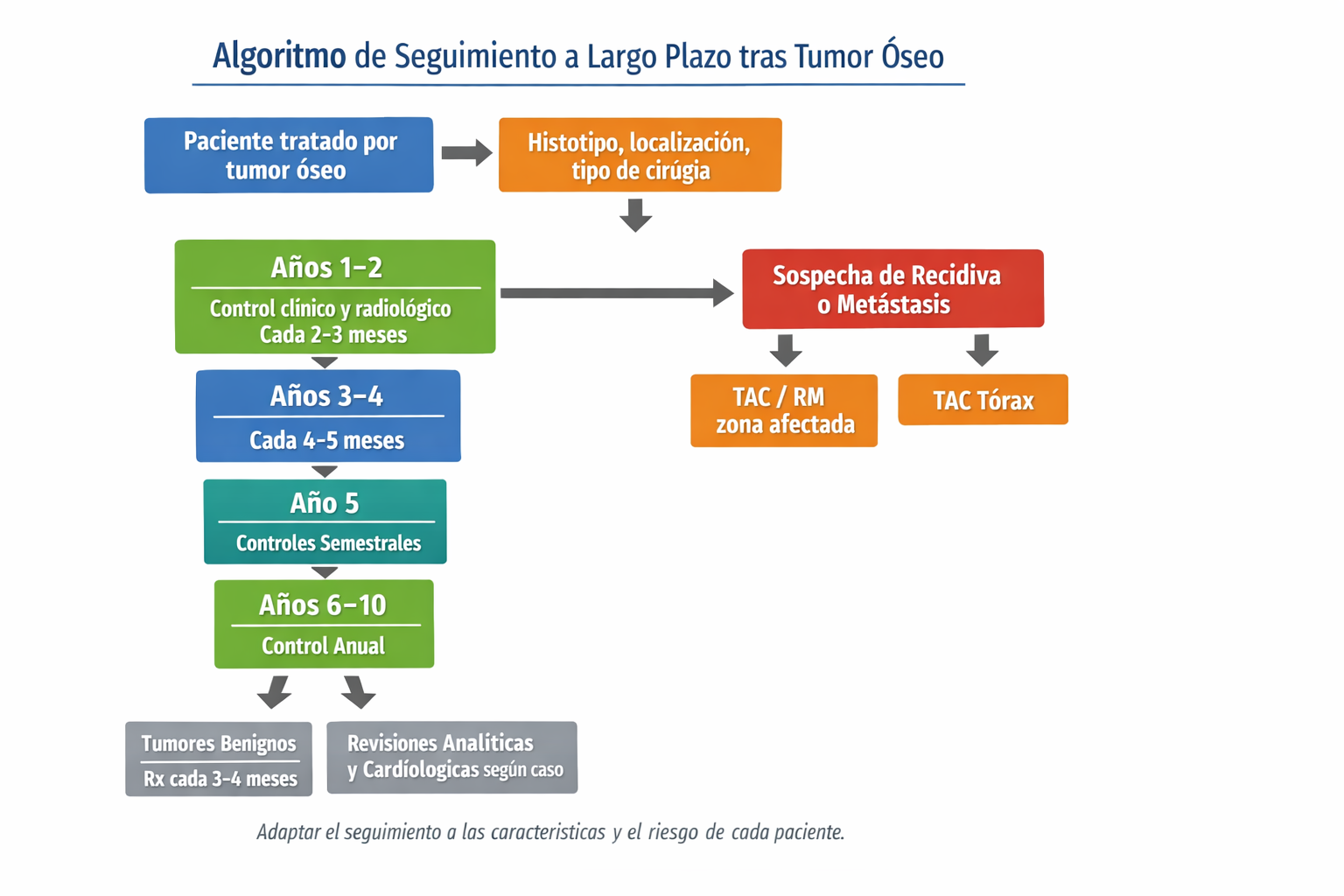
Punto clave: ante cualquier discordancia clínica o radiológica (dolor nuevo, masa, hallazgo en imagen), se sale del protocolo rutinario y se pasa a estudio dirigido con TC o RM de la zona y TC de tórax.
4) Si se sospecha recidiva o metástasis
Cuando existe sospecha clínica o radiológica de recidiva local o metástasis, es necesario realizar un estudio dirigido que permita confirmar o descartar la enfermedad. En estos casos se recomienda:
- TC o RM de la zona de la lesión primaria (o de la zona sospechosa), con contraste cuando esté indicado, para evaluar la extensión local.
- TC de tórax para descartar metástasis pulmonares, que son la localización más frecuente en la mayoría de los sarcomas.
En función de los hallazgos y del contexto clínico, se pueden añadir otras pruebas (PET/TC, biopsia, estudios moleculares) para confirmar el diagnóstico y planificar el tratamiento. La decisión debe tomarse en comité multidisciplinar.
5) Gammagrafía ósea
La gammagrafía ósea se realiza una vez al año, especialmente en pacientes con tumores que tienen tendencia a producir metástasis óseas, como el sarcoma de Ewing, o cuando los síntomas hacen sospechar una localización esquelética. También puede ser útil en el seguimiento de pacientes con tumores óseos primarios de alto riesgo. Sin embargo, su uso rutinario no está indicado en todos los sarcomas, y su interpretación debe hacerse con precaución por la posibilidad de falsos positivos (artrosis, fracturas, áreas de estrés).
6) Tumores benignos
Aunque la mayoría de los tumores óseos benignos no requieren un seguimiento tan estricto como los malignos, es importante mantener controles periódicos para detectar recidivas locales o, en algunos casos, transformación maligna. Se recomiendan controles clínicos y radiográficos cada 3–4 meses durante los 3 primeros años, espaciándose posteriormente si la lesión permanece estable.
En el tumor de células gigantes (TCG), se debe añadir radiografía de tórax al seguimiento debido al potencial (aunque infrecuente) de metástasis pulmonares, que pueden ocurrir incluso muchos años después del tratamiento local. En casos de recidiva local, se debe reevaluar la extensión y considerar un manejo más agresivo.
7) Osteosíntesis / prótesis
En los pacientes en los que se ha implantado material de osteosíntesis (placas, clavos) o una prótesis tumoral, la interpretación de las imágenes puede verse dificultada por artefactos metálicos en TC y RM. Es fundamental que el radiólogo esté informado del tipo de implante y que se utilicen secuencias específicas para minimizar los artefactos (como STIR en RM o protocolos con supresión de metal en TC). La comparación con estudios previos es esencial para distinguir cambios postoperatorios normales de posibles recidivas o complicaciones (aflojamiento, infección, fractura del implante).
En las prótesis tumorales, además del seguimiento oncológico, se debe vigilar la estabilidad mecánica, el estado de las reinserciones musculares y la aparición de complicaciones como infección, aflojamiento o fractura periprotésica.
8) Laboratorio y controles por quimioterapia
En algunos tumores malignos, la determinación seriada de fosfatasa alcalina (en osteosarcoma) y lactato deshidrogenasa (LDH) (en sarcoma de Ewing) puede ser útil como marcador de recidiva o progresión, aunque no son específicos y deben interpretarse en el contexto clínico.
En los pacientes que han recibido quimioterapia, especialmente regímenes con antraciclinas (doxorrubicina) o ifosfamida, se debe realizar un seguimiento de la función cardíaca (ecocardiograma, determinación de troponinas) y función renal (creatinina, filtrado glomerular) según las recomendaciones de las guías clínicas. Los efectos tardíos de la quimioterapia pueden aparecer años después del tratamiento, por lo que la vigilancia debe prolongarse.
Resumen para la práctica clínica
Indicaciones
- ✓ Planificar seguimiento adaptado a histotipo, edad, localización y tratamiento.
- ✓ Protocolizar controles (clínica + Rx local + tórax) según fase evolutiva.
- ✓ Ante sospecha de recidiva/metástasis: TC/RM local + TC de tórax.
- ✓ En tumores con tendencia a metástasis óseas o síntomas: considerar gammagrafía anual.
- ✓ En tumor de células gigantes: incluir control torácico.
Técnica
- 🔧 Asegurar comparabilidad: mismas proyecciones y series cuando sea posible.
- 🔧 Coordinar con radiología en casos con material (artefactos en TC/RM).
- 🔧 Documentar y explicar al paciente el plan y el horizonte de seguimiento (hasta 10 años).
- 🔧 Seleccionar analítica y controles cardiológicos según esquema de quimioterapia.
Riesgos
- ⚠️ Recidiva local o metástasis no detectadas si el seguimiento es insuficiente.
- ⚠️ Falsas alarmas por hallazgos inespecíficos (interpretar con contexto clínico-radiológico).
- ⚠️ Limitaciones de imagen por artefacto de osteosíntesis/prótesis.
- ⚠️ Toxicidad tardía de quimioterapia: necesidad de vigilancia dirigida.
Resultados
- ✅ Seguimiento claro y escalonado, centrado en detección precoz y función.
- ✅ Estrategia práctica ante sospecha de recidiva/metástasis.
- ✅ Control de riesgos específicos: metástasis óseas, tórax y toxicidad por tratamiento.
Bibliografía y lecturas recomendadas
Soft Tissue and Bone Tumours. 5th ed. IARC; 2020.
Bone Cancer / Soft Tissue Sarcoma (versión vigente).
Bone sarcomas; Soft tissue and visceral sarcomas. Ann Oncol. 2021.
Pediatric and Adolescent Osteosarcoma. Springer; 2009.
Seguimiento postoperatorio y oncológico (adaptar a cada centro).
Seguimiento a largo plazo
Cronograma · Recidiva · Metástasis · Función · Toxicidad tardía
