Última revisión:
Condrosarcoma
El condrosarcoma es un tumor maligno productor de matriz cartilaginosa. En la clasificación de la
Organización Mundial de la Salud (OMS), el término tumor cartilaginoso atípico
(ACT, Atypical Cartilaginous Tumor) se usa con frecuencia para el equivalente a
condrosarcoma central grado 1 cuando asienta en el esqueleto apendicular (p. ej., huesos largos).
En el esqueleto axial (p. ej., pelvis, escápula, columna, base de cráneo) suele preferirse
el término condrosarcoma grado 1 por su mayor impacto clínico y quirúrgico.
En la práctica, los retos principales son: (1) distinguir lesiones condroides benignas frente a ACT/condrosarcoma de bajo grado,
(2) reconocer signos de agresividad y subtipos de alto riesgo (p. ej., desdiferenciado, mesenquimal),
y (3) planificar biopsia y cirugía en el circuito correcto (trayecto resecable).
1) Definición y conceptos útiles
El condrosarcoma es un tumor maligno que produce matriz cartilaginosa. Puede ser primario (de novo) o secundario (sobre lesión cartilaginosa previa, típicamente exostosis o encondroma en contextos concretos). Su comportamiento es muy variable, desde lesiones de bajo grado con bajo riesgo metastásico hasta formas altamente agresivas con diseminación sistémica.
Lo que importa en la práctica clínica:
- • Localización: pelvis, columna, base de cráneo implican mayor complejidad quirúrgica y peor margen.
- • Grado (bajo vs alto) y subtipo (desdiferenciado, mesenquimal) determinan el riesgo de metástasis.
- • Márgenes quirúrgicos: son el factor más importante para el control local.
- • Planificación: imagen adecuada y biopsia con trayecto resecable evitan errores irreversibles.
2) Epidemiología y localización
El condrosarcoma predomina en adultos; es excepcional antes de la pubertad. La localización más frecuente es la pelvis y el fémur proximal, seguida de costillas, húmero proximal, tibia proximal y escápula. En los huesos largos suele originarse en la metáfisis/diáfisis y puede invadir la epífisis. Las localizaciones axiales (pelvis, columna, base de cráneo) representan un reto quirúrgico mayor y un umbral más bajo para derivación a centros especializados.
Idea práctica: en pelvis y localizaciones profundas, el diagnóstico suele ser más tardío y la resección más compleja; por eso el umbral de derivación a una unidad de sarcomas debe ser bajo.
3) Presentación clínica
La presentación clínica típica es un dolor persistente y progresivo de meses de evolución, a menudo sordo, que puede interferir el sueño y no mejora claramente con el reposo. Según la localización, puede haber cojera (pelvis, fémur proximal) o síntomas por compresión neurológica (columna, sacro). En la exploración física puede no palparse una masa evidente, o bien haber una tumefacción discreta. La limitación articular adyacente y la marcha antiálgica son hallazgos frecuentes.
4) Señales de alarma
Cuándo sospechar malignidad o progresión
- Dolor progresivo, persistente, nocturno o no mecánico que no responde a analgesia convencional.
- Crecimiento rápido de una masa o aumento claro de volumen en semanas o meses.
- Destrucción ósea agresiva en imagen (patrón permeativo, cortical rota, gran componente de partes blandas).
- Fractura patológica o debilidad estructural marcada sin traumatismo significativo.
- Recidiva precoz o repetida tras tratamiento previo.
Cuándo activar biopsia / circuito tumoral
- Cualquier lesión con masa de partes blandas o cortical rota.
- Lesión con criterios de agresividad en RX/TC/RM, aunque la clínica sea poco llamativa.
- Lesión indeterminada en la que el diagnóstico pueda cambiar el tratamiento.
- Nunca biopsiar “por tu cuenta” sin planificar la vía como si fuera un sarcoma.
Regla práctica: ante duda razonable, se deriva y se aborda como potencial lesión tumoral hasta demostrar lo contrario.
5) Imagen: lo que aporta RX / TC / RM
La imagen orienta de forma crucial en el diagnóstico del condrosarcoma. La radiografía simple muestra las características calcificaciones condroides en "anillos y arcos" o "palomitas", y permite evaluar la erosión endostal (scalloping), la expansión cortical, la reacción perióstica y la presencia de una masa de partes blandas asociada. La tomografía computarizada (TC) es superior para definir la mineralización y la integridad cortical, especialmente en localizaciones complejas como pelvis, costillas y escápula. La resonancia magnética (RM) es la prueba de elección para valorar la extensión medular, la relación con partes blandas y planificar el abordaje quirúrgico.
Error a evitar: etiquetar como “metástasis” por la edad del paciente sin revisar el patrón condroide y sin completar el estudio de imagen con TC/RM.
📷 Radiografía
La radiografía suele mostrar matriz condroide calcificada, con patrón en anillos y arcos, junto con scalloping endostal y posible expansión cortical.
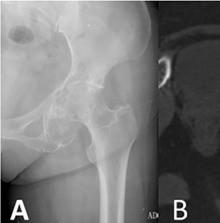
Figura 1. Radiografía de condrosarcoma con matriz condroide calcificada.
🖥️ Tomografía computarizada (TC)
La TC define mejor la mineralización condroide y la integridad cortical, y es especialmente útil en pelvis, costillas, escápula y otras localizaciones complejas.
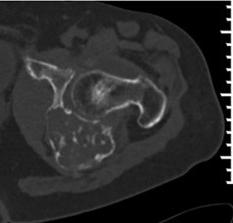
Figura 2. TC de condrosarcoma con mejor definición de la mineralización y la cortical.
🧲 Resonancia magnética (RM)
La RM es la prueba de elección para valorar la extensión medular, la masa de partes blandas y la planificación quirúrgica.
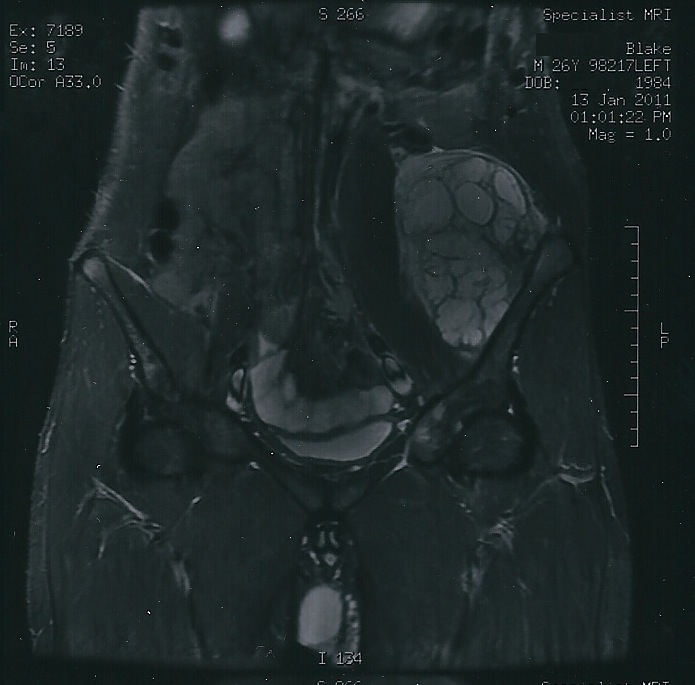
Figura 3. RM de condrosarcoma para valorar la extensión local.
6) Checklist práctico: encondroma vs ACT / bajo grado
Idea clave (OMS): en huesos largos y esqueleto apendicular se usa con frecuencia el término ACT (tumor cartilaginoso atípico) para lesiones de bajo grado; en el esqueleto axial (pelvis, escápula, columna) suele preferirse “condrosarcoma grado 1” por su mayor riesgo local y peor resecabilidad.
| Dato | Más compatible con benignidad | Más compatible con ACT / bajo grado |
|---|---|---|
| Clínica | Asintomático o dolor no progresivo, no atribuible claramente a la lesión. | Dolor progresivo, persistente, “nuevo” o que despierta al paciente. |
| Erosión endostal | Leve, estable en el tiempo, sin progresión. | Amplia, profunda (>2/3 del diámetro cortical), progresiva en controles. |
| Cortical | Íntegra, sin rotura, con borde escleroso. | Adelgazamiento marcado, rotura cortical o reacción perióstica agresiva. |
| Partes blandas | No hay masa extraósea. | Masa de partes blandas (señal de alarma mayor). |
| Crecimiento | No demostrado en seguimiento o crecimiento muy lento. | Crecimiento demostrado en controles seriados. |
Nota: en las lesiones condroides, el diagnóstico real suele ser integrado (clínica + imagen + anatomía patológica), porque la histología aislada puede ser sutil y no reflejar el comportamiento agresivo.
7) Biopsia: reglas de seguridad
Regla de oro: la biopsia debe estar planificada por el equipo que realizará la cirugía definitiva, con un trayecto que pueda ser resecado en bloque con el tumor. Una biopsia mal realizada puede contaminar planos anatómicos, empeorar la resección y aumentar el riesgo de recidiva.
Enfoque práctico
Si la sospecha clínica y radiológica es clara, una biopsia con aguja gruesa (core needle) guiada por imagen suele ser suficiente, siempre que el trayecto sea elegido en coordinación con el cirujano. En casos complejos o cuando se necesita más tejido para estudios complementarios (inmunohistoquímica, genética molecular), puede estar indicada una biopsia abierta o incisional planificada. Es importante recordar la heterogeneidad tumoral: el grado puede subestimarse si la muestra se toma de una zona “amable” o periférica.
8) Patología, grado y notas OMS
El condrosarcoma de bajo grado puede parecerse mucho a un encondroma. La clave diagnóstica suele ser el patrón global (imagen + clínica) y los signos de infiltración o actividad (invasión de hueso medular, atipia citológica, hipercelularidad). El sistema de gradación (grado 1, 2 y 3) es pronóstico y se basa en la celularidad, la atipia nuclear y la actividad mitótica.
| Grado | Idea práctica |
|---|---|
| Grado 1 / ACT | Muy parecido a benigno; riesgo metastásico muy bajo (<2%). Dificultad: distinguir de encondroma → manda la integración clínico-radiológica y el manejo en centro experto. |
| Grado 2 | Mayor celularidad y atipia; riesgo metastásico intermedio (10-20%). Puede tener áreas mixoides. |
| Grado 3 | Atipia marcada, mayor riesgo de metástasis (>50%). Requiere seguimiento más estricto. |
Genética/molecular (útil en subtipos)
- IDH1/IDH2: frecuentes en condrosarcoma convencional central (y en lesiones relacionadas). Su detección apoya el diagnóstico pero no define el grado.
- Mesénquimal: suele asociar alteraciones específicas como HEY1::NCOA2 en muchas series.
- En enfermedad avanzada seleccionada con IDH1 mutado, existen datos clínicos con inhibidores IDH1 (p. ej., ivosidenib) que han mostrado control de enfermedad en parte de los pacientes.
Mensaje clínico: si hay duda real “encondroma vs ACT/condrosarcoma de bajo grado”, la decisión se toma en circuito especializado, priorizando la seguridad oncológica y evitando sobretratar lesiones estables.
9) Condrosarcoma típico (primario y central)
El condrosarcoma central convencional es el subtipo más frecuente. Se origina en el interior del hueso, típicamente en la metáfisis o diáfisis de huesos largos, con extensión hacia la epífisis en estadios avanzados. Las localizaciones más comunes son pelvis, fémur proximal, húmero proximal, costillas y escápula. Clínicamente se manifiesta con dolor persistente y progresivo, a veces nocturno, y cojera si afecta a la extremidad inferior. La base del tratamiento es la resección quirúrgica completa con márgenes oncológicos adecuados. En el condrosarcoma convencional, la quimioterapia y la radioterapia tienen un papel muy limitado, reservándose para situaciones excepcionales.
10) Otros condrosarcomas (subtipos)
10.1) Condrosarcoma desdiferenciado
Subtipo raro y muy agresivo, caracterizado por la coexistencia de un componente condroide bien diferenciado junto a un sarcoma de alto grado no condroide (osteosarcoma, fibrosarcoma, pleomórfico). El riesgo de metástasis es elevado, y el manejo requiere estadiaje completo y un enfoque multidisciplinar en unidad de sarcomas, con cirugía amplia y consideración de tratamiento sistémico según protocolo.
10.2) Condrosarcoma extraóseo (partes blandas)
Tumor raro que se origina en tejidos blandos, sin relación con el hueso subyacente. Se maneja como un sarcoma de partes blandas, con resección amplia y, en casos seleccionados, radioterapia adyuvante. El pronóstico depende del grado y la resecabilidad.
10.3) Condrosarcoma de células claras
Tumor raro de crecimiento lento, a menudo epifisario, que puede confundirse con un condroblastoma pero tiene comportamiento maligno. Es más frecuente en fémur proximal y húmero proximal. El tratamiento consiste en resección quirúrgica con márgenes adecuados; el pronóstico es mejor que el de otros condrosarcomas de alto grado.
10.4) Condrosarcoma mesenquimal
Subtipo poco frecuente con potencial agresivo; puede ser óseo o de partes blandas. Histológicamente combina áreas de cartílago bien diferenciado con áreas de células pequeñas redondas (patrón tipo Ewing). El manejo es multidisciplinar, con estadificación sistemática y estrategia sistémica individualizada según protocolos de sarcomas.
10.5) Condrosarcoma de la base del cráneo
Localización compleja, que condiciona el manejo. El tratamiento combina cirugía cuando es posible (a menudo parcial) y radioterapia de alta precisión (protonterapia, radioterapia con partículas) en equipos neuro-oncológicos especializados. El pronóstico depende de la resecabilidad y la respuesta a la radioterapia.
10.6) Condrosarcoma periférico (sobre exostosis)
Surge sobre una exostosis osteocartilaginosa (solitaria o múltiple). La TC y la RM ayudan a valorar el componente cartilaginoso (capuchón engrosado, >2 cm) y la extensión. El tratamiento es quirúrgico, con resección en bloque incluyendo la exostosis y el tejido blando adyacente.
10.7) Condrosarcoma perióstico (yuxtacortical)
Tumor raro de superficie ósea (fémur, tibia, húmero), que crece sobre la cortical. En radiografía se ve una masa calcificada adherida al hueso, con "saucerización" cortical. El manejo consiste en resección amplia, que suele ser curativa en la mayoría de los casos.
11) Tratamiento
El pilar del tratamiento es la cirugía, con el objetivo de lograr una resección completa (márgenes amplios) cuando sea posible. La elección de la técnica quirúrgica depende de la localización, el grado y la extensión tumoral. En el condrosarcoma convencional, la quimioterapia y la radioterapia tienen un papel limitado; se reservan para subtipos agresivos, localizaciones complejas o enfermedad avanzada seleccionada.
Principios quirúrgicos
- Márgenes quirúrgicos: la resección con márgenes adecuados es el factor más importante para prevenir la recidiva local. Los márgenes intralesionales o marginales se asocian a un mayor riesgo de recaída.
- Localizaciones complejas: pelvis, columna y base de cráneo requieren una planificación detallada y, a menudo, abordajes combinados con radioterapia adyuvante.
- Recidiva local: si es resecable con margen, puede ser tratable; si la recidiva es precoz o cambia el patrón histológico, se debe sospechar progresión de grado.
Radioterapia (cuándo tiene sentido)
- Escenarios anatómicos donde el margen quirúrgico completo es muy difícil (p. ej., base de cráneo, columna cervical) y en enfermedad residual seleccionada.
- Preferencia por técnicas conformadas y, cuando está disponible, radioterapia con partículas (protones, carbono) para minimizar la toxicidad sobre estructuras nobles.
Tratamiento sistémico (muy resumido)
- Convencional: la respuesta a la quimioterapia es generalmente limitada; no se recomienda de forma rutinaria en el manejo inicial.
- Subtipos agresivos (desdiferenciado, mesenquimal): la estrategia sistémica se individualiza en unidad de sarcomas, con quimioterapia o terapias dirigidas según el perfil molecular.
- Enfermedad avanzada IDH1-mutada: existen datos clínicos con ivosidenib (inhibidor de IDH1) en series y ensayos seleccionados, con control de enfermedad en parte de los pacientes.
12) Pronóstico y seguimiento
El pronóstico depende sobre todo del grado, el subtipo, la localización y la calidad de los márgenes quirúrgicos. El seguimiento se individualiza según el riesgo. Como regla general, el control se centra en la recidiva local (con RM o TC según localización) y en la detección de metástasis pulmonares (TC de tórax). La intensidad del seguimiento es mayor en los primeros años y puede espaciarse si no hay evidencia de recidiva. En pacientes con subtipos agresivos o grados altos, se recomienda seguimiento prolongado.
13) Algoritmos prácticos
13.2) Biopsia segura (trayecto resecable)

13.3) Manejo por riesgo (grado/subtipo/localización)

Resumen para la práctica clínica
Indicaciones
- ✓ Lesión condroide con dolor progresivo o signos de agresividad en imagen.
- ✓ Dudas entre encondroma vs ACT/condrosarcoma de bajo grado (especialmente en pelvis o si hay síntomas).
- ✓ Sospecha de subtipo agresivo (desdiferenciado, mesenquimal) o masa de partes blandas.
- ✓ Recidiva local o cambio rápido del patrón clínico/radiológico.
Técnica
- 🔧 RX + TC (mineralización/cortical) y RM (extensión medular/partes blandas) para plan.
- 🔧 Biopsia planificada por el equipo definitivo; trayecto resecable; evitar contaminación.
- 🔧 Tratamiento base: resección completa con márgenes adecuados cuando sea posible.
- 🔧 En subtipos/localizaciones complejas: comité multidisciplinar (unidad de sarcomas).
Riesgos
- ⚠️ Recidiva local si márgenes insuficientes o localización compleja.
- ⚠️ Metástasis (sobre todo en grados altos y subtipos agresivos).
- ⚠️ Impacto funcional y complicaciones reconstructivas según localización.
Resultados
- ✅ Bajo grado resecado completamente: control local alto en muchos casos.
- ✅ Grados altos/subtipos agresivos: más riesgo sistémico; seguimiento más estricto.
- ✅ La seguridad oncológica depende de planificación (imagen/biopsia) y márgenes.
14) Bibliografía
Soft Tissue and Bone Tumours. 5th ed. IARC; 2020.
Chondrosarcoma: A Clinical Review. Curr Oncol. 2023;30(3):3425-3437.
Ivosidenib in advanced IDH1-mutant chondrosarcoma. J Clin Oncol. 2024;42(15_suppl):11512.
Resultados oncológicos y rol de cirugía + radioterapia de precisión (incluye protonterapia).
Tumores cartilaginosos y uso de “ACT” en esqueleto apendicular.
Condrosarcoma: guía práctica
Clasificación · Grados · Subtipos · Tratamiento · Seguimiento
