Última revisión:
Características de Algunos Tumores Óseos
Esta página constituye un resumen orientativo de las características clínicas, radiológicas y de manejo
de los principales tumores óseos. Integra información sobre edad típica, localización más frecuente,
patrón radiológico y tratamiento habitual.
Las frecuencias, edades y patrones radiológicos varían según las series y registros. En sospecha de lesión agresiva o sarcoma,
lo recomendable es derivar a una unidad o centro de referencia y discutir el caso en comité multidisciplinar.
Esta tabla es una guía práctica, no un sustituto del diagnóstico integrado clínico-radiológico-patológico.
Índice de contenido
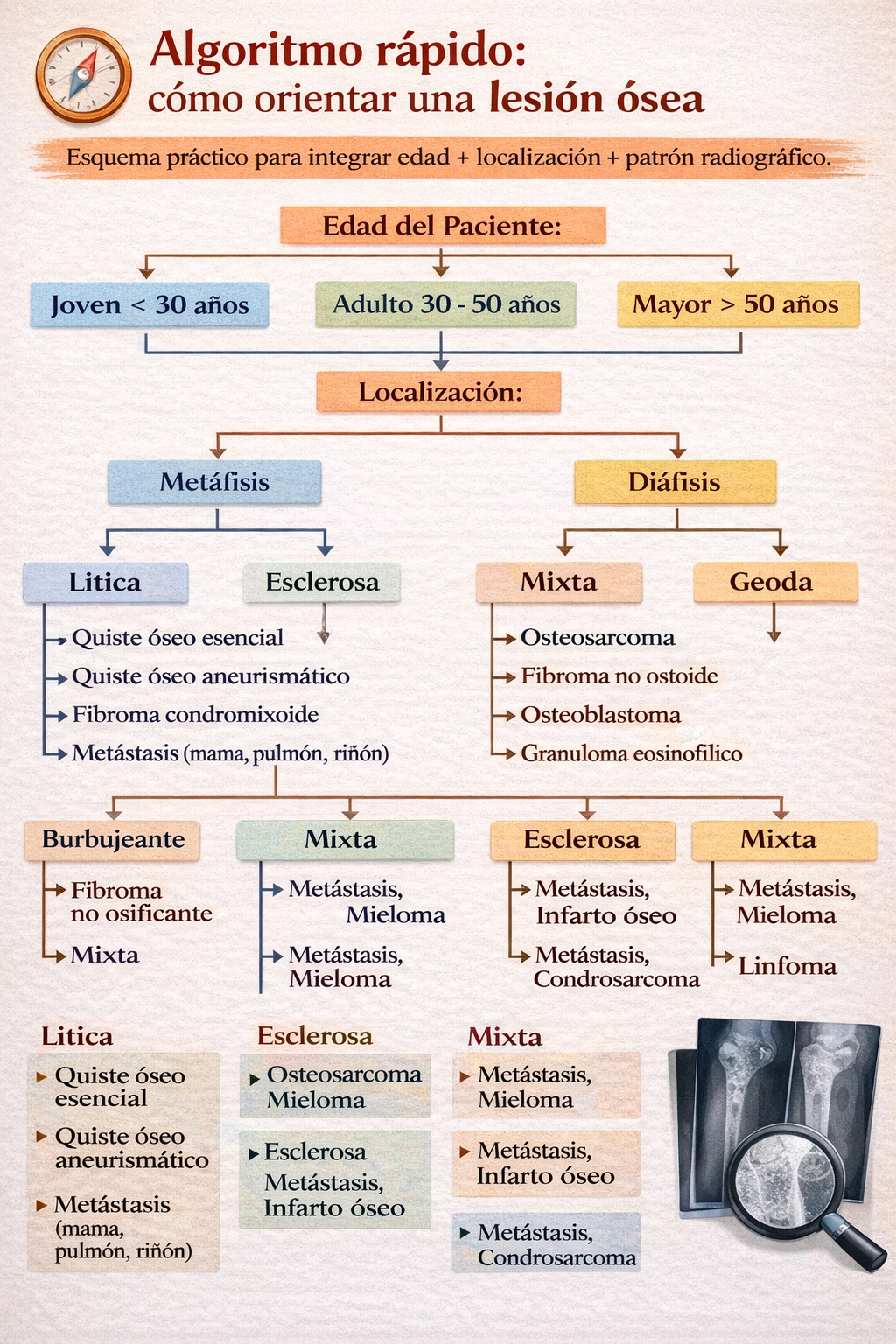
Algoritmo rápido: cómo orientar una lesión ósea
Esquema práctico para integrar edad + localización + patrón radiográfico. Este algoritmo ayuda a orientar el diagnóstico diferencial, pero la decisión final requiere siempre correlación con anatomía patológica en casos dudosos.
1) Tumores cartilaginosos
Punto clave: Diferenciar encondroma de condrosarcoma de bajo grado por síntomas (dolor atribuible), crecimiento documentado y signos radiológicos de agresividad (endostosis marcada, erosión cortical, masa de partes blandas).
| Entidad | Edad típica | Localización | Radiología | Tratamiento |
|---|---|---|---|---|
| Encondroma | 10-40 años | Mano/pie, huesos largos (metáfisis) | Calcificaciones en "aros y anillos", patrón lobulado, matriz condroide. | Observación / curetaje si sintomático o con duda. |
| Condroblastoma | Adolescente (10-20 años) | Epífisis de huesos largos (rodilla, húmero) | Lítico epifisario, edema perilesional en RM, calcificaciones finas. | Curetaje + adyuvante local (fenol, criocirugía). |
| Osteocondroma | Niño-joven (10-30 años) | Metáfisis de rodilla, húmero proximal, pelvis | Exostosis con continuidad cortical y medular con el hueso madre. | Observación; resección si síntomas, crecimiento post-madurez o sospecha de transformación. |
| Fibroma condromixoide | Joven (10-30 años) | Metáfisis tibial (frecuente), fémur | Lítico excéntrico con aspecto "burbuja", bordes esclerosos. | Curetaje + injerto óseo. |
| Condrosarcoma | 30-70 años | Pelvis, fémur proximal, costillas, húmero | Matriz condroide, erosión cortical, endostosis, crecimiento progresivo. | Resección amplia (márgenes oncológicos). RT en casos seleccionados. |
2) Tumores formadores de hueso
| Entidad | Edad típica | Localización | Radiología | Tratamiento |
|---|---|---|---|---|
| Osteoma | Adulto | Cráneo, senos paranasales, mandíbula | Densa, bien delimitada, homogénea. | Observación / resección si síntomas estéticos o funcionales. |
| Osteoma osteoide | 10-30 años | Cortical de fémur, tibia, columna posterior | Nidus central (< 2 cm) con esclerosis reactiva perilesional. Dolor nocturno característico. | Ablación percutánea con radiofrecuencia (curativa en >95%). |
| Osteoblastoma | 10-30 años | Columna posterior, fémur, tibia | Lítico expansivo >2 cm, puede tener calcificaciones. Dolor menos característico que osteoma osteoide. | Escisión amplia (puede recidivar si resección incompleta). |
| Osteosarcoma | Adolescente (10-25 años) / adulto mayor secundario | Metáfisis de fémur distal, tibia proximal, húmero proximal | Matriz osteoide (nube densa), reacción perióstica (Codman, sol naciente), destrucción cortical. | Quimioterapia neoadyuvante + cirugía amplia ± quimioterapia adyuvante. |
3) Lesiones pseudotumorales
| Entidad | Edad | Localización | Radiología | Manejo |
|---|---|---|---|---|
| Fibroma no osificante | Niño/adolescente | Metáfisis excéntrica de fémur, tibia | Elíptica, borde escleroso, central radiolúcido. Asintomática. | Observación. Resuelve espontáneamente con la madurez esquelética. |
| Displasia fibrosa | 10-30 años | Costillas, fémur proximal, cráneo, tibia | "Vidrio esmerilado", expansión ósea, cayado de pastor en fémur. | Observación. Cirugía si deformidad, dolor, fractura o sospecha. |
| Histiocitosis de células de Langerhans (granuloma eosinófilo) | Niño (5-15 años) | Cráneo ("botón a botón"), costillas, vértebras (vértebra plana), fémur | Lítica, bordes bien definidos, puede tener secuestro óseo. | Biopsia ± curetaje. Observación en lesiones seleccionadas. |
| Quiste óseo aneurismático | Niño/adolescente | Metáfisis de huesos largos, columna posterior | Expansivo, niveles líquido-líquido en RM, cortical adelgazada. | Curetaje + adyuvantes (fenol, criocirugía), embolización selectiva. |
| Quiste óseo simple | Niño (3-15 años) | Húmero proximal, fémur proximal | Lítico central, adelgazamiento cortical, "fragmento caído". | Observación; infiltración con corticosteroides si riesgo de fractura. |
4) Tumores misceláneos de hueso
| Entidad | Edad típica | Localización | Radiología | Tratamiento |
|---|---|---|---|---|
| Tumor de células gigantes (TCG) | 20-50 años | Epífisis de huesos largos (rodilla, radio distal), sacro | Lítico excéntrico, subcondral, sin esclerosis periférica. | Curetaje amplio + adyuvantes. Denosumab neoadyuvante en casos seleccionados. |
| Adamantinoma | Adulto joven (20-40 años) | Diáfisis tibial (95%), peroné | Lítico, bordes nítidos, multiloculado, expansión cortical. | Resección amplia (márgenes oncológicos). Seguimiento prolongado por riesgo de metástasis tardías. |
| Cordoma | Adulto (40-70 años) | Sacro, clivus, columna cervical | Lítico destructivo, masa de partes blandas, calcificaciones. | Cirugía amplia + radioterapia de alta energía (protones). |
| Leiomiosarcoma óseo | >20 años (raro) | Fémur, tibia, pelvis | Lítico agresivo, mal definido, destrucción cortical. | Cirugía amplia ± quimioterapia/radioterapia según grado. |
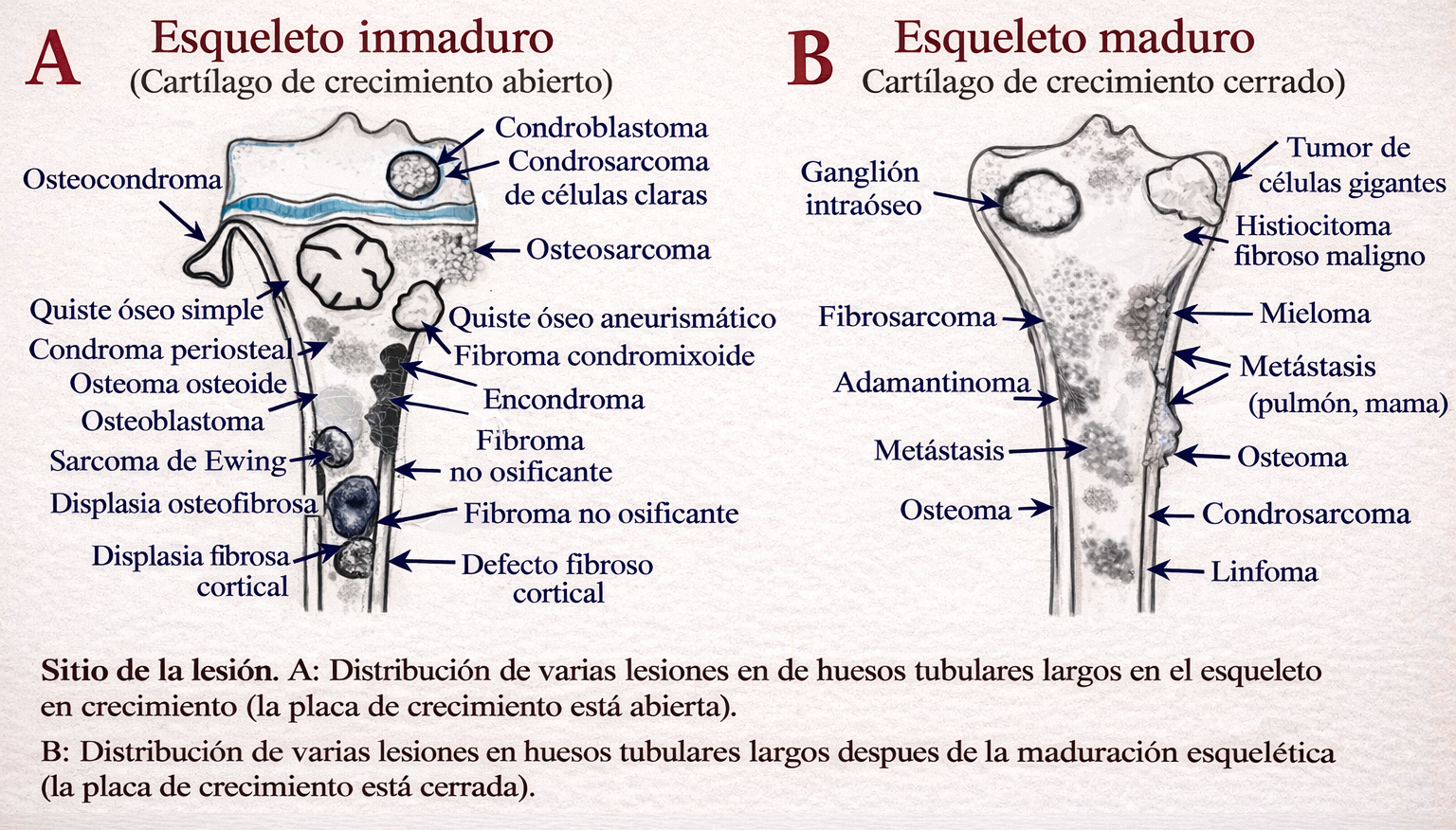
Mapa visual: edad y zona del hueso
Resumen visual por edad y localización (epífisis/metáfisis/diáfisis/axial). Este mapa ayuda a orientar el diagnóstico diferencial según la localización anatómica y el grupo etario.
5) Tumores de células redondas
Estrategia correcta: biopsia planificada, evitar cirugías no oncológicas, confirmación histológica con inmunohistoquímica y estudios moleculares según sospecha.
| Entidad | Edad | Localización | Pistas clínico-radiológicas |
|---|---|---|---|
| Sarcoma de Ewing | Niño-adolescente (5-20 años) | Diáfisis de huesos largos, pelvis, costillas | Dolor, masa de partes blandas, fiebre, patrón permeativo, reacción perióstica laminada ("capas de cebolla"). |
| Linfoma óseo primario | Adulto (>50 años) | Fémur, pelvis, columna | Dolor, masa, imagen variable (puede simular osteomielitis). Biopsia esencial. |
| Mieloma múltiple / plasmocitoma | >50 años | Columna, pelvis, cráneo, costillas | Lesiones líticas múltiples "en sacabocados", dolor, anemia, proteinograma monoclonal. |
| Histiocitosis de células de Langerhans | Niño (5-15 años) | Cráneo, costillas, vértebras, fémur | Lesión lítica aislada o múltiple, vértebra plana, "botón a botón" en cráneo. |
6) Fibrosos / fibro-histiocíticos
En la literatura antigua aparece el término "histiocitoma fibroso maligno (MFM)" o "fibrohistiocitoma maligno". Hoy, estos diagnósticos se reclasifican como sarcoma pleomórfico indiferenciado (UPS) tras excluir otras líneas de diferenciación (liposarcoma, leiomiosarcoma, MPNST, etc.).
🟢 Benignos / frecuentes
- Fibroma no osificante – lesión cortical benigna, resuelve espontáneamente.
- Desmoide (fibromatosis) – localmente agresivo, sin metástasis, manejo con observación activa.
- Histiocitoma fibroso benigno – lesión dérmica frecuente.
🔴 Malignos (concepto moderno)
- UPS (sarcoma pleomórfico indiferenciado) – diagnóstico de exclusión tras descartar otras estirpes.
- Fibrosarcoma – raro como entidad "pura" en la clasificación actual.
- Otros sarcomas reclasificados – leiomiosarcoma, liposarcoma pleomórfico, MPNST.
7) Alertas rápidas: cuándo pensar en malignidad
- ! Dolor no mecánico, progresivo, nocturno – orienta a malignidad o osteoma osteoide.
- ! Crecimiento documentado de lesión ósea o masa de partes blandas.
- ! Destrucción cortical y reacción perióstica agresiva (lamelada, "sol naciente", espolón de Codman).
- ! Masa de partes blandas asociada a lesión ósea – sugiere extensión extraósea.
- ! Lesión en pelvis / axial con rasgos cartilaginosos – mayor riesgo de condrosarcoma.
- ! Sospecha de sarcoma → biopsia planificada, nunca curetaje o exéresis sin diagnóstico.
- ! Discordancia clínico-radiológica – si la imagen no encaja con la clínica, ampliar estudio.
Regla práctica: si dudas, trata el caso como potencial sarcoma hasta demostrar lo contrario. La derivación temprana a un centro especializado es la mejor inversión.
Resumen para la práctica clínica
Indicaciones
- ✓ Cuadros con duda diagnóstica tras clínica + imagen.
- ✓ Lesiones con signos de agresividad o crecimiento.
- ✓ Diferencial benigno vs maligno (cartílago en pelvis, síntomas progresivos).
- ✓ Necesidad de biopsia planificada y circuito oncológico.
- ✓ Derivación a centro especializado si sospecha de sarcoma.
Técnica
- 🔧 Biopsia planificada (evitar contaminar compartimentos).
- 🔧 Correlación radiología–patología: elegir zona viable.
- 🔧 Evitar cirugías intralesionales en lesiones potencialmente malignas.
- 🔧 Integrar hallazgos con anatomía patológica; usar inmuno/molecular.
Riesgos
- ⚠️ Error de muestreo (biopsia poco representativa).
- ⚠️ Tratamientos intralesionales que complican resecciones.
- ⚠️ Interpretación radiológica aislada sin correlación.
- ⚠️ Demoras por no derivar a circuito especializado.
Resultados
- ✅ La mayoría de decisiones se basan en diagnóstico integrado.
- ✅ Si la sospecha es alta, priorizar confirmación diagnóstica.
- ✅ En sarcomas, el manejo cambia radicalmente según entidad/grado.
- ✅ Evitar infratratamiento o cirugías inadecuadas.
Bibliografía y lecturas recomendadas
Soft Tissue and Bone Tumours. 5th ed. IARC; 2020.
Bone sarcomas. Ann Oncol. 2021;32:1520-1536.
Bone Cancer. Version 2.2026.
Differential Diagnosis of Tumors and Tumor-Like Lesions of Bones and Joints. Lippincott-Raven.
Bone and Soft Tissue Tumors. Springer; 1999.
Correlación radio-patológica en tumores óseos (literatura actualizada).
Resumen práctico de tumores óseos
Edad · Localización · Patrón radiológico · Agresividad · Biopsia planificada
