Última revisión:
Biología Molecular en Tumores Musculoesqueléticos
En tumores óseos y de partes blandas, la biología molecular ha pasado de ser "un extra" a convertirse, en muchos casos, en una herramienta fundamental que confirma el diagnóstico, afina la clasificación OMS, aporta información pronóstica y, en escenarios seleccionados, orienta tratamientos dirigidos o el acceso a ensayos clínicos. Sin embargo, no sustituye a la clínica, la imagen ni la anatomía patológica: las completa, integrándose en un enfoque multidisciplinar.
1) ¿Por qué importa en sarcomas?
Muchos sarcomas y tumores óseos raros tienen alteraciones genéticas características que pueden detectarse mediante técnicas moleculares. Detectar estas alteraciones puede:
- ✓ Confirmar un diagnóstico cuando la morfología es dudosa o atípica.
- ✓ Distinguir entidades con pronóstico y tratamiento radicalmente diferentes.
- ✓ Evitar errores diagnósticos en lesiones que parecen benignas sin serlo.
- ✓ Seleccionar terapia dirigida en casos concretos con dianas accionables.
- ✓ Acceder a ensayos clínicos cuando se identifican alteraciones moleculares específicas.
Idea clave: lo molecular se solicita cuando responde a una pregunta clínica real, no como un cribado indiscriminado.
2) Conceptos básicos (sin jerga innecesaria)
El cáncer es, en esencia, una enfermedad del material genético de las células tumorales. La mayoría de los sarcomas no son hereditarios, sino que surgen por alteraciones adquiridas en las células somáticas. Dos grandes grupos de genes están implicados en la tumorigénesis:
🛑 Genes "freno" (supresores tumorales)
Estos genes codifican proteínas que evitan divisiones celulares inadecuadas. Cuando se inactivan (por mutación o deleción), el freno falla. Ejemplos característicos en sarcomas son TP53 y RB1.
🚀 Genes "acelerador" (oncogenes)
Si estos genes se activan de forma anómala (por mutación, amplificación o translocación), envían señales de crecimiento continuas. Ejemplo típico es la amplificación de MDM2 en liposarcomas bien diferenciados.
En sarcomas, es muy frecuente que la "firma" molecular sea una fusión génica resultante de una translocación cromosómica equilibrada.
3) Tipos de alteraciones genéticas relevantes
Las alteraciones genéticas que se detectan en los sarcomas son diversas. Cada una tiene implicaciones diagnósticas y, en algunos casos, pronósticas o terapéuticas:
- Translocaciones / fusiones: crean un gen "quimérico" con actividad oncogénica. Es el mecanismo más característico en sarcomas (Ewing, sinovial, liposarcoma mixoide).
- Mutaciones puntuales: cambios en una sola base que pueden activar oncogenes (IDH1/IDH2 en tumores cartilaginosos) o inactivar supresores.
- Amplificaciones: aumento del número de copias de un gen, como MDM2 en liposarcomas bien diferenciados o MYC en angiosarcomas radioinducidos.
- Deleciones/pérdidas: pérdida de material genético que inactiva supresores tumorales.
- Alteraciones epigenéticas: cambios en la metilación del ADN que pueden generar firmas diagnósticas útiles en tumores difíciles de clasificar.
Traducción clínica: una firma molecular reconocida ayuda a cerrar el diagnóstico y evitar tratamientos inadecuados.
4) Técnicas: qué aporta cada una y cuándo se usa
No se solicita "todo a todos". La técnica se elige según la pregunta clínica, la calidad de la muestra y la sospecha diagnóstica. Cada técnica tiene sus indicaciones y limitaciones:
| Técnica | Qué detecta | Cuándo es útil |
|---|---|---|
| Inmunohistoquímica (IHQ) | Proteínas (expresión) | Primera línea: orienta linaje, confirmación de sobreexpresión (STAT6, MDM2). |
| FISH (hibridación in situ fluorescente) | Reordenamientos / amplificaciones | Fusiones específicas (EWSR1, SS18) y amplificaciones (MDM2). Buen rendimiento incluso con descalcificación. |
| RT-PCR | Fusiones concretas (ARN) | Detección de una fusión específica cuando hay buena calidad de ARN. |
| NGS (paneles de secuenciación) | Mutaciones + fusiones + CNV | Casos complejos, tumores indiferenciados, búsqueda de dianas en enfermedad avanzada. |
| Perfil de metilación | Firma epigenética | Tumores difíciles de clasificar (sarcoma de Ewing-like, sarcomas indiferenciados). |
Regla de oro: primero define qué quieres resolver; luego elige la técnica más eficiente para responder a esa pregunta.
5) Fase preanalítica: biopsia, fijación y descalcificación
El mayor enemigo de la biología molecular no es la tecnología: es la muestra. Una muestra inadecuada, mal conservada o mal procesada puede invalidar cualquier estudio molecular. Por ello, la fase preanalítica es crítica.
🧷 Biopsia planificada
- Trayecto pensado para la resección definitiva (resecable en bloque).
- Muestreo suficiente (múltiples cilindros) evitando zonas de necrosis.
- Coordinación entre radiología, cirugía y anatomía patológica.
🧫 Fijación y logística
- Evitar tiempos extremos de isquemia fría (preferiblemente < 1 hora).
- Reservar material para ARN/fusiones (congelación o conservante adecuado).
- Registrar meticulosamente los datos del procesado.
Descalcificación (punto crítico): usar EDTA en lugar de ácidos fuertes (ácido nítrico, ácido fórmico) para preservar el ADN y el ARN. Avisar al laboratorio si se necesita estudio molecular para que utilicen el protocolo adecuado.
6) Algoritmo de decisión molecular en sarcomas
Algoritmo práctico para decidir qué prueba molecular solicitar según el objetivo diagnóstico y la calidad de la muestra disponible:
Regla operativa: tumor indiferenciado / de células pequeñas redondas → enfoque con ARN para detección de fusiones (NGS o RT-PCR dirigida).
7) Ejemplos clínicos 'clásicos' que sí cambian decisiones
Estos son ejemplos de alteraciones moleculares que tienen un impacto directo en el diagnóstico y, en algunos casos, en el tratamiento o pronóstico:
🧬 Fusiones "clásicas"
- Sarcoma de Ewing: EWSR1–FLI1 (y otras variantes con EWSR1)
- Sarcoma sinovial: SS18–SSX1/SSX2
- Rabdomiosarcoma alveolar: PAX3/7–FOXO1
- Liposarcoma mixoide: FUS–DDIT3 (o EWSR1–DDIT3)
- DFSP (dermatofibrosarcoma protuberans): COL1A1–PDGFB
- Tumor fibroso solitario (SFT): NAB2–STAT6
🎯 Alteraciones con implicación práctica
- MDM2: amplificación en liposarcomas bien diferenciados y desdiferenciados.
- IDH1/IDH2: mutaciones en tumores cartilaginosos (condrosarcoma central de bajo grado).
- H3F3A (G34W): mutación característica del tumor de células gigantes óseo.
- CIC / BCOR: familias "Ewing-like" con comportamiento más agresivo.
- ALK, ROS1, NTRK: dianas terapéuticas en subtipos específicos (IMT, sarcoma infantil).
8) Tabla rápida (tumor ↔ alteración ↔ prueba típica)
| Entidad | Alteración típica | Prueba habitual |
|---|---|---|
| Sarcoma de Ewing | EWSR1–FLI1 (u otras con EWSR1/FUS) | FISH / RT-PCR / NGS |
| Sarcoma sinovial | SS18–SSX | FISH / RT-PCR / NGS |
| Rabdomiosarcoma alveolar | PAX3/7–FOXO1 | FISH / RT-PCR / NGS |
| Liposarcoma mixoide | FUS–DDIT3 | FISH / RT-PCR / NGS |
| DFSP | COL1A1–PDGFB | FISH / RT-PCR / NGS |
| Liposarcoma bien diferenciado/desdiferenciado | Amplificación MDM2 / CDK4 | FISH / NGS / IHQ (MDM2, CDK4) |
| Tumor de células gigantes | Mutación H3F3A (G34W) | IHQ (H3.3 G34W) / secuenciación |
| Tumor fibroso solitario (SFT) | NAB2–STAT6 | IHQ (STAT6 nuclear) / FISH / NGS |
Nota: son patrones típicos. La elección real depende de la sospecha diagnóstica, la muestra disponible y el objetivo clínico.
9) Mensajes prácticos para clínicos y pacientes
- ✓ No todo lo molecular cambia el tratamiento, pero a menudo cambia el diagnóstico y evita errores.
- ✓ En hueso, la descalcificación con ácidos fuertes puede degradar el ADN/ARN; avisar al laboratorio si se necesita estudio molecular.
- ✓ El mayor rendimiento diagnóstico llega cuando trabajan juntos: radiología + patología + clínica + biología molecular.
- ✓ En sospecha de sarcoma, el circuito debe ser especializado y la decisión tomarse en comité multidisciplinar.
- ✓ Los paneles amplios de NGS pueden generar hallazgos incidentales que requieren interpretación experta; no son una herramienta de cribado indiscriminado.
Resumen para la práctica clínica
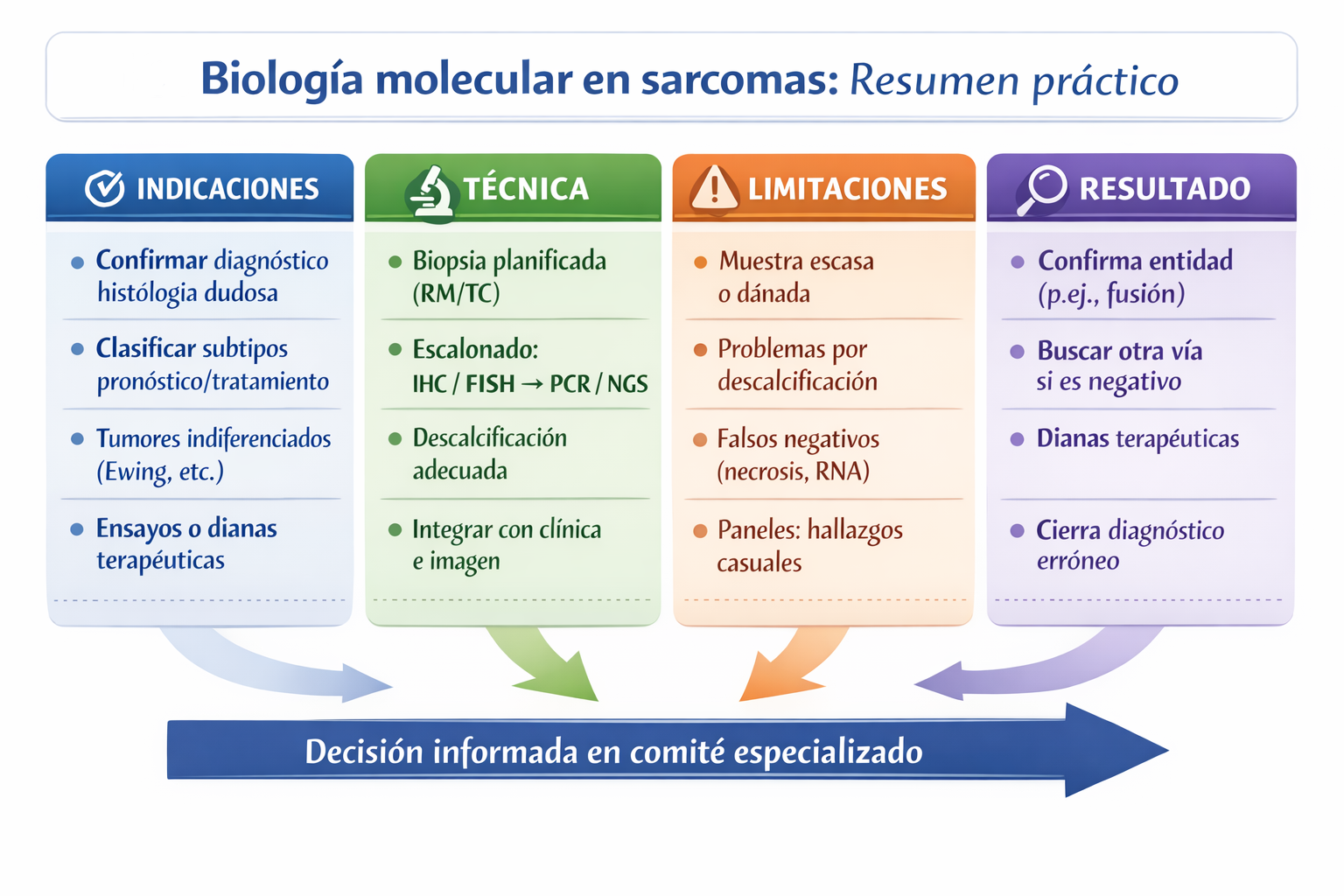
Indicaciones
- ✓ Confirmar diagnóstico cuando histología/IHQ no son concluyentes.
- ✓ Clasificar subtipos con implicación pronóstica o terapéutica.
- ✓ Tumores indiferenciados / de células pequeñas-redondas.
- ✓ Sospecha de amplificación (p. ej., MDM2).
- ✓ Casos con posible diana terapéutica o candidatos a ensayo.
Técnica
- 🔧 Definir pregunta clínica y seleccionar técnica según sospecha.
- 🔧 Elegir zona viable evitando necrosis/hemorragia.
- 🔧 Coordinar procesado en hueso (descalcificación y reserva de material).
- 🔧 Interpretar resultados integrando clínica, imagen y patología.
Riesgos
- ⚠️ Falsos negativos por muestra escasa, necrosis o baja calidad de ADN/ARN.
- ⚠️ Limitaciones por descalcificación agresiva (sobre todo para ARN).
- ⚠️ Hallazgos incidentales en paneles amplios: requieren interpretación experta.
- ⚠️ Retrasos si no se planifica el circuito.
Resultados
- ✅ Confirmación/descartar entidades clave (especialmente en sarcomas de fusión).
- ✅ Mejor clasificación y menor riesgo de error diagnóstico.
- ✅ En escenarios seleccionados, posibilidad de orientar dianas/ensayos.
- ✅ Plan clínico más sólido al afinar el 'apellido' del tumor.
10) Bibliografía actualizada (selección operativa)
Soft Tissue and Bone Tumours. 5th ed. IARC; 2020.
Soft Tissue Tumors. 7th ed. Elsevier; 2020.
Soft tissue and bone sarcomas. Ann Oncol. 2021.
Bone Cancer / Soft Tissue Sarcoma. Version 2.2026.
Diagnostic Molecular Pathology in Soft Tissue Tumors. Mod Pathol. 2024.
Molecular Pathology of Bone and Soft Tissue Tumors. Surg Pathol Clin. 2025.
Biología molecular en sarcomas
Diagnóstico · Clasificación · Dianas terapéuticas · Ensayos clínicos
